Viết các phương trình hoá học và ghi đầy đủ điều kiện khi cho hiđro phản ứng với:
a) clo ; b) lưu huỳnh ; c) brom.
Cho biết trạng thái của các chất tạo thành.
Câu 2: (3,5 điểm). Viết các phương trình hoá học (nếu có) và ghi đầy đủ điều kiện phản ứng trong các trường hợp sau:
a) Cho khí oxi tác dụng lần lượt với: Kali, magie, đồng, cacbon, phôtpho, bạc.
b) Cho khí hiđro dư đi qua các ống mắc nối tiếp, nung nóng, chứa lần lượt các chất: Al2O3 , FeO, CaO, BaO, Ag2O, P2O5
c) Cho dung dịch axit H2SO4 loãng tác dụng lần lượt với các chất: Nhôm, sắt, magie, đồng, kẽm, bạc.
Câu 2:
a, \(4K+O_2\underrightarrow{t^o}2K_2O\)
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(C+O_2\underrightarrow{t^o}CO_2\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
b, \(FeO+H_2\underrightarrow{t^o}Fe+H_2O\)
\(Ag_2O+H_2\rightarrow2Ag+H_2O\)
c, \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
Câu 2: (3,5 điểm). Viết các phương trình hoá học (nếu có) và ghi đầy đủ điều kiện phản ứng trong các trường hợp sau:
a) Cho khí oxi tác dụng lần lượt với: Kali, magie, đồng, cacbon, phôtpho, bạc.
b) Cho khí hiđro dư đi qua các ống mắc nối tiếp, nung nóng, chứa lần lượt các chất: Al2O3 , FeO, CaO, BaO, Ag2O, P2O5
c) Cho dung dịch axit H2SO4 loãng tác dụng lần lượt với các chất: Nhôm, sắt, magie, đồng, kẽm, bạc.
Từ hiđro, clo, nitơ và các hóa chất cần thiết, hãy viết các phương trình hóa học (có ghi rõ điều kiện phản ứng) điều chế phân đạm amoni clorua.
Hiđro clorua (HCl) là một chất khí được dùng để sản xuất axit clohiđric (một trong các axit được dùng phổ biến trong phòng thí nghiệm). Trong công nghiệp, hiđro clorua được điều chế bằng cách đốt khí hiđro trong khí clo. Tính thể tích khí clo (ở điều kiện tiêu chuẩn ) cần dùng để phản ứng vừa đủ với 67,2 lít khí hiđro ( ở đktc) và khối lượng khí hiđro clorua thu được sau phản ứng.
Nêu các bước giải bài toán theo phương trình hoá học.
b1: viết pthh
cl2+ h2-> 2hcl
b2: tính số mol cá chất dựa vào khối lượng hoăc thể tích đề bài cho
nH2= 67,2/224=3 mol
b3: dựa vào phương trình tính số mol các chất còn lại
theo pthh: ncl2=nh2=3 mol
nhcl=2nh2=3*2=6 mol
b4: tính khối lượng hoặc thể tích chất đề bài yêu cầu
=> Vcl2= 3*22,4=67,2l
mhcl=6* 36,5= 219g
CHÚC BẠN HỌC TỐT!
Bước 1: Tìm số mol chất đã cho trong đề bài.
nH2 = VH2/22,4 = 67,2/22,4 = 3 (mol)
Bước 2: Viết PTHH, cân bằng.
H2 + Cl2 -> 2HCl
Bước 3: Từ hệ số trong PTHH => số mol chất cần tìm.
3 mol -> 3 mol -> 6 mol
Bước 4: Tính theo yêu cầu đề bài.
- VCl2 = nCl2 . 22,4 = 3 . 22,4 = 67,2 (lít)
* Bài giải hoàn chỉnh:
- nH2 = VH2/22,4 = 67,2/22,4 = 3 (mol)
- H2 + Cl2 -> 2HCl
- 3 mol -> 3 mol -> 6 mol
- VCl2 = nCl2 . 22,4 = 3 . 22,4 = 67,2 (lít)
- mHCl = nHCl . MHCl = 6 . 36,5 = 219 (g)
Nếu bạn nào thắc mắc về câu trả lời của mk hay không hiểu chỗ nào, cứ việc bình luận. Mk sẽ nói rõ hơn! Mơn nhìu! >3<
Hiđro clorua (HCl) là một chất khí được dùng để sản xuất axit clohiđric (một trong các axit được dùng phổ biến trong phòng thí nghiệm). Trong công nghiệp, hiđro clorua được điều chế bằng cách đốt khí hiđro trong khí clo. Tính thể tích khí clo (ở điều kiện tiêu chuẩn ) cần dùng để phản ứng vừa đủ với 67,2 lít khí hiđro ( ở đktc) và khối lượng khí hiđro clorua thu được sau phản ứng.
Nêu các bước giải bài toán theo phương trình hoá học.
Có: nH2= 67,2:22,4=3(mol)
PTPƯ: H2 + Cl2 --to--> 2 HCl
(mol) 1 1 2
(mol) 3 3 6
(l) 67,2 67,2 134,4
(g) 6 213 219
Bước 1: Viet PTHH
H2 + Cl2 \(\rightarrow\) 2HCl
Bước 2: Ta tính số mol các chất đã cho theo gia thiết
Số mol H2 la
\(n_{H_2}=\)\(V_{H_2}\): 22,4= 67,2 : 22,4 = 3 (mol)
Bước 3: Dựa vào PTHH, ta có thể tính số mol các chất còn lại
Theo PTHH: \(n_{H_2=}2n_{HCl}=3\cdot2=6\left(mol\right)\)
Bước 4: Tính khối lượng (m) hay thể tích (V) các chất cần tìm.
Thể tích Cl cần dùng là
\(V_{Cl}=n_{Cl}\cdot22,4=3\cdot22,4=67,2\left(l\right)\)
Khối lượng HCl thu được là
\(m_{HCl}=M_{HCl}\cdot n_{HCl}=36,5\cdot6=219\left(g\right)\)
Chúc bạn học giỏi.![]()
Để điều chế một lượng khí hiđro một học sinh cho 13 gam Zn tác dụng vừa đủ với 3, gam axit clo hiđric
a, Viết phương trình phản ứng xảy ra
b, Tính thể tích khí hiđro thu được ở điều kiện tiêu chuẩn
Đề cho bao nhiêu gam axit clohidric bạn nhỉ?
a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{3}{36,5}=\dfrac{6}{73}\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{\dfrac{6}{73}}{2}\), ta được Zn dư.
Theo PT: \(n_{H_2}=\dfrac{1}{2}n_{HCl}=\dfrac{3}{73}\left(mol\right)\)
\(\Rightarrow V_{H_2}=\dfrac{3}{73}.22,4=\dfrac{336}{365}\left(l\right)\)
Cho a (g) kim loại natri tác dụng vừa đủ với 4,6(g) rượu etylic. Kết thúc phản ứng thu được natrietylic và v (1) khí hiđro ở điều kiện tiêu chuẩn viết phương trình hoá học và tính a và v
\(2Na+2C_2H_5OH\rightarrow2C_2H_5ONa+H_2\\ n_{C_2H_5OH}=\dfrac{4,6}{46}=0,1\left(mol\right)\\ n_{Na}=n_{C_2H_5OH}=0,1\left(mol\right)\\ n_{H_2}=\dfrac{0,1}{2}=0,05\left(mol\right)\\ a=m_{Na}=0,1.23=2,3\left(g\right)\\ V=V_{H_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\)
Viết các phương trình hóa học (ghi điều kiện phản ứng) khi:
a) Nhôm tác dụng với dung dịch HCl
b) Sắt tác dụng với khí clo
c) Đồng tác dụng với khi oxi
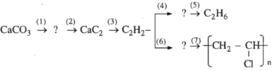
Viết phương trình hoá học của phản ứng thực hiện các biến hoá dưới đây và ghi rõ điều kiện phản ứng (nếu có).