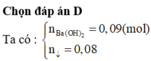Những câu hỏi liên quan
Hòa tan hoàn toàn 7,2 gam hỗn hợp A gồm 2 muối cacbonat của 2 kim loại kiềm thổ thuộc 2 chu kì liên tiếp bằng dd H2SO4 loãng thu đc khí B. Cho khí B hấp thụ hết vào 450 ml dd Ba(OH)2 0,2M thu đc 15,76gam kết tủa. Xác định tên 2 kim loại kiềm thổ trong hỗn hợp A ?
Hòa tan hoàn toàn 7,2 gam hỗn hợp A gồm 2 muối cacbonat của 2 kim loại kiềm thổ thuộc 2 chu kì liên tiếp bằng dd H2SO4 loãng thu đc khí B. Cho khí B hấp thụ hết vào 450 ml dd Ba(OH)2 0,2M thu đc 15,76gam kết tủa. Xác định tên 2 kim loại kiềm thổ trong hỗn hợp A ?
Đặt công thức chung của 2 muối trong A là MCO3
PTHH: MCO3 + H2SO4 ==> MSO4 + CO2 + H2O (1)
CO2 + Ba(OH)2 ==> BaCO3 + H2O (2)
2CO2 + Ba(OH)2 ==> Ba(HCO3)2 (3)
Ta có: +) nBaCO3 = \(\frac{15,76}{197}=0,08\left(mol\right)\)
+) nBa(OH)2 = 0,45 x 0,2 = 0,09 (mol)
=> nCO2 (PT2) = nBa(OH)2 (PT2) = 0,08 (mol)
=> nBa(OH)2 (PT3) = 0,09 - 0,08 = 0,01 (mol)
=> nCO2 (PT3) = 0,02 (mol)
\(\Rightarrow\sum n_{CO2}=0,08+0,02=0,1\left(mol\right)\)
=> nMCO3 = 0,1 (mol)
=> MMCO3 = \(\frac{7,2}{0,1}=72\left(\frac{g}{mol}\right)\)
=> MM = 12 (g/mol)
Vì 2 kiềm loại này thuộc 2 chu kì liên tiếp nhau và là kim loại kiềm thổ
=> 2 kim loại đó là Mg và Be
Đúng 0
Bình luận (0)
Một hỗn hợp A nặng 7,2 gam gồm 2 muối cacbonat của 2 kim loại kiềm thổ. Hoà tan hết A bằng
H
2
SO
4
loãng thu được khí B, cho B hấp thụ hết vào 450 ml dung dịch
Ba
OH
2
0,2M được 15,76 gam kết tủa. Nếu thêm nước vôi trong vào dung dịch sau phản ứng lại thấy có kết tủa xuất hiện. Kim loại chắc chắn có mặt trong hỗn hợp A là A. Be B. Mg C. Ca D. Sr
Đọc tiếp
Một hỗn hợp A nặng 7,2 gam gồm 2 muối cacbonat của 2 kim loại kiềm thổ. Hoà tan hết A bằng H 2 SO 4 loãng thu được khí B, cho B hấp thụ hết vào 450 ml dung dịch Ba OH 2 0,2M được 15,76 gam kết tủa. Nếu thêm nước vôi trong vào dung dịch sau phản ứng lại thấy có kết tủa xuất hiện. Kim loại chắc chắn có mặt trong hỗn hợp A là
A. Be
B. Mg
C. Ca
D. Sr
Hòa tan hoàn toàn 7,2 gam hỗn hợp A gồm 2 muối cacbonat của 2 kim loại kiềm thổ thuộc 2 chu kì liên tiếp bằng dd H2SO4 loãng thu đc khí B. Cho khí B hấp thụ hết vào 450 ml dd Ba(OH)2 0,2M thu đc 15,76gam kết tủa. Xác định tên 2 kim loại kiềm thổ trong hỗn hợp A ?![]() giúp với
giúp với
Hòa tan hoàn toàn 7,2 gam hỗn hợp A gồm 2 muối cacbonat của 2 kim loại kiềm thổ thuộc 2 chu kì liên tiếp bằng dd H2SO4 loãng thu đc khí B. Cho khí B hấp thụ hết vào 450 ml dd Ba(OH)2 0,2M thu đc 15,76gam kết tủa. Xác định tên 2 kim loại kiềm thổ trong hỗn hợp A ?
Đặt công thức chung của hai muối cacbonat là MCO3MCO3
M cũng là KLNTTB của hai kim loại IIA kế tiếp.
Phản ứng: MCO3+H2SO4→MSO4+CO2+H2OMCO3+H2SO4→MSO4+CO2+H2O (1)(1)
Khí B là CO2(nCO2−nMCO3)CO2(nCO2−nMCO3) tác dụng dung dịch Ba(OH)2Ba(OH)2 tạo kết tủa.
Có thể có hai phản ứng: CO2+Ba(OH)2→BaCO3+H2OCO2+Ba(OH)2→BaCO3+H2O (2)(2)
Có thể: 2CO2+Ba(OH)2→Ba(HCO3)22CO2+Ba(OH)2→Ba(HCO3)2 (3)(3)
Có hai trường hợp :
Trường hợp (1)(1): Ba(OH)2Ba(OH)2 dư chỉ có phản ứng (2)(2) xảy ra
nCO2=nBa(OH)2=15,76197=0,08mol⇒MCO3=7,20,08=90⇒M=30nCO2=nBa(OH)2=15,76197=0,08mol⇒MCO3=7,20,08=90⇒M=30
⇒⇒ hai kim loại kế tiếp nhau là Mg=24<30<Ca=40Mg=24<30<Ca=40
Công thức hai muối: MgCO3(x)mol,CaCO3(y)molMgCO3(x)mol,CaCO3(y)mol
Có hệ phương trình: Tổng mol hỗn hợp: x+y=0,08x+y=0,08 ; Tổng khối lượng hỗn hợp: 84x+100y=7,284x+100y=7,2
⇒MgCO3=84.0,057,2.100%=58,33%;%CaCO3=41,67%⇒MgCO3=84.0,057,2.100%=58,33%;%CaCO3=41,67%
Trường hợp (2)(2) : Ba(OH)2Ba(OH)2 phản ứng hết 0,45.0,2=0,09mol0,45.0,2=0,09mol (2)(2) phản ứng (2)(2) (3)(3) xảy ra:
nCO2nCO2(2)=0,08;nCO2=0,08;nCO2(3)=2nBa(OH)2=2.0,01=0,02=2nBa(OH)2=2.0,01=0,02
⇒nMCO3=nCO2=0,08+0,02=0,1⇒M=12⇒nMCO3=nCO2=0,08+0,02=0,1⇒M=12
Hai muối BeCO3;MgCO3BeCO3;MgCO3
%BeCO3=76,67%;%MgCO3=23,33%%BeCO3=76,67%;%MgCO3=23,33%
Đúng 0
Bình luận (5)
Hòa 7.2g hh A gồm 2 muối cacbonat của 2 KL thuộc phân nhóm chính nhóm II (nhóm 2A) thuộc 2 chu kỳ kế tiếp trong bang tuần hoàn bằng dd H2SO4 loãng thu được khí B. Cho B hấp thụ hết vào 450ml dd Ba(OH)2 0.2M thu được 15.76g kết tủa. Xác định tên 2 kim loại
gọi công thức 2 muối cacbonat là : MCO3
MCO3 + H2SO4 -> MSO4 + H2O + CO2(1)
CO2 + Ba(OH)2 -> BaCO3 + 2H2O (2)
CO2 + BaCO3 + H2O -> Ba(HCO3)2(3)
nBaCO3=15,76/197=0,08 mol
nBa(OH)_2=O,2*0,45=0,09 mol
từ 1,2,3 => nCO_2=0,09+(0,09-0,08)=0,1 mol
=> MCO_3=7,2/0,1=72=>M=12
=>2 muối cacbonat là: MgCO3 và BeCO3
Đúng 1
Bình luận (0)
gọi công thức 2 muối cacbonat là : MCO3
MCO3 + H2SO4 -> MSO4 + H2O + CO2(1)
CO2 + Ba(OH)2 -> BaCO3 + 2H2O (2)
CO2 + BaCO3 + H2O -> Ba(HCO3)2(3)
nBaCO3=15,76/197=0,08 mol
nBa(OH)_2=O,2*0,45=0,09 mol
từ 1,2,3 => nCO_2=0,09+(0,09-0,08)=0,1 mol
=> MCO_3=7,2/0,1=72=>M=12
=>2 muối cacbonat là: MgCO3 và BeCO3
Đúng 2
Bình luận (0)
Cho 7,2 gam hỗn hợp X gồm hai muối cacbonat của hai kim loại kế tiếp nhau M, R trong nhóm IIA (M R) tác dụng với dung dịch HCl dư. Hấp thụ toàn bộ khí CO2 sinh ra vào 450 ml dung dịch Ba(OH)2 0,2M thu được 15,76 gam kết tủa. Khối lượng mol lớn nhất có thể đạt của M là A. 9 (Be). B. 24 (Mg). C. 40 (Ca). D. 88 (Sr).
Đọc tiếp
Cho 7,2 gam hỗn hợp X gồm hai muối cacbonat của hai kim loại kế tiếp nhau M, R trong nhóm IIA (M < R) tác dụng với dung dịch HCl dư. Hấp thụ toàn bộ khí CO2 sinh ra vào 450 ml dung dịch Ba(OH)2 0,2M thu được 15,76 gam kết tủa. Khối lượng mol lớn nhất có thể đạt của M là
A. 9 (Be).
B. 24 (Mg).
C. 40 (Ca).
D. 88 (Sr).
Đáp án B
7,2 gam MCO3 + HCl → CO2 + 0,09 mol Ba(OH)2 → 0,08 mol BaCO3↓
• CO2 + Ba(OH)2 → BaCO3↓ + H2O(*)
BaCO3 + CO2 + H2O → Ba(HCO3)2 (**)
Theo (*) nCO2(*) = 0,09 mol; nBaCO3 (*) = 0,09 mol
Theo (**) nBaCO3 (**) dư = 0,08 mol → nBaCO3 (**) phản ứng = 0,09 - 0,08 = 0,01 mol
→ nCO2 (**) = 0,01 mol → ∑nCO2 = 0,1 mol
• MCO3 + 2HCl → MCl2 + CO2 + H2O
nMCO3 = nCO2 = 0,1 mol → MMCO3 = 7,2 : 0,1 = 72 → MM = 12 → Be và Mg (9 < 20 < 24)
Đúng 0
Bình luận (0)
Một hỗn hợp A có khối lượng là 19,1g gồm 2 muối cacbonat của 2 kim loại kìm thuộc 2 chu kì kế tiếp nhau trong bảng hệ thống tuần hoàn. Hòa tan hết A trong dung dịch HCl thu được khí B. Hấp thụ hoàn toàn khí B trong 700ml dung dịch Ba(OH)2 0,5M thu được 29,55g kết tủa a) Xác định công thức của 2 muối cacbonatb) Tính thành phần phần trăm theo khối lượng của mỗi muối trong hỗn hợp A
Đọc tiếp
Một hỗn hợp A có khối lượng là 19,1g gồm 2 muối cacbonat của 2 kim loại kìm thuộc 2 chu kì kế tiếp nhau trong bảng hệ thống tuần hoàn. Hòa tan hết A trong dung dịch HCl thu được khí B. Hấp thụ hoàn toàn khí B trong 700ml dung dịch Ba(OH)2 0,5M thu được 29,55g kết tủa
a) Xác định công thức của 2 muối cacbonat
b) Tính thành phần phần trăm theo khối lượng của mỗi muối trong hỗn hợp A
Gọi CT dạng chung của 2 muối cacbonat là \(M_2CO3\)
\(M2CO3+2HCl\rightarrow2MCl+H2O+CO2\)
Ta có: \(n_{Ba\left(OH\right)2}=0,7.0,5=0,35\left(mol\right)\)
\(n_{BaCO3}=\dfrac{29,55}{ }=0,15\left(mol\right)\)
=>TH1: Ba(OH)2 dư=> tạo 1 muối trung hoà
\(CO2+Ba\left(OH\right)2\rightarrow BaCO3+H2O\)
\(n_{CO2}=n_{BaCO3}=0,15\left(mol\right)\)
\(n_{M2CO3}=n_{CO2}=0,15\left(mol\right)\)
\(M_{M2CO3}=\dfrac{19,1}{0,15}=127,3\)
\(\Rightarrow M_M=\dfrac{127,3-12-16.3}{2}=33,65\)
=> 2 muối cacbonat là \(Na2CO3\) và K2CO3
Gọi \(n_{Na2CO3}=a\left(mol\right),n_{K2CO3}=b\left(mol\right)\)
khi đó:
\(\left\{{}\begin{matrix}106a+138b=19,1\\a+b=0,15\left(theo-CO2\right)\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}a=0,05\\b=0,1\end{matrix}\right.\)
\(\%m_{Na2CO3}=\dfrac{0,05.106}{19,1}.100\%=27,75\%\)
\(\%m_{K2CO3}=100-27,75=72.25\%\)
TH2: CO2 dư=>tạo 2 muối
\(CO2+Ba\left(OH\right)2\rightarrow BaCO3+H2O\)
0,15<---0,15<-----------0,15(mol)
\(\Rightarrow n_{Ba\left(OH\right)2}\)còn lại\(=0,25-0,15=0,2\left(mol\right)\)
\(2CO2+Ba\left(OH\right)2\rightarrow Ba\left(HCO3\right)2\)
0,4<-------0,2(mol)
\(\Rightarrow n_{M2CO3}=n_{CO2}=0,4\left(mol\right)\)
\(M_{M2CO3}=\dfrac{19,1}{0,4}=47,45\)
\(\Rightarrow M_M=\dfrac{47,45-12-16.3}{2}=-6,125\)
=> LOẠI
Chúc bạn học tốt^^
Đúng 2
Bình luận (1)
Cho 7,2 gam hỗn hợp A gồm hai muối cacbonat của hai kim loại kế tiếp nhau trong nhóm IIA tác dụng với dung dịch HCl dư. Hấp thụ khí CO2 vào 450ml dung dịch Ba(OH)2 0,2M thu được 15,76 gam kết tủa. Xác định công thức 2 muối A. BeCO3 và MgCO3 B. MgCO3 và CaCO3 C. CaCO3 và SrCO3 D.Đáp án khác
Đọc tiếp
Cho 7,2 gam hỗn hợp A gồm hai muối cacbonat của hai kim loại kế tiếp nhau trong nhóm IIA tác dụng với dung dịch HCl dư. Hấp thụ khí CO2 vào 450ml dung dịch Ba(OH)2 0,2M thu được 15,76 gam kết tủa. Xác định công thức 2 muối
A. BeCO3 và MgCO3
B. MgCO3 và CaCO3
C. CaCO3 và SrCO3
D.Đáp án khác