Đốt cháy 10 cm3 khí hiddro trong 10 cm3 khí oxi. Thể tích chất khí còn lại sau phản ứng :
Đốt cháy 10 c m 3 khí hidro trong 10 c m 3 khí oxi. Thể tích chất khí còn lại sau phản ứng:
A. 5 c m 3 hidro B. 10 c m 3 hidro
C. Chỉ có 10 c m 3 hơi nước D. 5 c m 3 oxi
Tìm câu trả lời đúng, biết các thể tích khí đo cùng ở 100 0 C và áp suất khí quyển.
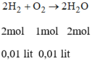
* Chú ý: cùng đktc: tỉ lệ số mol = tỉ lệ thể tích
Tỉ số mol của H 2 và O 2 :
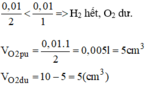
Chọn D
Đốt 10 cm3 một hiđrocacbon bằng 70 cm3 oxi (lấy du), thu được 90 cm3 sản phẩm khí và hơi. Dẫn sản phẩn khí qua bình đụng Ca(OH)2 (dư), thi còn lại 20 cm3 khí thoát ra. Các thể tích khí đo trong cùng điều kiện. CTPT của hiđrocacbon là
\(20cm^3\) khí thoát ra là \(O_2\)
\(\Rightarrow V_{O_2\left(d\text{ư}\right)}=20\left(cm^3\right)\Rightarrow\left\{{}\begin{matrix}V_{O_2\left(p\text{ư}\right)}=70-20=50\left(cm^3\right)\\V_{CO_2}+V_{H_2O}=90-20=70\left(cm^3\right)\end{matrix}\right.\)
Đặt CTPT của hiđrocacbon là \(C_xH_y\left(x,y\in N\text{*}\right)\)
Vì các khí đo ở cùng điều kiện nên tỉ lệ thể tích cũng là tỉ lệ mol
\(\Rightarrow n_{C_xH_y}:n_{O_2}:\left(n_{CO_2}+n_{H_2O}\right)=V_{C_xH_y}:V_{O_2}:\left(V_{CO_2}+V_{H_2O}\right)=10:50:70=1:5:7\)
\(\Rightarrow\left\{{}\begin{matrix}n_{CO_2}+n_{H_2O}=7n_{C_xH_y}\\n_{O_2}=5n_{C_xH_y}\end{matrix}\right.\)
PTHH: \(C_xH_y+\left(x+\dfrac{y}{4}\right)O_2\xrightarrow[]{t^o}xCO_2+\dfrac{y}{2}H_2O\)
\(\Rightarrow\left\{{}\begin{matrix}x+\dfrac{y}{2}=7\\x+\dfrac{y}{4}=5\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=3\\y=8\end{matrix}\right.\left(TM\right)\)
Vậy CTPT của hiđrocacbon là \(C_3H_8\)
Trộn 200 cm3 hỗn hợp chất hữu cơ X và nitơ với 450 cm3 khí oxi dư rồi đốt. Hỗn hợp sau khi đốt cháy có thể tích là 0,7 lít. Sau khi cho hơi nước ngưng tụ thì còn 400 cm3, tiếp tục cho qua dung dịch NaOH thì còn lại 200 cm3. Công thức phân tử của chất X là:
A. C2H4
B. CH4
C. C2H6
D. C3H8
Đáp án C
Quan sát 4 đáp án ta có công thức của X có dạng CxHy
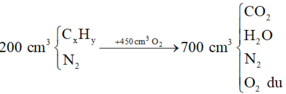
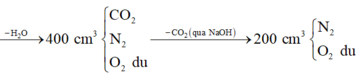
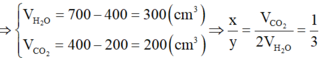
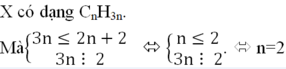
![]()
Câu 8: Để đốt cháy 1 kg than có chứa 85% C, 10% S còn lại là tạp chất không cháy, thì:
a- Cần dùng hết bao nhiêu lít khí oxi đktc? Bao nhiêu lít kk
b- Tính thể tích khí CO 2 thu được trong không khí sau phản ứng, biết trong không khí trước
phản ứng có 78% khí nito, 20 % khí oxi, 2% khí cacbonic?( giả thiết phản úng xảy ra
trong bình không khí kín)
Bạn tham khảo tại đây nhé
https://sites.google.com/site/hoahocquan10/bai-tap/bai-tap-hoa-8/hoa-8-chuong-iv
Cho không khí (chứa 80% thể tích là khí nito tác dụng với đồng nung nóng trong thiết bị kín, xảy ra phản ứng oxi hóa đồng thành đồng (II) oxit. Phản ứng xong, người ta thu được 160 c m 3 khí nito. Thể tích không khí trong thiết bị trước khi xảy ra phản ứng là:
A. 200 c m 3 B.400 c m 3 .
C. 300 c m 3 D. 500 c m 3 .
(Các thể tích khí đo ở đktc)
Trong không khí chứa 80% thể tích là khí nito
Vậy thể tích của không khí trong thiết bị trước khi xảy ra phản ứng:
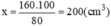
⇒ Chọn A.
1. Trong bình đốt khí người ta dung tia lửa điện để đốt một hỗn hợp gồm60 cm3 gồm khí hiđro và khí oxi.
a) Sau phản ứng còn thừa khí nào không? Thừa bao nhiêu cm3?
b) Tính thể tích và khối lượng hơi nước thu được? (Biết các thể tích khí và hơi đo ở đktc).
2. Để hòa tan hoàn toàn 4 gam hỗn hợp A gồm oxit của Đồng (II) và Sắt (III) cần vừa đủ 25,55 gam dung dịch HCl 20%.
a) Tính khối lượng từng chất trong hỗn hợp A.
b) Nếu đem hỗn hợp A nung nóng trong ống sứ rồi dẫn khí CO đi qua, trong điều kiện thí nghiệm thấy cứ 4 phân tử chất rắn mỗi loại tham gia phản ứng thì có 1 phân tử không tham gia phản ứng. Xác định thành phần và khối lượng chất rắn thu được sau phản ứng trong ống sứ?
Bài 16: Đốt cháy 24 gam kim loại Magie trong không khí, sau khi phản ứng thu được 32 gam magie oxit. Giả sử oxi chiếm 20% thể tích không khí, còn lại là nitơ.
a) Tính thể tích không khí (ở đktc) dùng để đốt cháy Magie.
b) Tính hiệu suất phản ứng.
giúp mình
1 mẩu kim loại Mg có lẫn tạp chất trơ( không tham gia phản ứng). đốt cháy 20 gam kim loại đó trong không khí sau khi phản ứng hoàn toàn thu được 32 g Magie oxit .Giả sử oxi chiếm 20% thể tích không khí còn lại là Nitơ
a Tính thể tích không khí đủ dùng để đốt cháy( điều kiện tiêu chuẩn)
b tính phần trăm theo khối lượng của Mg trong mẩu kim loại nói trên
a)a)nMgO=\(\dfrac{32}{40}\)=0,8(mol)
PT:2Mg+O2to→2MgO
⇒nO2=\(\dfrac{0,8}{2}\)=0,4(mol)
⇒VO2=0,4.22,4=8,96(l)
⇒Vkk=8,96:20%=44,8(l)
b)b)nMg=nMgO=0,8(mol)
⇒mMg=24.0,8=19,2(g)
%mMg=\(\dfrac{19,2}{20}\).100%=96%
a) Số mol magie oxit là 32/40=0,8 (mol).
2Mg (0,8 mol) + O2 (0,4 mol) \(\underrightarrow{t^o}\) 2MgO (0,8 mol).
Thể tích không khí đủ dùng để đốt cháy là:
V=0,4.22,4:20%=44,8 (lít).
b) Khối lượng kim loại Mg đã phản ứng là 0,8.24=19,2 (g).
Phần trăm theo khối lượng của Mg trong mẩu kim loại nói trên:
%mMg=19,2/20=96%.
Trộn 30cm khối hiddro ở thể khí với 210cm3 khí trong bình oxi. Đốt hỗn hợp khí, phản ứng xong đưa hỗn hợp khí trên về các điều kiện ban đầu. Nhận thấy trong bình còn 165cm3 khí, trong đó có 120cm3 là khí CO2 còn lại là khí oxi. Xác định công thức phân tử và viết công thức cấu tạo của hiđrocacbon này (giúp em với ạ, em đang cần gấp ạ)
30cm3 ban đầu là hidro hay hidrocacbon em?