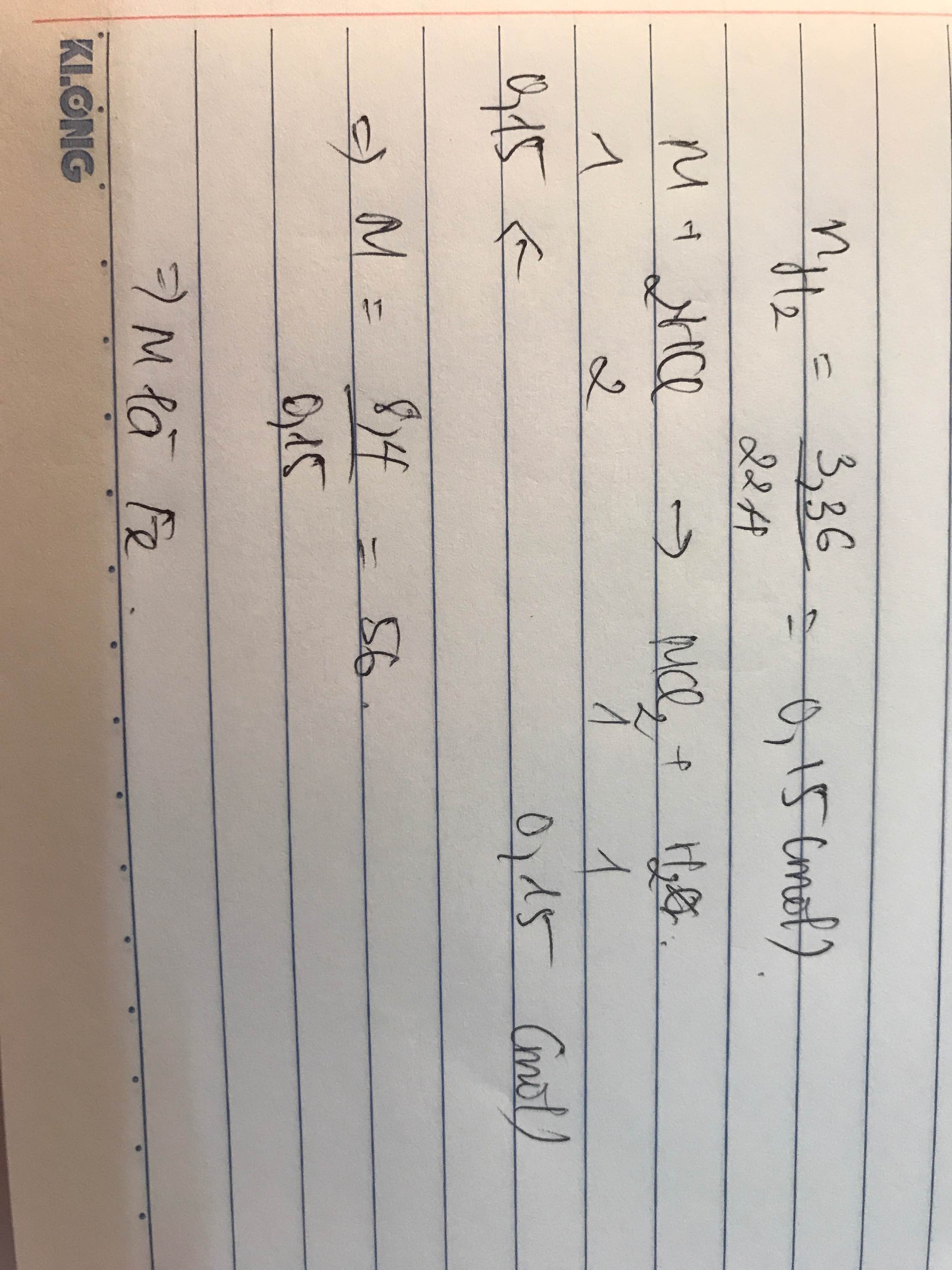Hòa tan hoàn toàn 9,4g Kali oxit vào nước thu được 500ml dung dịch A.
a. Xác định CM dung dịch A
b. Cần phải dùng bao nhiêu g dung dịch H2SO4 9,8% để trung hòa hoàn toàn 500ml dung dịch A

Những câu hỏi liên quan
Hòa tan hoàn toàn 30,6 gam BaO vào nước thu được 200 ml dung dịch A.
a. Tính nồng độ mol của dung dịch A.
b. Tính thể tích dung dịch HCl 0,5M cần dùng để trung hòa hết 200 ml dung dịch A.
a)
$BaO + H_2O \to Ba(OH)_2$
$n_{Ba(OH)_2} = n_{BaO} = \dfrac{30,6}{153} = 0,2(mol)$
$C_{M_{Ba(OH)_2}} = \dfrac{0,2}{0,2} = 1M$
b)
$Ba(OH)_2 + 2HCl \to BaCl_2 + 2H_2O$
$n_{HCl} = 2n_{Ba(OH)_2} = 0,4(mol)$
$V_{dd\ HCl} = \dfrac{0,4}{0,5} = 0,8(lít)$
Đúng 4
Bình luận (0)
cho 8,4 gam một kim loại M hóa trị II vào dung dịch HCl 10% dư. Sau khi kim loại hòa tan hoàn toàn thu được 3,36 lít khí đo ở đktc và dung dịch A.
a. Xác định kim loại M
b.Để phản ứng hết dung dịch A cần 500ml dung dịch NaOH 1M. Tính nồng độ phần trăm các chất trong dung dịch A
dạ em làm xong câu B rồi mọi người khỏi cần trả lời nữa ạ
Đúng 0
Bình luận (2)
hòa tan hoàn toàn hỗn hợp A chứa: 9,4g K2O và 4g MgO vào 200g dung dịch H2SO4. Để trung hòa axit dư phải:
1) C% dung dịch H2SO4 đem dùng
2) C% từng muối dung dịch có trong dung dịch sau khi hòa tan hỗn hợp A
giúp mình với
\(1)n_{K_2O}=\dfrac{9,4}{94}=0,1mol;n_{MgO}=\dfrac{4}{40}=0,1mol\\ K_2O+H_2SO_4\rightarrow K_2SO_4+H_2O\\ MgO+H_2SO_4\rightarrow MgSO_4+H_2O\\ n_{H_2SO_4}=0,1+0,1=0,2mol\\ C_{\%H_2SO_4}=\dfrac{0,2.98}{200}\cdot100=9,8\%\\ 2)n_{K_2SO_4}=n_{K_2O}=n_{MgSO_4}=n_{MgO}=0,1mol\\ C_{\%K_2SO_4}=\dfrac{0,1.174}{9,4+4+200}\cdot100=8,2\%\\ C_{\%MgSO_4}=\dfrac{0,1.120}{9,4+4+200}\cdot100=5,6\%\)
Đúng 2
Bình luận (0)
Bài 6: Hòa tan hoàn toàn m gam hỗn hợp X gồm 4 oxit bazơ cần dùng vừa đúng 1,6 lít dung dịch H2SO4 0,5M thu được dung dịch Y chứa 4 muối sunfat trung hòa. Cô cạn dung dịch Y được 107,4g muối khan. Xác định giá trị m?Bài 7: Để trung hòa V ml dung dịch X gồm HCl 1M và H2SO4 0,5M thì cần 200 ml dung dịch Ba(OH)2 1M thu được m gam kết tủa, dung dịch Y. a) Tính V, m. b) Tính khối lượng muối khan thu được khi cô cạn dung dịch Y.Bài 8: Cho 2,88 gam một kim loại X có hóa trị không đổi tác dụng với 300 m...
Đọc tiếp
Bài 6: Hòa tan hoàn toàn m gam hỗn hợp X gồm 4 oxit bazơ cần dùng vừa đúng 1,6 lít dung dịch H2SO4 0,5M thu được dung dịch Y chứa 4 muối sunfat trung hòa. Cô cạn dung dịch Y được 107,4g muối khan. Xác định giá trị m?
Bài 7: Để trung hòa V ml dung dịch X gồm HCl 1M và H2SO4 0,5M thì cần 200 ml dung dịch Ba(OH)2 1M thu được m gam kết tủa, dung dịch Y. a) Tính V, m. b) Tính khối lượng muối khan thu được khi cô cạn dung dịch Y.
Bài 8: Cho 2,88 gam một kim loại X có hóa trị không đổi tác dụng với 300 ml dung dịch HCl 1M thu được dung dịch A. Để trung hòa vừa đủ trong dung dịch A cần 60 ml dung dịch NaOH 1M. Xác định tên kim loại X.
Bài 6 :
Bảo toàn nguyên tố H :
$n_{H_2O} = n_{H_2SO_4} =1,6.0,5 = 0,8(mol)$
Bảo toàn khối lượng :
$m = 107,4 + 0,8.18 - 0,8.98 = 43,4(gam)$
Bài 7 :
$Ba(OH)_2 + 2HCl \to BaCl_2 + 2H_2O$
$Ba(OH)_2 + H_2SO_4 \to BaSO_4 + 2H_2O$
$n_{HCl} = 0,001V(mol) ; n_{H_2SO_4} = 5.10^{-4}V(mol)$
Theo PTHH :
$n_{Ba(OH)_2} = \dfrac{0,001}{2} + 5.10^{-4}V = 10^{-3}V = 0,2$
$\Rightarrow V = 200(ml)$
$n_{BaSO_4} = n_{H_2SO_4} = 0,1(mol)$
$m = 0,1.233 = 23,3(gam)$
b)
$n_{BaCl_2} = \dfrac{1}{2}n_{HCl} = 0,1(mol)$
$m_{BaCl_2} = 0,1.208 = 20,8(gam)$
Đúng 2
Bình luận (0)
Câu 8 :
$n_{HCl} = 0,3(mol)$
$HCl + NaOH \to NaCl + H_2O$
$n_{HCl\ dư} = n_{NaOH} = 0,06(mol)$
$\Rightarrow n_{HCl\ pư} = 0,3 - 0,06 = 0,24(mol)$
Gọi n hóa trị của X
$2X + 2nHCl \to 2XCl_n + nH_2$
Theo PTHH :
$n_X = \dfrac{1}{n}.n_{HCl} = \dfrac{0,24}{n}(mol)$
$\Rightarrow \dfrac{0,24}{n}.X = 2,88 \Rightarrow X = 12n$
Với n = 2 thì $X = 24(Magie)$
Đúng 2
Bình luận (0)
Hòa tan 54,44 gam hỗn hợp X gồm PCl3 và PBr3 vào nước được dung dịch Y. Để trung hòa hoàn toàn Y cần dùng 500ml dung dịch KOH 2,6M. Tính % khối lượng của PCl3 trong X là: A. 26,96% B. 12,125% C. 8,08% D. 30,31%
Đọc tiếp
Hòa tan 54,44 gam hỗn hợp X gồm PCl3 và PBr3 vào nước được dung dịch Y. Để trung hòa hoàn toàn Y cần dùng 500ml dung dịch KOH 2,6M. Tính % khối lượng của PCl3 trong X là:
A. 26,96%
B. 12,125%
C. 8,08%
D. 30,31%
Đáp án D
Hướng dẫn giải:
Gọi số mol PCl3 là x mol; số mol PBr3 là y mol
Phương trình phản ứng :
PCl3 + 3H2O → H3PO3+ 3HCl
x x 3x mol
PBr3+ 3H2O → H3PO3+ 3HBr
y y 3y mol
Dung dịch Y phản ứng với KOH
HX + KOH → KX + H2O
(3x+3y)
H3PO3 + 2KOH → K2HPO3 + 2H2O
(x+y) 2(x+y) mol
Ta có 137,5x + 271 y= 54,44; nKOH= 5x + 5y= 1,3 mol
Giải hệ trên ta có x= 0,12 và y= 0,14
%mPCl3= 30,31%
Đúng 0
Bình luận (0)
Khử một oxit sắt bằng khí CO trong binh kín sau khi phản ứng kết thúc thu được chất rắn A và hỗn hợp khí B. Hòa tan chất rắn A trong 300g dung dịch axit H2SO4 49%, để kết tủa hoàn toàn dung dịch muối thu được cần dùng 500ml dung dịch Ba(OH)2 3M, đem kết tủa nung đến khối lượng không đổi thu được 376,5 g chất rắn. Mặt khác dẫn hỗn hợp khí B qua 500ml dung dịch Ca(OH)2 3,5M thì thu được 150 g kết tủa. Tìm công thức hóa học và tên gọi oxit sắt.
Đọc tiếp
Khử một oxit sắt bằng khí CO trong binh kín sau khi phản ứng kết thúc thu được chất rắn A và hỗn hợp khí B. Hòa tan chất rắn A trong 300g dung dịch axit H2SO4 49%, để kết tủa hoàn toàn dung dịch muối thu được cần dùng 500ml dung dịch Ba(OH)2 3M, đem kết tủa nung đến khối lượng không đổi thu được 376,5 g chất rắn. Mặt khác dẫn hỗn hợp khí B qua 500ml dung dịch Ca(OH)2 3,5M thì thu được 150 g kết tủa. Tìm công thức hóa học và tên gọi oxit sắt.
Hòa tan 54,44 gam hỗn hợp X gồm PCl3 và PBr3 vào nước được dung dịch Y. Để trung hòa hoàn toàn dung dịch Y cần 500ml dung dịch KOH 2,6M. Tỷ lệ % khối lượng của PCl3 trong X là A. 8,08% B. 26,96% C. 30,31% D. 12,125%
Đọc tiếp
Hòa tan 54,44 gam hỗn hợp X gồm PCl3 và PBr3 vào nước được dung dịch Y. Để trung hòa hoàn toàn dung dịch Y cần 500ml dung dịch KOH 2,6M. Tỷ lệ % khối lượng của PCl3 trong X là
A. 8,08%
B. 26,96%
C. 30,31%
D. 12,125%
Hòa tan hoàn toàn 8 gam một kim loại A nhóm IIA vào 500ml nước thu được dung dịch X và 4,48 lít khí (đktc).
a. Xác định tên kim loại A.
b. Tính nồng độ mol/l dung dịch X
a) \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: A + 2H2O --> A(OH)2 + H2
0,2<--------------0,2<-----0,2
=> \(M_A=\dfrac{8}{0,2}=40\left(g/mol\right)\)
=> A là Ca (Canxi)
b) \(C_M=\dfrac{0,2}{0,5}=0,4M\)
Đúng 5
Bình luận (0)
1. Hòa tan hoàn toàn 16,2(g) kẽm oxit trong 196(g) dung dịch H2SO4 12% sau phản ứng thu được dung dịch X. Tính C% các chất có trong dung dịch X?2. Hòa tan hoàn toàn 16(g) CuO trong 245(g) dung dịch H2SO4 12% sáu phản ứng thu được dung dịch A?3. Hòa tan 16(g) NaOH(rắn) vào nước được 200ml dung dịch NaOH có nồng độ a(M).a) Tìm a?b) Phải thêm vào dung dịch trên bao nhiêu ml nước để thu được dung dịch NaOH 0,5(M)
Đọc tiếp
1. Hòa tan hoàn toàn 16,2(g) kẽm oxit trong 196(g) dung dịch H2SO4 12% sau phản ứng thu được dung dịch X. Tính C% các chất có trong dung dịch X?
2. Hòa tan hoàn toàn 16(g) CuO trong 245(g) dung dịch H2SO4 12% sáu phản ứng thu được dung dịch A?
3. Hòa tan 16(g) NaOH(rắn) vào nước được 200ml dung dịch NaOH có nồng độ a(M).
a) Tìm a?
b) Phải thêm vào dung dịch trên bao nhiêu ml nước để thu được dung dịch NaOH 0,5(M)