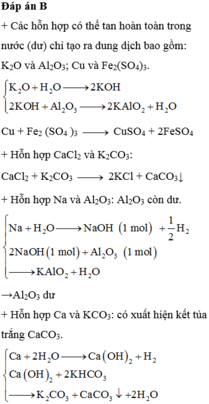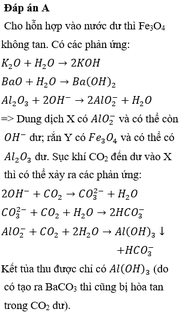cho hỗn hợp rắn gồm K2O;BaO;Al2O3. Viết cac phương trình hoá học điền chế K,Ba,Al từ hộn hợp trên sao cho khối lượng từng kim loại không đổi

Những câu hỏi liên quan
Cho hỗn hợp rắn gồm K2o, BaO, Al2O3 . Hãy tách K, Ba, Al ra khỏi hỗn hợp trên sao cho khối lượng từng kim loại không đổi
Cho năm hỗn hợp, mỗi hỗn hợp gồm hai chất rắn có số mol bằng nhau: K2O và Al2O3; Cu và Fe2(SO4)3; CaCl2 và K2CO3; Na và Al2O3; Ca và KHCO3. Số hỗn hợp có thể tan hoàn toàn trong nước (dư) chỉ tạo ra dung dịch là A. 1. B. 2. C. 3. D. 4.
Đọc tiếp
Cho năm hỗn hợp, mỗi hỗn hợp gồm hai chất rắn có số mol bằng nhau: K2O và Al2O3; Cu và Fe2(SO4)3; CaCl2 và K2CO3; Na và Al2O3; Ca và KHCO3. Số hỗn hợp có thể tan hoàn toàn trong nước (dư) chỉ tạo ra dung dịch là
A. 1.
B. 2.
C. 3.
D. 4.
Đề Bài: Cho hỗn A gồm 3 oxit: Al2O3, CuO và K2O. Tiến hành 3 thí nghiệm:- Thí nghiệm 1: nếu cho hỗn hợp A vào nước dư, khuấy kĩ thấy còn 15g chất rắn không tan.- Thí nghiệm 2: Nếu cho thêm vào hỗn hợp A một lượng Al2O3 bằng 50% lượng Al2O3 trong A ban đầu rồi lại hòa tan vào nước dư. Sau thí nghiệm còn lại 21g chất rắn không tan.- Thí nghiệm 3: Nếu cho vào hỗn hợp A một lượng Al2O3 bằng 75% lượng Al2O3 trong A, rồi lại hòa tan vào nước dư, thấy còn lại 25g chất rắn không tan.Tính khối lượng oxit...
Đọc tiếp
Đề Bài: Cho hỗn A gồm 3 oxit: Al2O3, CuO và K2O. Tiến hành 3 thí nghiệm:
- Thí nghiệm 1: nếu cho hỗn hợp A vào nước dư, khuấy kĩ thấy còn 15g chất rắn không tan.
- Thí nghiệm 2: Nếu cho thêm vào hỗn hợp A một lượng Al2O3 bằng 50% lượng Al2O3 trong A ban đầu rồi lại hòa tan vào nước dư. Sau thí nghiệm còn lại 21g chất rắn không tan.
- Thí nghiệm 3: Nếu cho vào hỗn hợp A một lượng Al2O3 bằng 75% lượng Al2O3 trong A, rồi lại hòa tan vào nước dư, thấy còn lại 25g chất rắn không tan.
Tính khối lượng oxit trong hỗn hợp A.
Đáp án như này đúng ko :
Gọi nAl2O3: x, nK2O: y, nCuO: z
Phương trình phản ứng
K2O + H2O → 2KOH
y → 2y
Al2O3 + 2KOH → 2KAlO2 + H2O
y → 2y → 2y
Sau thí nghiệm 2: khối lượng chất rắn tăng lên 6g, khi tăng 25% Al2O3 nữa thì khối lượng chất rắn tăng 4g. Trong trường hợp thí nghiệm 1 Al2O3 hết KOH dư.
80z = 15 => z = 0,1875 mol (1)
Sau TN2: 80z + (15x - y).102 = 21 => 1,5x - y = 6/102 (2)
Sau TN3: 80z + (15x - y).102 = 25 => 1,75x - y = 10/102 (3)
Từ (2), (3) suy ra: x = 16/102=> = 16g
y = 18/102 => = 18/102 x 94 = 16,59g
trả lời đi mình like cho thế là tăng điểm
chẹp chẹp chắc tôi giải đúng rồi
Đúng 2
Bình luận (1)
tôi giải đúng chưa vậy để tui còn chép chẹp chẹp
Đúng 0
Bình luận (0)
mà thực ra đây là bài anh tôi nhưng anh ko có tài khoản nên nhờ tôi đó he he
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Cho hỗn hợp gồm K2O, BaO, Al2O3 và FeO vào lượng nước dư, thu được dung dịch X và chất rắn Y. Sục khí CO2 đến dư vào dung dịch X, thu được kết tủa là A. Fe(OH)2 B. FeCO3 C. Al(OH)3 D. BaCO3.
Đọc tiếp
Cho hỗn hợp gồm K2O, BaO, Al2O3 và FeO vào lượng nước dư, thu được dung dịch X và chất rắn Y. Sục khí CO2 đến dư vào dung dịch X, thu được kết tủa là
A. Fe(OH)2
B. FeCO3
C. Al(OH)3
D. BaCO3.
Đáp án C
Dung dịch X chứa các anion OH– và AlO2–.
Sục CO2 ta có các phản ứng:
CO2 + OH– → HCO3–.
CO2 + AlO2– + H2O → Al(OH)3↓ + HCO3–
Đúng 0
Bình luận (0)
Cho hỗn hợp gồm K2O, BaO, Al2O3 và FeO vào lượng nước dư, thu được dung dịch X và chất rắn Y. Sục khí CO2 đến dư vào dung dịch X, thu được kết tủa là A. Fe(OH)2. B. FeCO3. C. Al(OH)3. D. BaCO3.
Đọc tiếp
Cho hỗn hợp gồm K2O, BaO, Al2O3 và FeO vào lượng nước dư, thu được dung dịch X và chất rắn Y. Sục khí CO2 đến dư vào dung dịch X, thu được kết tủa là
A. Fe(OH)2.
B. FeCO3.
C. Al(OH)3.
D. BaCO3.
Đáp án C
Dung dịch X chứa các anion OH– và AlO2–.
Sục CO2 ta có các phản ứng:
CO2 + OH– → HCO3–.
Đúng 0
Bình luận (0)
Cho hỗn hợp A gồm 3 oxit Al2O3 , K2O , CuO lần lượt làm 3 thí nghiệm sau:TN1: cho hh A vào H20 dư thì thu được 15 g chất rắn không tan.TN2: cho thêm 50% Al2O3 có trong A vào A rồi hòa tan trong nước dư được 21 g chất rắn không tan .TN3:cho thêm 75% Al2O3 có trong A vào A rồi hòa tan trong nước dư được 25 g chất rắn không tan .TÍnh khối lượng các chất có trong A.
Đọc tiếp
Cho hỗn hợp A gồm 3 oxit Al2O3 , K2O , CuO lần lượt làm 3 thí nghiệm sau:TN1: cho hh A vào H20 dư thì thu được 15 g chất rắn không tan.TN2: cho thêm 50% Al2O3 có trong A vào A rồi hòa tan trong nước dư được 21 g chất rắn không tan .TN3:cho thêm 75% Al2O3 có trong A vào A rồi hòa tan trong nước dư được 25 g chất rắn không tan .TÍnh khối lượng các chất có trong A.
Đề bài không hợp lý bạn ạ
Al2O3, CuO không tác dụng với H2O; K2O tác dụng với H2O ra KOH (bazo tan). Vậy nên không có kết tủa bạn à, bạn xem lại đề nhé!
Đúng 0
Bình luận (4)
\(K_2O+H_2O\rightarrow2KOH\)
\(2KOH+Al_2O_3\rightarrow2KAlO_2+H_2O\)
Gọi a,b,c là số mol của \(Al_2O_3,CuO,K_2O\) ban đầu
TN1: a,b,c mol \(Al_2O_3,CuO,K_2O\) + \(H_2O\rightarrow\) 15 g chất rắn
TN2: 1,5a ,b,c mol \(Al_2O_3,CuO,K_2O+H_2O\rightarrow\) 21 g chất rắn
TN3: 1,75a,b,c mol \(Al_2O_3,CuO,K_2O+H_2O\rightarrow\) 25 g chất rắn
Nhận xét :
TN2 : tăng 0,5a mol \(Al_2O_3\) thì tăng 6 g chất rắn
TN3: tăng 0,25a mol \(Al_2O_3\) thì tăng 4 g chất rắn \(>\dfrac{6}{2}=3\left(g\right)\)
\(\Rightarrow\) ởTN2 \(Al_2O_3\) dư còn \(KOH\) hết
\(\Rightarrow\) ở TN1 \(KOH\) dư, \(Al_2O_3\) hết
\(\Rightarrow m_{CuO}=15\left(g\right)\)
Ta có: TN2 và TN3
\(K_2O+H_2O\rightarrow2KOH\)
c -------------------- 2c (mol)
\(2KOH+Al_2O_3\rightarrow2KAlO_2+H_2O\)
2c ----------- c (mol)
\(\rightarrow n_{Al_2O_3}pư=c\left(mol\right)\)
TN2 : m rắn = \(m_{CuO}+m_{Al_2O_3}=21\rightarrow15+102\left(1,5a-c\right)=21\)
TN3 : m rắn = \(m_{CuO}+m_{Al_2O_3}=25\rightarrow15+102\left(1,75a-c\right)=25\)
\(\Rightarrow\left\{{}\begin{matrix}a=\dfrac{8}{51}\\c=\dfrac{3}{17}\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Al_2O_3}=16\left(g\right)\\m_{K_2O}=16.59\left(g\right)\end{matrix}\right.\)
\(K_2O+H_2O\rightarrow2KOH\)
\(2KOH+Al_2O_3\rightarrow2KAlO_2+H_2O\)
Sau TN2 khối lượng tăng lên 6g, thí nghiệm 3 khối lượng tăng lên 10g
\(\Rightarrow\) ởTN2 và TN3 Al2O3 dư còn KOH hết
Đúng 1
Bình luận (0)
Cho 17,2 gam hỗn hợp gồm K2O và K vào nước dư. Sau khi kết thúc phản ứng thu được 2,24 lít khí H2
a, Tính khối lượng mỗi chất trong hỗn hợp?
b, Dẫn khí H2 thu được ở trên qua 12 gam CuO nung nóng. Sau 1 thời gian thu được 10,8 gam chất rắn. Tính hiệu suất phản ứng
\(a,n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ PTHH:2K+2H_2O\rightarrow2KOH+H_2\uparrow\\ Theo.pt:n_K=2n_{H_2}=2.0,1=0,2\left(mol\right)\\ m_K=0,2.39=7,8\left(g\right)\\ m_{K_2O}=17,2-7,8=9,4\left(g\right)\\ b,n_{CuO\left(bđ\right)}=\dfrac{12}{80}=0,15\left(mol\right)\\ PTHH:CuO+H_2\underrightarrow{t^o}Cu+H_2O\\ LTL:0,15>0,1\Rightarrow Cu.dư\)
Gọi nCuO (pư) = a (mol)
=> nCu = a (mol)
mchất rắn sau pư = 80(0,15 - a) + 64a = 10,8
=> a = 0,075 (mol)
=> nH2 (pư) = 0,075 (mol)
\(H=\dfrac{0,075}{0,1}=75\%\)
Đúng 3
Bình luận (0)
Cho hỗn hợp gồm: K2O, BaO, Al2O3, Fe3O4 vào nước (dư), thu được dung dịch X và chất rắn Y. Sục khí CO2 đến dư vào dung dịch X. Sau khi các phản ứng xảy ra hoàn toàn, thu được kết tủa là A. Al(OH)3 B. K2CO3 C. BaCO3 D. Fe(OH)3
Đọc tiếp
Cho hỗn hợp gồm: K2O, BaO, Al2O3, Fe3O4 vào nước (dư), thu được dung dịch X và chất rắn Y. Sục khí CO2 đến dư vào dung dịch X. Sau khi các phản ứng xảy ra hoàn toàn, thu được kết tủa là
A. Al(OH)3
B. K2CO3
C. BaCO3
D. Fe(OH)3
Cho hỗn hợp gồm K2O, BaO, Al2O3 và MgO vào nước dư, sau phản ứng xảy ra hoàn toàn thu được dung dịch X và chất rắn Y. Sục khí CO2 tới dư và dung dịch X, sau phản ứng thu được kết tủa là: A. BaCO3 B. Al(OH)3. C. MgCO3 D. Mg(OH)2.
Đọc tiếp
Cho hỗn hợp gồm K2O, BaO, Al2O3 và MgO vào nước dư, sau phản ứng xảy ra hoàn toàn thu được dung dịch X và chất rắn Y. Sục khí CO2 tới dư và dung dịch X, sau phản ứng thu được kết tủa là:
A. BaCO3
B. Al(OH)3.
C. MgCO3
D. Mg(OH)2.
Các phương trình hóa học: 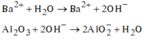
=> Dung dịch X gồm: ![]() có thể có
O
H
-
dư
có thể có
O
H
-
dư
Sục khí CO2 dư vào dung dịch X:
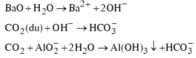
=> Kết tủa thu được là Al(OH)3. Đáp án B.
Đúng 0
Bình luận (0)