hòa tan 8,6 gam oleum X vào nước được dung dịch Y . Để trung hòa dung dịch Y cần 200 ml dung dịch NaOH 1M . Công thức của oleum X là gì ?

Những câu hỏi liên quan
Hòa tan 6,76 gam oleum vào nước dung dịch Y, để trung hòa dung dịch Y cần 160 ml dung dịch NaOH 1M. Công thức phân tử tử oleum là A.
H
2
SO
4
.
nSO
3
B.
H
2
SO
4
.
5
SO
3
C.
H
2
SO...
Đọc tiếp
Hòa tan 6,76 gam oleum vào nước dung dịch Y, để trung hòa dung dịch Y cần 160 ml dung dịch NaOH 1M. Công thức phân tử tử oleum là
A. H 2 SO 4 . nSO 3
B. H 2 SO 4 . 5 SO 3
C. H 2 SO 4 . 3 SO 3
D. H 2 SO 4 . 4 SO 3
Đáp án C
Số mol NaOH là: n NaOH = 0 , 16 . 1 = 0 , 16 mol
Đặt công thức của oleum là H 2 SO 4 . nSO 3
Oleum tác dụng với H 2 O :
H 2 SO 4 . nSO 3 + nH 2 O → ( n + 1 ) H 2 SO 4 ( 1 )
Dung dịch Y là dung dịch H 2 SO 4 . Trung hòa dung dịch Y bằng dung dịch NaOH:
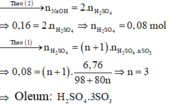
Đúng 0
Bình luận (0)
Hòa tan 3,38 gam oleum A vào lượng nước dư ta được dung dịch A. Để trung hòa 1/20 lượng dung dịch A cần dùng 40 ml dung dịch NaOH 0,1M. Tìm công thức của oleum
CTPT oleum: H2SO4.nSO3 có x (mol)
H2SO4.nSO3 + nH2O → (n + 1)H2SO4
x → x(n + 1)
H2SO4 + 2NaOH → Na2SO4 + 2H2O
x(n + 1)→ 2x(n + 1)
=> (98 + 80n)x = 3,38 và 2x (n + 1) = 0,08
=> x = 0,01 và nx = 0,03
=> n = 3
Suy ra CTPT oleum: H2SO4.3SO3
Đúng 0
Bình luận (0)
Sau khi hoà tan 8,45 gam oleum A vào nước được dung dịch B, để trung hoà dung dịch B cần 200 ml dung dịch NaOH 1M. Xác định công thức của A.
Đặt công thức oleum là H 2 SO 4 . nSO 3
Số mol NaOH là 0,2 mol
H 2 SO 4 . nSO 3 + n H 2 O → (n+1) H 2 SO 4
H 2 SO 4 4 + 2NaOH → Na 2 SO 4 + 2 H 2 O
M( H 2 SO 4 . nSO 3 ) = 8,45/0,1 (n+1) = 98 + 80n
84,5n + 84,5 = 98 + 80n
n = 3
vậy công thức của A : H 2 SO 4 . 3 SO 3
Đúng 0
Bình luận (0)
Hòa tan hết 1,69 gam oleum có công thức H 2 S O 4 . 3 S O 3 vào nước dư. Trung hòa dung dịch thu được cần V ml dung dịch KOH 1M. Giá trị của V là
A. 20
B. 40
C. 30
D. 10
axit H2SO4 100% hấp thụ SO3 tạo ra oleum theo phương trình H2SO4 + SO3 -> H2SO4.nSO3 . Hòa tan 6,76 gam gam oleum vào nước thành 200 ml dung dịch H2SO4 . 10 ml dung dịch trung hòa vừa hết 16 ml dung dịch NaOH 0,5 M a- tính n b- tính hàm lượng % SO3 trong oleum c- cần có bao nhiêu gam oleum có hàm lượng SO3 như trên để pha vào 100 ml dung dịch H2SO4 40% , d= 1,31 g/ml để tạo ra oleum có hàm lượng SO3 là 10%.
H2SO4 + nSO3 => H2SO4.nSO3
H2SO4.nSO3 + nH2O >> n+1H2SO4
H2SO4 + 2NaOH >> Na2SO4 + 2H2O
Số mol NaOH = 0,008 , số mol H2SO4 200ml = 0,008/2 . 200/10 =0,08
Theo (2) nH2SO4.nSO3 =0,08/n+1
MH2SO4.nSO3 =98 +80n = 6,76/0,08/n+1 =84,5n+ 84,5
13,5 =4,5n
=>n=3
%SO3=3.80/2.80+98 =71%
c,Theo câu b , hàm lượng % của SO3 có trong oleum trên là 71
Cứ 100g oleum có 71g SO3 và 29g H2SO4 Khi đó mdd = 1,31.100 = 131g
a g có 71a/100 ...............29a/100
Vì dd H2SO4 có C=40%
Cứ 100g dd có 40g H2SO4 và 60g H2O
=>131g >> 131.40/100 = 52,4g H2SO4 và 131.60/100 = 78,6 g H2O
Khi cho oleum vào dd H2SO4 thì SO3+H2O
SO3 + H2O >> H2SO4
Cứ 80g cần 18g >> 98g
Vậy ..x..g cần 78,6g >>..y..g
x= 78,6.80/18 = 349,3g
y= 78,6.98/18 = 427,9g
Trong loại oleum mới 10% thì mSO3 = 71a/100 -349,3g
và mH2SO4 = 29a/100 +52,4+ 427,9
=> 71a/100 -349,4 / 29a/100 +480,3 = 10/90
=> Bạn ấn máy tìm a nhé
Đúng 1
Bình luận (0)
Hòa tan hết 8,36 gam Oleum có công thức H2SO4.4SO3 vào nước dư. Trung hòa dung dịch thu được cần V ml dung dịch hỗn hợp gồm NaOH 1,5M và KOH 0,5 M. Giá trị của V là:
A. 200 B. 120 C. 50 D. 100
\(n_{H_2SO_4.4SO_3}=\dfrac{8,36}{418}=0,02\left(mol\right)\)
PTHH: H2SO4.4SO3 + 4H2O --> 5H2SO4
0,02------------------->0,1
\(\left\{{}\begin{matrix}n_{NaOH}=0,001V.1,5=0,0015V\left(mol\right)\\n_{KOH}=0,001V.0,5=0,0005V\left(mol\right)\end{matrix}\right.\)
PTHH: 2NaOH + H2SO4 --> Na2SO4 + 2H2O
0,0015V-->0,00075V
2KOH + H2SO4 --> K2SO4 + 2H2O
0,0005V->0,00025V
=> 0,00075V + 0,00025V = 0,1
=> V = 100 (ml)
=> D
Đúng 1
Bình luận (0)
Cho 0,015 mol một loại hợp chất oleum vào nước thu được 200ml dung dịch X. Để trung hòa 100 ml dung dịch X cần dùng 200 ml dung dịch NaOH 0,15M. Thành phần phần trăm về khối lượng của nguyên tố lưu huỳnh trong oleum trên là
A. 37,86%
B. 35,96%
C. 23,97%
D. 32,655%
hòa tan 84,5 gam oleum X vào nước thu được dung dịch Y.Để trung hòa Y cần 1 lít dung dịch NaOH 2M. phần trăm khối lượng lưu huỳnh trong X là ?
\(CT:H_2SO_4.nSO_3\left(xmol\right)\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(xn.............xn\)
\(n_{H_2SO_4}=x+xn=x\left(n+1\right)\left(mol\right)\)
\(n_{NaOH}=2\cdot1=2\left(mol\right)\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+H_2O\)
\(2..................1\)
\(m_X=x\left(98+80n\right)=84.5\left(g\right)\left(1\right)\)
\(n_{H_2SO_4}=x\left(n+1\right)=1\left(mol\right)\left(2\right)\)
\(\dfrac{\left(1\right)}{\left(2\right)}=\dfrac{98+80n}{n+1}=\dfrac{84.5}{1}\)
\(\Leftrightarrow n=3\)
\(CT:H_2SO_4.3H_2O\)
\(x=0.25\)
\(\%S=\dfrac{0.25\cdot4\cdot32}{84.5}\cdot100\%=37.87\%\)
Đúng 1
Bình luận (0)
Cho 1,69 gam một oleum có công thức H2SO4.3SO3 vào nước dư thu được dung dịch X. Để trung hòa dung dịch X cần dùng vừa đủ V lít dung dịch NaOH 2M. Giá trị của V là: A. 20 B. 40 C. 80 D. 10
Đọc tiếp
Cho 1,69 gam một oleum có công thức H2SO4.3SO3 vào nước dư thu được dung dịch X. Để trung hòa dung dịch X cần dùng vừa đủ V lít dung dịch NaOH 2M. Giá trị của V là:
A. 20
B. 40
C. 80
D. 10
Đáp án : A
nOleum = 0,005 mol => nH2SO4 sau hòa tan = nS(Oleum) = 4nOleum = 0,02 mol
=> nNaOH = 2V = 2nH2SO4 = 0,04 mol => V = 0,02 lit = 20 ml
Đúng 0
Bình luận (0)












