Nguyên tử Y có tổng số hạt là 46 hạt. Biết rằng trong hạt nhân nguyên tử có tổng số hạt ko quá 32 hạt. Tìm tên nguyên tử Y và vẽ sơ đồ cấu tạo n.tử

Những câu hỏi liên quan
Một nguyên tử X có tổng số hạt trong nguyên tử là 46 hạt, biết số hạt mang điện nhiều hơn số hạt không mang điện là 14 hạt. Tính số p, e , n và cho biết X là nguyên tố hoá học nào? Vẽ sơ đồ cấu tạo nguyên tử?
Bài 2: Biết tổng số hạt proton, nơtron, electron trong nguyên tử X là 28. Tỉ số giữa số hạt mang điện và số hạt không mang điện là 1,8.a) Tìm số proton, nơtron và electron của nguyên tử X.b) Vẽ sơ đồ cấu tạo nguyên tử X. Bài 3: Nguyên tử Y có tổng số các hạt proton, nơtron, electron là 52. Trong hạt nhân nguyên tử Y, số hạt không mang điện nhiều hơn số hạt mang điện là 1.a) Hãy xác định số hạt proton, nơtron, electron trong nguyên tử X.b) Vẽ sơ đồ cấu tạo nguyên tử Y.
Đọc tiếp
Bài 2: Biết tổng số hạt proton, nơtron, electron trong nguyên tử X là 28. Tỉ số giữa số hạt mang điện và số hạt không mang điện là 1,8.
a) Tìm số proton, nơtron và electron của nguyên tử X.
b) Vẽ sơ đồ cấu tạo nguyên tử X.
Bài 3: Nguyên tử Y có tổng số các hạt proton, nơtron, electron là 52. Trong hạt nhân nguyên tử Y, số hạt không mang điện nhiều hơn số hạt mang điện là 1.
a) Hãy xác định số hạt proton, nơtron, electron trong nguyên tử X.
b) Vẽ sơ đồ cấu tạo nguyên tử Y.
Một nguyên tử X có tổng số hạt là 46 trong đó số hạt không mạng điện chiếm khoảng 34,8%
a/ Tính số hạt mỗi loại trong nguyên tử. Cho biết X là nguyên tử của nguyên tố nào?
b/ Vẽ sơ đồ cấu tạo nguyên tử của nguyến tố đó và cho biết nguyên tử đó có bao nhiêu lớp e, có bao nhiêu e lớp ngoài cùng.
a) Tổng số hạt là 46
=> 2Z + N= 46 (*)
Số hạt mang điện chiếm khoảng 34,8%
=> N=46.34,8%=16
Từ (*) => Z=15=P=E
Vì Z=15 => X là Phốt pho (P)
b) Cấu hình e : \(1s^22s^22p^63s^23p^3\)
Sơ đồ cấu tạo nguyên tử của nguyến tố Phốt pho
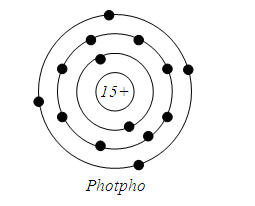
=> Có 3 lớp e, có 5e lớp ngoài cùng
Đúng 0
Bình luận (0)
Giải hộ mình với. Một nguyên tử X có tổng số hạt là 34 số hạt mang điện tích nhiều hơn số hạt ko mang điện tích là 10. Tìm tên nguyên tử X. Vẽ sơ đồ cấu tạo nguyên tử X cho biết số lớp e số e lớp ngoài cùng.
Theo đề bài ta có: \(\left\{{}\begin{matrix}2Z+N=34\\2Z-N=10\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}Z=11\\N=12\end{matrix}\right.\)
Z=11 => X là Na

1s22s22p63s1
Số e ngoài cùng là 1
Đúng 3
Bình luận (0)
1 nguyên tử y có tổng số hạt e,p,n là 40 số hạt mang điện nhiều hơn số hạt không mang điện là 12 tính số hạt mỗi loại trong y, vẽ sơ đồ cấu tạo nguyên tử y
Ta có p + e + n = 40.
Mà p = e => 2p + n = 40
Mặt khác, số hạt không mang điện (n) là 12 => n = 12
=> 2p = 40 - 12 = 28
=> p = 14
Vậy p = e = 14
n = 12
Đúng 2
Bình luận (0)
Tổng số hạt cơ bản trong nguyên tử là 49. Biết số hạt không mang điện nhiều hơn số hạt mang điện trong nhân là 1 đơn vị.
a) Cho biết số p, số n, số e trong nguyên tử ?
b) Cho biết tên và khhh của nguyên tố ?
c) Vẽ sơ đồ đơn giản cấu tạo của nguyên tử .
a)Ta có: p+e+n=49
⇔ 2p+n=49 (do p=e)
Ta có:n-p=1
⇒ p=e=16,n=17
b)Nguyến tố đó là lưu huỳnh (S)
c)Vẽ lớp 1 có 2 e;lớp 2 có 8e;lớp 3 có 6e
Đúng 3
Bình luận (1)
a)theo bài ra:p+n=e=49
vì điện tích trung hòa ⇒2p+n=49 (1)
do số hạt không mang điện nhiều hơn số hạt mang điện trong nhân là 1 đơn vị nên n\(-p=1\)
Từ (1),(2) ta có hệ pt:\(\left\{{}\begin{matrix}2p+n=49\\n-p=1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}p=16=e\\n=17\end{matrix}\right.\)
b)với p=16 nên là nguyên tố lưu huỳnh(S)
Đúng 2
Bình luận (0)
CHO MÌNH HỎI GIẢNG BÀI NAY CHO MÌNH ĐƯỢC KO MN
MỘT NGUYÊN TỬ X CÓ TỔNG SỐ HẠT LÀ 46 ,SỐ HẠT KO MANG ĐIỆN LÀ 8/15 SỐ HẠT MANG ĐIỆN . XÁC DỊNH NGUYỆN TỬ X THUỘC NGUYÊN TÓ NÀO? VẼ SƠ ĐỒ CẤU TẠO NGUYÊN TỬ X
vì số hạt ko mang điện bằng 8/15 số hạt mang điện
=> n = 8/15(p+e)
=>n=8/15 . 2p(vì số p=số e)=> n=16/15p
Có n+p+e=46
=> 16/15p+p+p=46 (vì số p= số e)
=>46/15p=46=>p=15
=> X là nguyên tử thuộc nguyên tố Photpho .Kí Hiệu :P
Đúng 2
Bình luận (1)
Cho nguyên tử X có tổng số hạt là 18. Số hạt ko mang điện trong hạt nhân bằng 1/3 tổng số hạt. a. Tính p,n,e b. Vẽ sơ đồ cấu tạo
\(a.p+e+n=2p+n=18\\ n=\dfrac{1}{3}\left(2p+n\right)\Leftrightarrow\dfrac{2n}{3}=\dfrac{2p}{3}\Rightarrow n=p\Rightarrow p=\dfrac{18}{3}=6\\ X:C\left(carbon\right)\\ b.\)
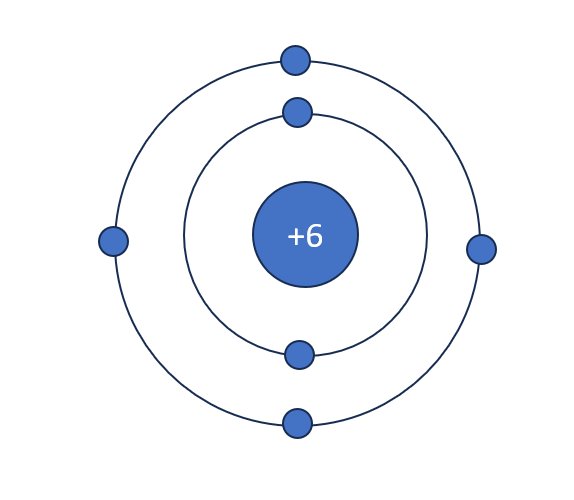
Đúng 2
Bình luận (0)
MIK CẦN GẤP Ạ
Bài 1: Nguyên tử của nguyên tố Y được cấu tạo bởi 86 hạt, trong đó số hạt mang điện trong hạt nhân ít hơn số hạt không mang điện là 5. Xác định số lượng các hạt có trong nguyên tử X, vẽ sơ đồ cấu tạo nguyên tử X.
Ta có hpt: 2p + n = 86
..................n - p=5
=> p = e = 27; n = 32
=> X là Co
Đúng 1
Bình luận (0)





















