Nguyên tử nguyên tố X có tổng số hạt proton, neutron và electron là 18.

Những câu hỏi liên quan
Nguyên tử X có tổng số hạt cơ bản electron, proton, neutron bằng 18. Biết trong tự nhiên, các đồng vị bền luôn có tỉ lệ . Xác định số hạt electron, proton, neutron của nguyên tử X.
Ta có: P + N + E = 18
Mà: P = E (do nguyên tử trung hòa về điện)
⇒ 2P + N = 18 ⇒ N = 18 - 2P
Luôn có: \(1\le\dfrac{N}{P}\le1,5\) \(\Rightarrow P\le18-2P\le1,5P\)
\(\Rightarrow5,14\le P\le6\)
⇒ P = E = 6
N = 6
Đúng 1
Bình luận (0)
Tổng số hạt proton, neutron và electron trong nguyên tử của nguyên tố X là 10, p\(\le\)n\(\le\)1,33p. Số khối của nguyên tử nguyên tố X là
Sửa đề: P ≤ N ≤ 1,33P → P ≤ N ≤ 1,5P (Đây là điều kiện bền của nguyên tử bạn nhé.)
Ta có: P + N + E = 10
Mà: P = E (Do nguyên tử trung hòa về điện.)
⇒ 2P + N = 10 ⇒ N = 10 - 2P
Có: P ≤ N ≤ 1,5P
⇒ P ≤ 10 - 2P ≤ 1,5P
⇒ 2,85 ≤ P ≤ 3,33
⇒ P = E = 3, N = 4
⇒ A = 3 + 4 = 7
Đúng 4
Bình luận (1)
Nguyên tử X có tổng số hạt proton,neutron và electron là 48. Số hạt proton bằng số hạt neutron. Em hãy cho biết a. Số hạt mỗi loại trong nguyên tử X b. Tính khối lượng nguyên tử X c. Vẽ mô hình nguyên tử X, cho biết X có mấy lớp electron, có bao nhiêu electron lớp ngoài cùng?
`#3107.101107`
a.
Gọi số hạt proton, neutron, electron trong nguyên tử X lần lượt là `p, n, e`
Tổng số hạt trong nguyên tử X là `48`
`=> p + n + e = 48`
Mà trong nguyên tử, số `p = e`
`=> 2p + n = 48`
Mà số hạt `p = n`
`=> 3p = 48`
`=> p = 48 \div 3`
`=> p = 16`
Vậy, số `p = n = e = 16`
b.
Khối lượng nguyên tử X là: `16 + 16 = 32` (amu)
c.
Bạn tham khảo mô hình NT X:
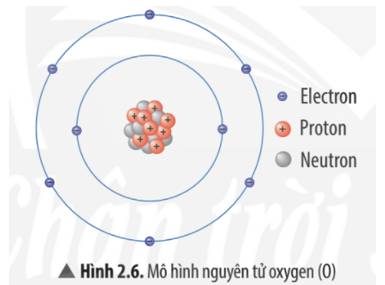
- X có `3` lớp electron
- X có `6` electron lớp ngoài cùng.
Đúng 4
Bình luận (0)
một nguyên tử của nguyên tố có tổng số hạt proton notron và electron là 28 . Số Neutron trong nguyên tử khối là bao nhiêu
trong 1 nguyên tử của nguyên tố X có tổng số hạt proton,neutron,electron là 58, số khối của X<40.Xác định số hiệu nguyên tử của X.Tìm số electron trong mỗi lớp electron của nguyên tử X
Gọi p là số proton
Gọi n là số nơ tron
Gọi e là số electron
Theo đề bài ta có :
p+n+e=58 và p+n<40
Ta thấy p+n=39<40 (số khối hay Khối lượng nguyên tử) ⇒ n=58-39=19 electron (lớp 1 : 2 electron; lớp 2 : 8 electron; lớp 3: 8 electron; lớp 4 : 1 electron)
⇒ Nguyên tử đó có 4 lớp electron và lớp ngoài cùng có 1 electron ⇒ Thuộc chu kỳ 4 và Nhóm IA
Vậy nguyên tử đó là K (Protassium) và số hiệu nguyên tử là 19
Đúng 0
Bình luận (0)
nguyên tử của nguyên tố X có tổng số hạt proton,neutron,electron là 52,trong đó số hạt không mang điện hơn số hạt mang điện âm là 1 hạt.số khối của nguyên tử X là?
\(2p+n=52\\ n-e=n-p=1\\ p=\dfrac{51}{3}=17\\ n=52-34=18\\ A_X=17+18=35\)
Đúng 1
Bình luận (0)
nguyên tử của nguyên tố X có tổng số hạt proton,neutron,electron là 52,trong đó số hạt không mang điện hơn số hạt mang điện âm là 1 hạt.số khối của nguyên tử X là?
Nguyên tử của nguyên tố X có tổng số hạt proton, neutron, electron là 52 có:
\(p+e+n=2p+n=52\left(1\right)\)
Số hạt không mang điện hơn số hạt mang điện âm là 1 hạt trong nguyên tử của nguyên tố X, có:
\(n-e=1\\ \Leftrightarrow n-p=1\\ \Leftrightarrow-p+n=1\left(2\right)\)
Từ (1), (2) giải được: \(\left\{{}\begin{matrix}p=17\\n=18\end{matrix}\right.\)
Vậy số khối của nguyên tử X là: \(p+n=17+18=35\)
Đúng 1
Bình luận (0)
Giúp mình với :))
Nguyên tử của nguyên tố X có tổng số hạt proton, neutron,
electron là 36, trong đó số hạt mang điện gấp đôi số hạt không mang điện. Tìm số hạt mỗi loại trong nguyên tử và vẽ mô hình nguyên tử X.
Đọc tiếp
Giúp mình với :))
Nguyên tử của nguyên tố X có tổng số hạt proton, neutron,
electron là 36, trong đó số hạt mang điện gấp đôi số hạt không mang điện. Tìm số hạt mỗi loại trong nguyên tử và vẽ mô hình nguyên tử X.
\(p+e+n=36\)
mà \(p+e=2n\)
\(\Rightarrow2n+n=36\)
\(\Rightarrow3n=36\)
\(\Rightarrow n=12\)
\(\Rightarrow p+e=24\)
mà \(p=e\)
\(\Rightarrow p=e=24:2=12\)
Đúng 4
Bình luận (1)
proton là 12 hạt
neutron là 12 hạt
electron là 12 hạt
Đúng 0
Bình luận (0)
trong 1 nguyên tử của nguyên tố x có tổng số hạt proton,neutron,electron là 60, số khối của x<41.xác định số hiệu nguyên tử của x




















