tính số mol hỗn hợp A gồm (0.22 mol Al và 0.25 Cu)

Những câu hỏi liên quan
hỗn hợp A gồm (0.22 mol al và 0.25 mol Cu)
Ta có:
\(m_{Al}=n_{Al}\cdot M_{Al}=0,22\cdot27=5,94\left(g\right)\)
\(m_{Cu}=n_{Cu}\cdot M_{Cu}=0,25\cdot64=16\left(g\right)\)
Nên khối lượng của hỗn hợp A là:
\(m_A=m_{Al}+m_{Cu}=5,94+16=21,94\left(g\right)\)
Đúng 2
Bình luận (0)
Hãy tính:
a) Số mol của : 28g Fe 64g Cu 5,4g Al.
b) Thể tích khí (đktc) của 0,175 mol CO2; 1,25 mol H2; 3 mol N2.
c) Số mol và thể tích của hỗn hợp khí (dktc) gồm có 0,44g CO2 0,04g H2 và 0,56g N2.
a)
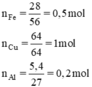
b) VCO2 = 22,4 .0,175 = 3,92l.
VH2 = 22,4 .1,25 = 28l.
VN2 = 22,4.3 = 67,2l.
c) Số mol của hỗn hợp khí bằng tổng số mol của từng khí.
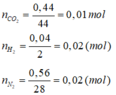
nhh = nCO2 + nH2 + nN2 = 0,01 + 0,02 + 0,02 = 0,05 mol
Vhh khí = (0,01 + 0,02 + 0,02) . 22,4 = 1,12l.
Đúng 0
Bình luận (0)
Hỗn hợp X gồm: 0,1 mol Cu; 0,2 mol Al và 0,3 mol Mg.
a) Tính % khối lượng mỗi kim loại trong hỗn hợp X.
b) Tính số gam acid HCl cần dùng để phản ứng vừa hết với hỗn hợp X. Từ đó tính thể tích khi thoát ra (đo ở đkc).
a) \(m_X=0,1\cdot64+0,2\cdot27+0,3\cdot24=19\left(g\right)\)
\(\Rightarrow\%m_{Cu}=\dfrac{0,1\cdot64\cdot100}{19}=34\%\)
\(\Rightarrow\%m_{Al}=\dfrac{0,2\cdot27\cdot100}{19}=28\%\)
\(\Rightarrow\%m_{Mg}=100\%-34\%-28\%=38\%\)
b) \(Cu+2HCl\rightarrow CuCl_2+H_2\) (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\) (2)
\(Mg+2HCl\rightarrow MgCl_2+H_2\) (3)
\(n_{HCl\left(1\right)}=2n_{Cu}=2\cdot0,1=0,2\left(mol\right)\)
\(n_{HCl\left(2\right)}=\dfrac{6\cdot n_{Al}}{2}=3\cdot0,2=0,6\left(mol\right)\)
\(n_{HCl\left(3\right)}=2n_{Mg}=2\cdot0,3=0,6\left(mol\right)\)
\(\Rightarrow m_{HCl}=\left(0,2+0,6+0,6\right)\cdot36,5=51,1\left(g\right)\)
\(n_{H_2\left(1\right)}=n_{Cu}=0,1\left(mol\right);n_{H_2\left(2\right)}=\dfrac{3\cdot0,2}{2}=0,3\left(mol\right);n_{H_2\left(3\right)}=n_{Mg}=0,3\left(mol\right)\)
\(V_{H_2\left(dkc\right)}=\left(0,1+0,3+0,3\right)\cdot24,79=17,353\left(l\right)\)
Đúng 1
Bình luận (1)
cho m gam hỗn hợp X gồm 2 kim loại là mg và al trộn với nhau có tỉ lệ mol là 3:1 phản ứng với o2 thu đc 13.1 gam hỗn hợp Y cho Y phản ứng hết với HCL thu đc 0.25 mol tính m
Cho các nhận định sau: (1) Hỗn hợp rắn gồm Al và Na (tỉ lệ mol 1 : 1) tan hết trong nước dư. (2) Hỗn hợp rắn gồm Fe3O4 và Cu (tỉ lệ mol 1 : 1) tan hết trong dung dịch HCl. (3) Hỗn hợp rắn gồm FeCl3 và Cu (tỉ lệ mol 2 : 1) tan hết trong nước dư. (4) Hỗn hợp rắn gồm FeS và CuS (tỉ lệ mol 1 : 1) tan hết trong dung dịch HCl Số nhận định đúng là A. 3 B. 2 C. 4. D. 1
Đọc tiếp
Cho các nhận định sau:
(1) Hỗn hợp rắn gồm Al và Na (tỉ lệ mol 1 : 1) tan hết trong nước dư.
(2) Hỗn hợp rắn gồm Fe3O4 và Cu (tỉ lệ mol 1 : 1) tan hết trong dung dịch HCl.
(3) Hỗn hợp rắn gồm FeCl3 và Cu (tỉ lệ mol 2 : 1) tan hết trong nước dư.
(4) Hỗn hợp rắn gồm FeS và CuS (tỉ lệ mol 1 : 1) tan hết trong dung dịch HCl
Số nhận định đúng là
A. 3
B. 2
C. 4.
D. 1
em cần gấp nhờ giúp cái ạ F22: Tính số mol mỗi kim loại ? Biết :a. 9,96 gam hỗn hợp X ( Fe , Al có tỷ lệ mol 1 : 1) .b. 27,6 gam hỗn hợp Y ( Fe , Cu có tỷ lệ mol 1 : 2) .c. 29,52 gam hỗn hợp Z ( Cu, Al có tỷ lệ mol 3 : 2 ) . F23: 11 gam hỗn hợp X (Al, Fe) có tổng số mol là 0,3. Tính khối lượng mỗi kim loại ?
Đọc tiếp
em cần gấp nhờ giúp cái ạ ![]()
F22: Tính số mol mỗi kim loại ? Biết :
a. 9,96 gam hỗn hợp X ( Fe , Al có tỷ lệ mol 1 : 1) .
b. 27,6 gam hỗn hợp Y ( Fe , Cu có tỷ lệ mol 1 : 2) .
c. 29,52 gam hỗn hợp Z ( Cu, Al có tỷ lệ mol 3 : 2 ) .
F23: 11 gam hỗn hợp X (Al, Fe) có tổng số mol là 0,3. Tính khối lượng mỗi kim loại ?
F22: Tính số mol mỗi kim loại ? Biết :
a. 9,96 gam hỗn hợp X ( Fe , Al có tỷ lệ mol 1 : 1) .
Gọi x, y lần lượt là số mol Fe, Al
\(\left\{{}\begin{matrix}56x+27y=9,96\\x=y\end{matrix}\right.\)
=> x=y= 0,12(mol)
b. 27,6 gam hỗn hợp Y ( Fe , Cu có tỷ lệ mol 1 : 2) .
Gọi x, y lần lượt là số mol Fe, Cu
\(\left\{{}\begin{matrix}56x+64y=27,6\\\dfrac{x}{y}=\dfrac{1}{2}\end{matrix}\right.\)
=> x= 0,15; y=0,3
c. 29,52 gam hỗn hợp Z ( Cu, Al có tỷ lệ mol 3 : 2 ) .
Gọi x, y lần lượt là số mol Cu, Al
\(\left\{{}\begin{matrix}64x+27y=29,52\\\dfrac{x}{y}=\dfrac{3}{2}\end{matrix}\right.\)
=> x= 0,36 ; y=0,24
F23: 11 gam hỗn hợp X (Al, Fe) có tổng số mol là 0,3. Tính khối lượng mỗi kim loại ?
Gọi x, y lần lượt là số mol Al, Fe
\(\left\{{}\begin{matrix}27x+56y=11\\x+y=0,3\end{matrix}\right.\)
=> x=0,2 , y =0,1
=> \(\left\{{}\begin{matrix}m_{Al}=0,2.27=5,4\left(g\right)\\m_{Fe}=0,1.56=5,6\left(g\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Hỗn hợp rắn X gồm Al, Fe2O3 và Cu có số mol bằng nhau. Hỗn hợp X tan hoàn toàn trong dung dịch
A. AgNO3 (dư).
B. HCl (dư).
C. NH3 (dư).
D. NaOH (dư).
Hỗn hợp rắn gồm Al, Fe2O3 và Cu có số mol bằng nhau. Hỗn hợp X hoà tan hoàn toàn trong dung dịch
A. AgNO3 (dư)
B. HCl (dư)
C. NH3 (dư)
D. NaOH (dư)
Hỗn hợp rắn X gồm Al, Fe2O3 và Cu có số mol bằng nhau. Hỗn hợp X tan hoàn toàn trong dung dịch A. AgNO3 (dư). B. HCl (dư). C. NH3 (dư). D. NaOH (dư).
Đọc tiếp
Hỗn hợp rắn X gồm Al, Fe2O3 và Cu có số mol bằng nhau. Hỗn hợp X tan hoàn toàn trong dung dịch
A. AgNO3 (dư).
B. HCl (dư).
C. NH3 (dư).
D. NaOH (dư).












