Quan sát Hình 9.1, nhận xét số electron trên lớp vỏ với số proton trong hạt nhân của mỗi ion tạo thành.

Những câu hỏi liên quan
Cho các nhận xét sau: trong nguyên tử: (1) Số hiệu nguyên tử bằng điện tích hạt nhân nguyên tử. (2) Số đơn vị điện tích hạt nhân nguyên tử bằng số hạt proton. (3) Số hạt proton trong hạt nhân luôn bằng số electron lớp vỏ của nguyên tử. (4) Số hạt proton bằng số hạt nơtron. Số nhận xét không đúng là: A. 2 B. 3 C. 1 D. 4
Đọc tiếp
Cho các nhận xét sau: trong nguyên tử:
(1) Số hiệu nguyên tử bằng điện tích hạt nhân nguyên tử.
(2) Số đơn vị điện tích hạt nhân nguyên tử bằng số hạt proton.
(3) Số hạt proton trong hạt nhân luôn bằng số electron lớp vỏ của nguyên tử.
(4) Số hạt proton bằng số hạt nơtron.
Số nhận xét không đúng là:
A. 2
B. 3
C. 1
D. 4
Số hiệu nguyên tử bằng số đơn vị điện tích hạt nhân ( chú ý điện tích hạt nhân là giá trị có dấu +, còn số hiệu nguyên tử là giá trị không có dấu) → (1) sai
Số đơn vị điện tích hạt nhân bằng số hạt proton → (2) đúng
Nguyên tử trung hòa về điện → số p = số e. → (3) đúng
Hầu hết các nguyên tử có số nơtron lớn hơn số proton → (4) sai
Đúng 0
Bình luận (0)
Cho các nhận xét sau: trong nguyên tử: (1) Số hiệu nguyên tử bằng điện tích hạt nhân nguyên tử; (2) số đơn vị điện tích hạt nhân nguyên tử bằng số hạt proton; (3) Số hạt proton trong hạt nhân luôn bằng số electron lớp vỏ của nguyên tử; (4) Số hạt proton bằng số hạt notron. Số nhận xét không đúng là: A. 2. B. 3. C. 1. D. 4.
Đọc tiếp
Cho các nhận xét sau: trong nguyên tử:
(1) Số hiệu nguyên tử bằng điện tích hạt nhân nguyên tử;
(2) số đơn vị điện tích hạt nhân nguyên tử bằng số hạt proton;
(3) Số hạt proton trong hạt nhân luôn bằng số electron lớp vỏ của nguyên tử;
(4) Số hạt proton bằng số hạt notron.
Số nhận xét không đúng là:
A. 2.
B. 3.
C. 1.
D. 4.
Số hiệu nguyên tử bằng số đơn vị điện tích hạt nhân ( chú ý điện tích hạt nhân là giá trị có dấu +, còn số hiệu nguyên tử là giá trị không có dấu) → (1) sai
Số đơn vị điện tích hạt nhân bằng số hạt proton → (2) đúng
Nguyên tử trung hòa về điện → số p = số e. → (3) đúng
Hầu hết các nguyên tử có số notron lớn hơn số proton → (4) sai
Đáp án B.
Đúng 0
Bình luận (0)
Quan sát Hình 6.2, em hãy mô tả sự tạo thành ion sodium, ion magnesium. Nhận xét về số electron lớp ngoài cùng của các ion này và cho biết sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm nào?
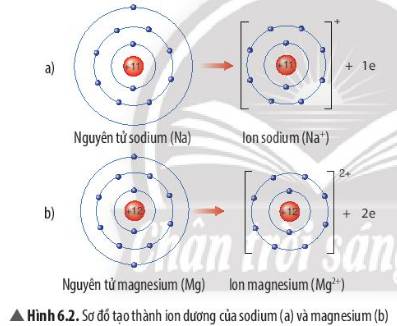
- Sự tạo thành ion sodium: Nguyên tử sodium (Na) cho đi 1 electron lớp ngoài cùng để tạo thành ion dương Na+
- Sự tạo thành ion magnesium: Nguyên tử magnesium (Mg) cho đi 2 electron lớp ngoài cùng để tạo thành ion dương Mg2+
=> Sau khi nhường electron, ion sodium và ion magnesium đều có 2 lớp electron và có 8 electron ở lớp ngoài cùng
=> Sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm Neon (Ne)
Đúng 0
Bình luận (0)
Quan sát Hình 6.3, em hãy mô tả sự tạo thành ion chloride, ion oxide. Nhận xét về số electron lớp ngoài cùng của các ion này và cho biết sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm nào?
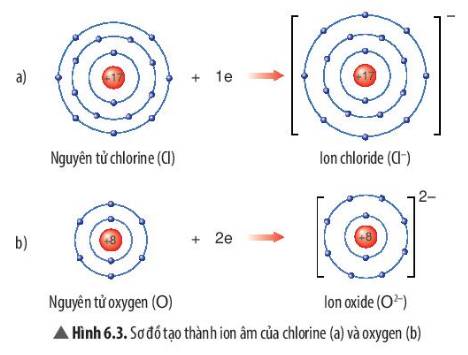
- Sự tạo thành ion chloride: Nguyên tử chlorine (Cl) nhận thêm 1 electron ở lớp ngoài cùng để tạo thành ion âm Cl-
- Sự tạo thành ion oxide: Nguyên tử oxygen (O) nhận thêm 2 electron ở lớp ngoài cùng để tạo thành ion âm O2-
- Sau khi nhận electron, ion chloride có 3 lớp electron và có 8 electron ở lớp ngoài cùng
=> Giống sự phân bố electron của nguyên tử khí hiếm Neon (Ne)
- Sau khi nhận electron, ion oxide có 2 lớp electron và có 8 electron ở lớp ngoài cùng
=> Giống sự phân bố electron của nguyên tử Argon (Ar)
Đúng 0
Bình luận (0)
Cho các nhận xét sau: 1. Một nguyên tử có điện tích hạt nhân là +1,6a.10-19 Culong thì số proton trong hạt nhân là a. 2. Trong một nguyên tử thì số proton luôn bằng số nơtron. 3. Khi bắn phá hạt nhân người ta tìm thấy một loại hạt có khối lượng gần bằng khối lượng của proton, hạt đó là electron. 4. Trong nguyên tử bất kì thì điện tích của lớp vỏ luôn bằng điện tích của hạt nhân nhưng ngược dấu. Số nhận xét đúng là A. 1 B. 2 C. 3 D. 4
Đọc tiếp
Cho các nhận xét sau:
1. Một nguyên tử có điện tích hạt nhân là +1,6a.10-19 Culong thì số proton trong hạt nhân là a.
2. Trong một nguyên tử thì số proton luôn bằng số nơtron.
3. Khi bắn phá hạt nhân người ta tìm thấy một loại hạt có khối lượng gần bằng khối lượng của proton, hạt đó là electron.
4. Trong nguyên tử bất kì thì điện tích của lớp vỏ luôn bằng điện tích của hạt nhân nhưng ngược dấu.
Số nhận xét đúng là
A. 1
B. 2
C. 3
D. 4
Cho các nhận xét sau: 1. Một nguyên tử có điện tích hạt nhân là +1,6a.10-19 Culong thì số proton trong hạt nhân là a 2. Trong một nguyên tử thì số proton luôn bằng số nơtron. 3. Khi bắn phá hạt nhân người ta tìm thấy một loại hạt có khối lượng gần bằng khối lượng của proton, hạt đó là electron. 4. Trong nguyên tử bất kì thì điện tích của lớp vỏ luôn bằng điện tích của hạt nhân nhưng ngược dấu. Số nhận xét đúng là A. 1 B. 2 C. 3 D. 4
Đọc tiếp
Cho các nhận xét sau:
1. Một nguyên tử có điện tích hạt nhân là +1,6a.10-19 Culong thì số proton trong hạt nhân là a
2. Trong một nguyên tử thì số proton luôn bằng số nơtron.
3. Khi bắn phá hạt nhân người ta tìm thấy một loại hạt có khối lượng gần bằng khối lượng của proton, hạt đó là electron.
4. Trong nguyên tử bất kì thì điện tích của lớp vỏ luôn bằng điện tích của hạt nhân nhưng ngược dấu.
Số nhận xét đúng là
A. 1
B. 2
C. 3
D. 4
1 proton có điện tích là + 1,6. 10-19 C → Một nguyên tử có điện tích hạt nhân là +1.6a.10-19 culong thì số proton trong hạt nhân là
1
,
6
a
.
10
-
19
1
,
6
.
10
-
19
= a → (1) đúng
Trong 1 nguyên tử thì số proton luôn bằng số electron → (2) sai
Trong hạt nhân gồm proton và notron → (3) sai
Trong 1 nguyên tử bất kì số p = số e, nếu điện tích của lớp vỏ mang điện tích âm (-Z) thì điện tích của hạt nhân là +Z → (4) đúng
Đáp án B.
Đúng 0
Bình luận (0)
Trong phân tử
M
2
X
có tổng số hạt (proton, nơtron, electron) là 140 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt. Số khối của ion
M
+
lớn hơn số khối của ion
X
2
-
là 23. Tổng số hạt proton, nơtron, electron trong ion
M
+
nhiều hơn trong ion ...
Đọc tiếp
Trong phân tử M 2 X có tổng số hạt (proton, nơtron, electron) là 140 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt. Số khối của ion M + lớn hơn số khối của ion X 2 - là 23. Tổng số hạt proton, nơtron, electron trong ion M + nhiều hơn trong ion X 2 - là 31 hạt. Nhận xét nào sau đây không đúng?
A. M 2 X tan trong nước tạo thành dung dịch kiềm.
B. Trong các phản ứng hóa học, M chỉ thể hiện tính khử.
C. X vừa có tính oxi hóa vừa có tính khử.
D. M 2 X là hợp chất ion.
Nguyên tử agon có kí hiệu là
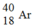
- Hãy xác định số proton, số proton trong hạt nhân và số electron ở vỏ electron của nguyên tử.
- Hãy xác định sự phân bố electron trên các lớp.
Z= 18 suy ra trong hạt nhân Ar có 18p và 22n (40 – 18), lớp vỏ electron của nguyên tử có 18e được phân bố như sau: 1s22s22p63s23p6.
Đúng 0
Bình luận (0)
Nguyên tử của nguyên tố Y nhận thêm 1 electron thì tạo thành ion Y - có cấu hình electron lớp ngoài cùng là 2 p 6 . Trong hạt nhân của Y có 10 nơtron. Số khối của Y là
A. 19
B. 20
C. 16
D. 9