Hòa tan 1,53 gam hỗn hợp Mg Al có số mol bằng nhau trong 200 ml dung dịch HCl 2M thể tích dung dịch không đổi. Xác định nồng độ mol của ion trong dung dịch thu được

Những câu hỏi liên quan
a, Tính nồng độ mol/l của ion trong dung dịch HCl 7,3% (D = 1,25g/ml) b, Hòa tan hoàn toàn 6,345 gam Al trong 400ml dung dịch HCl 2M. Tính pH của dung dịch thu được sau phản ứng (V dung dịch biến đổi không đáng kể).
a)
Coi V dd HCl = 100(ml)
m dd HCl = 1,25.100 = 125(gam)
n HCl = 125.7,3%/36,5 = 0,25(mol)
[H+ ] = [Cl- ] = CM HCl = 0,25/0,1 = 2,5M
b)
n Al = 0,235(mol)
2Al + 6HCl $\to$ 2AlCl3 + 3H2
n HCl pư = 3n Al = 0,705(mol)
n HCl dư = 0,4.2 - 0,705 = 0,095(mol)
[H+ ] = CM HCl dư = 0,095/0,4 = 0,2375M
pH = -log([H+ ]) = 0,624
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn hỗn hợp Al và
A
l
2
O
3
trong 200 ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa
A
l
(
O
H
)
3
(m ga...
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp Al và A l 2 O 3 trong 200 ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa A l ( O H ) 3 (m gam) phụ thuộc vào thể tích dung dịch NaOH (V ml) được biểu diễn bằng đồ thị bên. Giá trị của a là
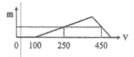
A. 0,5
B. 1,5
C. 1,0
D. 2,0
Đáp án D
Số mol HCl dư =0,1 (mol)
Số mol kết tủa
![]()
Số mol ![]()
Số mol HCl ban đầu = 3 . 0 , 1 + 0 , 1 = 0 , 4 ⇒ a = 2
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn hỗn hợp Al và Al2O3 trong 200 ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa Al(OH)3 (m gam) phụ thuộc vào thể tích dung dịch NaOH (V ml) được biểu diễn bằng đồ thị bên: Giá trị của a là A. 2,0. B. 1,5. C. 1,0. D. 0,5.
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp Al và Al2O3 trong 200 ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa Al(OH)3 (m gam) phụ thuộc vào thể tích dung dịch NaOH (V ml) được biểu diễn bằng đồ thị bên:
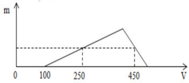
Giá trị của a là
A. 2,0.
B. 1,5.
C. 1,0.
D. 0,5.
Đáp án A
X gồm HCl dư (x mol) và AlCl3 (y mol)
=> x = 0,1 mol
+ Tại nNaOH = 0,25 mol: nNaOH = nHCl + 3nAl(OH)3 => nAl(OH)3 = (0,25-0,1)/3 = 0,05 mol
+ Tại nNaOH = 0,45 mol: nNaOH = nHCl + 4nAl3+ - nAl(OH)3 => 0,45 = 0,1 + 4y – 0,05 => y = 0,1 mol
BT “Cl” => nHCl = 3nAlCl3 + nHCl dư => nHCl = 0,1 + 3.0,1 = 0,4 mol
=> a = 0,4/0,2 = 2M
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn hỗn hợp Al và
Al
2
O
3
trong 200 ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa
Al
(
OH
)
3
(m gam) phụ thuộc vào thể tích dung dịch NaOH (V ml) được biểu diễn bằng đồ thị bên. Giá trị của a là A. 0,5 B....
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp Al và Al 2 O 3 trong 200 ml dung dịch HCl nồng độ
a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa Al ( OH ) 3 (m gam) phụ thuộc vào thể tích dung dịch NaOH (V ml) được biểu diễn bằng đồ thị bên. Giá trị của a là
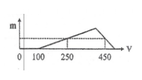
A. 0,5
B. 1,5
C. 1,0
D. 2,0
Hòa tan hoàn toàn hỗn hợp Al và Al2O3 trong 200 ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa Al(OH)3 (m gam) phụ thuộc vào thể tích dung dịch NaOH (V ml) được biểu diễn bằng đồ thị: Giá trị lớn nhất của m là A. 8,58. B. 7,02. C. 11,70. D. 7,80.
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp Al và Al2O3 trong 200 ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa Al(OH)3 (m gam) phụ thuộc vào thể tích dung dịch NaOH (V ml) được biểu diễn bằng đồ thị:
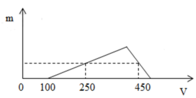
Giá trị lớn nhất của m là
A. 8,58.
B. 7,02.
C. 11,70.
D. 7,80.
Giải thích:
Ta chia đồ thị làm 3 giai đoạn
Giai đoạn 1: bắt đầu xuất hiện kết tủa => hết VNaOH = 100 ml => đây là lượng thể tích cần dùng để trung hòa lượng HCl còn dư sau phản ứng
=> nHCl dư = 0,1 (mol)
Giai đoạn 2: đồ thi bắt đầu đi lên đến điểm cực đại
Tại giai đoạn này xảy ra phản ứng:
Al3+ + 3OH- → Al(OH)3↓
(0,25 – 0, 1) → 0,05 (mol)
Giai đoạn 3: đồ thị đi xuống, tại giai đoạn này lượng kết tủa bị hòa tan theo phản ứng
Al(OH)3 + OH- → AlO2− + 2H2O
Từ đồ thị ta thấy tại giá trị VNaOH = 250 ml và VNaOH = 450 ml cùng thu được một lượng kết tủa như nhau
=> áp dụng công thức nhanh ta có:
nNaOH = 4nAl3+ - nAl(OH)3 + nH+ dư
=> 0,45 = 4a – 0,05 + 0,1
=> a = 0,1 (mol)
Vậy để lượng kết tủa cực đại thì tất cả lượng Al3+ sẽ chuyển hết thành Al(OH)3
=> nAl(OH)3 = nAl3+ = 0,1 (mol) => mAl(OH)3 = 0,1.78 = 7,8(g)
Đáp án D
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn hỗn hợp Al và Al2O3 trong 200 ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa Al(OH)3 (m gam) phụ thuộc vào thể tích dung dịch NaOH (V ml) được biểu diễn bằng đồ thị bên: Giá trị của a là A. 2,0 B. 1,5 C. 1,0 D. 0,5
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp Al và Al2O3 trong 200 ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa Al(OH)3 (m gam) phụ thuộc vào thể tích dung dịch NaOH (V ml) được biểu diễn bằng đồ thị bên:
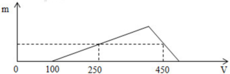
Giá trị của a là
A. 2,0
B. 1,5
C. 1,0
D. 0,5
Đáp án A
X gồm HCl dư (x mol) và AlCl3 (y mol)
=> x = 0,1 mol
+ Tại nNaOH = 0,25 mol: nNaOH = nHCl + 3nAl(OH)3 => nAl(OH)3 = (0,25-0,1)/3 = 0,05 mol
+ Tại nNaOH = 0,45 mol: nNaOH = nHCl + 4nAl3+ - nAl(OH)3 => 0,45 = 0,1 + 4y – 0,05 => y = 0,1 mol
BT “Cl” => nHCl = 3nAlCl3 + nHCl dư => nHCl = 0,1 + 3.0,1 = 0,4 mol
=> a = 0,4/0,2 = 2M
Đúng 0
Bình luận (0)
hòa tan 9,6g Mg vao 400 ml dung dịch FeCl3 0,5 mol/l người ta thu được dung dịch A và hỗn hợp rắn B.
a)Tính nồng độ mol/l của chất tan trong dung dich A.(Biết thễ tích dung dịch không thay đổi và các phản ứng hoàn toàn)
b)Hỗn hợp B tan hoàn tàn trong dung dịch HCl 30%(d=1,123 g/ml). Tính thể tích dung dịch HCl đã dùng.
Do sau phản ứng là hh chất rắn nên Mg dư, FeCl3 hết
PTHH
Mg + 2FeCl3 --> MgCl2 + 2FeCl2
x 2x 2x
Mg + FeCl2 --> MgCl2 + Fe
2x 2x 2x
3Mg + 2FeCl3 --> 3MgCl2 + 2Fe
y 2/3y 2/3y
Theo PTHH ta có: nFeCl3 = nFe = 0.2
2nMg = 3nFe = 0.3
nMg = nMgCl2 = 0.3
Nồng độ mol của các chất trong hh:
CmFeCl2 = 0.2/0.4 = 0.5M
CmMgCl2 = 0.3/0.4 = 0.75M
PTHH
Fe + 2HCl --> FeCl2 + H2
0.2 0.4
Mg + 2HCl --> MgCl2 + H2
0.3 0.6
Khối lượng HCl cần dùng: m = 1*36.5 = 36.5g
Đúng 0
Bình luận (1)
với lại bài này có cho Mg tác dụng với FeCl2 hay là chỉ cho tác dụng với FeCl3 với lại cho mình bik vì sao khi làm nhớ giải thích giùm mình nhé thank you
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn hỗn hợp Al và Al2O3 vào 200 ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa Al(OH)3 (m gam) phụ thuộc vào thể tích NaOH (V ml) được biểu diễn bằng đồ thị bên. Giá trị của a là: A. 0,5 B. 1,5 C. 1,0 D. 2,0
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp Al và Al2O3 vào 200 ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa Al(OH)3 (m gam) phụ thuộc vào thể tích NaOH (V ml) được biểu diễn bằng đồ thị bên. Giá trị của a là:
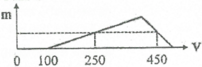
A. 0,5
B. 1,5
C. 1,0
D. 2,0
Hòa tan hoàn toàn hỗn hợp Al và Al2O3 vào 200 ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa Al(OH)3 (m gam) phụ thuộc vào thể tích NaOH (V ml) được biểu diễn bằng đồ thị bên. Giá trị của a là: A. 0,5 B. 1,5 C. 1,0 D. 2,0
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp Al và Al2O3 vào 200 ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa Al(OH)3 (m gam) phụ thuộc vào thể tích NaOH (V ml) được biểu diễn bằng đồ thị bên. Giá trị của a là:
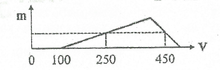
A. 0,5
B. 1,5
C. 1,0
D. 2,0
Hòa tan hoàn toàn hỗn hợp Al và Al2O3 trong 200ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa Al(OH)3 (m gam) phụ thuộc vào thể tích dung dịch NaOH (V ml) được biểu diễn bằng đồ thị bên. A. 2,0. B. 1,5. C. 1,0. D. 0,5.
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp Al và Al2O3 trong 200ml dung dịch HCl nồng độ a mol/l, thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, lượng kết tủa Al(OH)3 (m gam) phụ thuộc vào thể tích dung dịch NaOH (V ml) được biểu diễn bằng đồ thị bên.
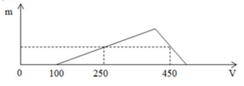
A. 2,0.
B. 1,5.
C. 1,0.
D. 0,5.
Giải thích:
X gồm HCl dư (x mol) và AlCl3 (y mol)
=> x = 0,1 mol
+ Tại nNaOH = 0,25 mol: nNaOH = nHCl + 3nAl(OH)3 => nAl(OH)3 = (0,25-0,1)/3 = 0,05 mol
+ Tại nNaOH = 0,45 mol: nNaOH = nHCl + 4nAl3+ - nAl(OH)3 => 0,45 = 0,1 + 4y – 0,05 => y = 0,1 mol
BT “Cl” => nHCl = 3nAlCl3 + nHCl dư => nHCl = 0,1 + 3.0,1 = 0,4 mol
=> a = 0,4/0,2 = 2M
Đáp án A
Đúng 0
Bình luận (0)










