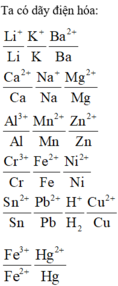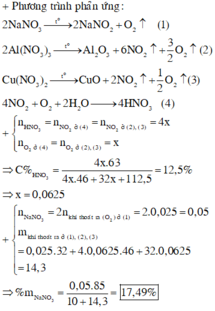Hỗn hợp A gồm Al(NO3)3; Cu(NO3)2; Pb(NO3)2. Biết thành phần % theo khối lượng của nguyên tố nitơ trong A là 14,43%. Tính khối lượng của 3 kim loại Al, Cu, Pb có trong 52,39g hỗn hợp A?

Những câu hỏi liên quan
2. Hỗn hợp X gồm Fe(NO3)3, Fe(NO3)2 và Al(NO3)3. Trong hỗn hợp X, nguyên tố nitơ chiếm 17,38% về khối lượng. Từ 14,5 gam hỗn hợp X có thể điều chế được tối đa m gam hỗn hợp Y gồm hai kim loại Fe và Al. Tính giá trị của m.
Cho Al đến dư vào dung dịch hỗn hợp gồm Cu(NO3)2, Ag(NO3)3, Mg(NO3)2, Fe(NO3)3 thì thứ tự các ion kim loại bị khử lần lượt là A. Ag+, Fe3+, Cu2+, Fe2+. B. Fe3+, Ag+, Cu2+, Mg2+. C. Ag+, Fe3+, Cu2+, Mg2+. D. Ag+, Cu2+, Fe3+, Mg2+.
Đọc tiếp
Cho Al đến dư vào dung dịch hỗn hợp gồm Cu(NO3)2, Ag(NO3)3, Mg(NO3)2, Fe(NO3)3 thì thứ tự các ion kim loại bị khử lần lượt là
A. Ag+, Fe3+, Cu2+, Fe2+.
B. Fe3+, Ag+, Cu2+, Mg2+.
C. Ag+, Fe3+, Cu2+, Mg2+.
D. Ag+, Cu2+, Fe3+, Mg2+.
Cho Al đến dư vào dung dịch hỗn hợp gồm Cu(NO3)2, Ag(NO3)3, Mg(NO3)2, Fe(NO3)3 thì thứ tự các ion kim loại bị khử lần lượt là A. Ag+, Fe3+, Cu2+, Fe2+. B. Fe3+, Ag+, Cu2+, Mg2+. C. Ag+, Fe3+, Cu2+, Mg2+. D. Ag+, Cu2+, Fe3+, Mg2+.
Đọc tiếp
Cho Al đến dư vào dung dịch hỗn hợp gồm Cu(NO3)2, Ag(NO3)3, Mg(NO3)2, Fe(NO3)3 thì thứ tự các ion kim loại bị khử lần lượt là
A. Ag+, Fe3+, Cu2+, Fe2+.
B. Fe3+, Ag+, Cu2+, Mg2+.
C. Ag+, Fe3+, Cu2+, Mg2+.
D. Ag+, Cu2+, Fe3+, Mg2+.
Đáp án A
Ta có dãy điện hóa:
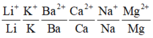
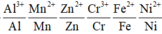
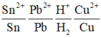
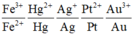
⇒ Thứ tự các ion kim loại bị khử lần lượt là Ag+ → Fe3+ → Cu2+ → Fe2+ ⇒ Chọn A.
Có thể loại 3 đáp án B C D và Chọn A luôn vì Al không tác dụng với Mg2+.
Đúng 0
Bình luận (0)
Nhiệt phân hoàn toàn hỗn hợp A gồm Al(NO3)3 và AgNO3 thu được hỗn hợp khí X gồm NO2, O2 có tỉ khối so với H2 bằng 21,25. Tính %m mỗi muối trong hỗn hợp A ban đầu
1) Hỗn hợp A gồm Al(NO3)3 , Cu(NO3)3, Pb(NO3)2. Biết thành phần % theo khối lượng của nguyên tố nitơ trong A là 14,43 %. Có thể điều chế được nhiều nhất bao nhiêu gam hh 3 kim loại từ 52,39g hh A?
2) Cho 1,69g hh A gồm Fe, Mg, Zn phản ứng với 202g dd HCl 0,75m (D=1,01 g/ml). Chứng tỏ rằng: hh A đã tan hết.
Al tác dụng với dung dịch HNO3 theo các sơ đồ phản ứng sau:
A
l
+
H
N
O
3
→
A
l
(
N
O
3
)
3
+
N
O
↑
+
H
2
O
A
l
+
H
N...
Đọc tiếp
Al tác dụng với dung dịch HNO3 theo các sơ đồ phản ứng sau:
A l + H N O 3 → A l ( N O 3 ) 3 + N O ↑ + H 2 O A l + H N O 3 → A l ( N O 3 ) 3 + N 2 O ↑ + H 2 O
Cho m gam Al tác dụng vừa đủ với dung dịch HNO3 tạo ra hỗn hợp khí A gồm 0,15mol NO và 0,05mol N2O (sản phẩm khử của N+5 chỉ có NO và N2O). Giá trị của m là
A. 7,85.
B. 7,76.
C. 7,65.
D. 8,85.
1.Hòa tan hoàn toàn 3,6 gam hỗn hợp bột kim loại M và oxit MO trong dung dịch H2SO4 dư thu được 14,4 gam muối.
a. Tìm kim loại M ?
b. Tính % khối lượng mỗi chất trong hỗn hợp ban đầu?
2.Cho hỗn hợp A gồm Mg(NO3)2, Al(NO3)3, Zn(NO3)2, Fe(NO3)3. Trong A nguyên tử oxi chiếm 60% về khối lượng. Tính tổng khối lượng kim loại có trong 2,5 tấn hỗn hợp A.
Nhiệt phân hoàn toàn hỗn hợp X gồm NaNO3; Al(NO3)3; Cu(NO3)2 thu được 10 gam chất rắn Y và hỗn hợp khí Z. Hấp thụ khí Z vào 112,5 gam H2O được dung dịch axit có nồng độ 12,5% và có 0,56 lít một khí duy nhất thoát ra (đktc). % khối lượng của NaNO3 trong hỗn hợp X là A. 17,49% B. 8,75% C. 42,5% D. 21,25%
Đọc tiếp
Nhiệt phân hoàn toàn hỗn hợp X gồm NaNO3; Al(NO3)3; Cu(NO3)2 thu được 10 gam chất rắn Y và hỗn hợp khí Z. Hấp thụ khí Z vào 112,5 gam H2O được dung dịch axit có nồng độ 12,5% và có 0,56 lít một khí duy nhất thoát ra (đktc). % khối lượng của NaNO3 trong hỗn hợp X là
A. 17,49%
B. 8,75%
C. 42,5%
D. 21,25%
Đáp án A
Nhiệt phân:
NaNO3→NaNO2+0,5O2(1)
0,05 ← 0,025
2Al(NO3)3→Al2O3+6NO2+1,5O2(2)
Cu(NO3)2→CuO+2NO2+0,5O2(3)
2NO2+0,5O2+H2O→2HNO3
x → 0,25x → x
nO2 dư=0,56/22,4=0,025=nO2(1)
C%HNO3=63x/(46x+0,25x.32+112,5)=0,125=> x=0,25 mol
=> nNO2=0,25 mol; nO2=nO2(2)+nO2(3)+nO2(1)=0,25x+0,025=0,0875 mol
BTKL: mX=mY+mNO2+mO2=10+0,25.46+0,0875.32=24,3 gam
%mNaNO3=0,05.85/24,3=17,49%
Đúng 0
Bình luận (0)
Nhiệt phân hoàn toàn hỗn hợp gồm NaNO3; Al(NO3)3; Cu(NO3)2, thu được 10 gam chất rắn Y và hỗn hợp khí. Hấp thụ khí Z vào 112,5 gam H2O được dung dịch axit có nồng độ 12,5% và có 0,56 lít một khí (đktc) duy nhất thoát ra. Phần trăm khối lượng của NaNO3 trong hỗn hợp X là A. 21,25% B. 42,5% C. 17,49% D. 8,75%
Đọc tiếp
Nhiệt phân hoàn toàn hỗn hợp gồm NaNO3; Al(NO3)3; Cu(NO3)2, thu được 10 gam chất rắn Y và hỗn hợp khí. Hấp thụ khí Z vào 112,5 gam H2O được dung dịch axit có nồng độ 12,5% và có 0,56 lít một khí (đktc) duy nhất thoát ra. Phần trăm khối lượng của NaNO3 trong hỗn hợp X là
A. 21,25%
B. 42,5%
C. 17,49%
D. 8,75%