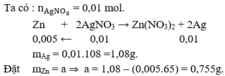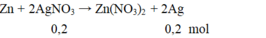Câu 27: Ngâm một lá trong 100ml dd AgNO3 0,1 mol/lit cho đến khi phản ứng kết thúc. Khối lượng Ag thu được là

Những câu hỏi liên quan
Ngâm một lá kẽm trong 100ml dung dịch AgNO3 0,1 mol. Kết thúc phản ứng, khối lượng lá kẽm là bao nhiêu?
A. 0,655g
B. 0,75g
C. 0,65g
D. 0,755g
Ngâm một lá kẽm (dư) vào trong 200ml dung dịch A g N O 3 0,5M. Khi phản ứng kết thúc khối lượng Ag thu được là
A. 8,8 g
B. 13 g
C. 6,5 g
D. 10,8 g
Ngâm một lá Zn dư vào 200 ml dung dịch A g N O 3 1M. Khi phản ứng kết thúc khối lượng Ag thu được là
A. 6,5 gam
B. 10,8 gam
C. 13 gam
D. 21,6 gam
Cho 0,1 mol glucozơ phản ứng với một lượng vừa đủ A g N O 3 trong N H 3 đun nóng. Kết thúc phản ứng thu được khối lượng Ag là
A. 1,08 gam
B. 10,08 gam
C. 2,16 gam
D. 21,6 gam
Câu 29: Ngâm 1 lá đồng trong dd AgNO3, sau khi phản ứng kết thúc, lấy lá đồng ra khỏi dd, rửa nhẹ, làm khô thấy khối lượng lá đồng tăng 1,52g. Khối lượng đồng tham gia phản ứng là
Gọi : \(n_{Cu\ pư} = a(mol)\)
\(Cu + 2AgNO_3 \to 2Ag + Cu(NO_3)_2\\ n_{Ag} = 2n_{Cu} = 2a(mol)\\ \Rightarrow 2a.108 - 64a = 1,52\\ \Rightarrow a = 0,01(mol)\\ m_{Cu\ pư} = 0,01.64 = 0,64(gam)\)
Đúng 1
Bình luận (0)
ngâm 1 lá kẻm trong 625 ml dd đồng 2 sunfat 0,1 m cho đến khi kẻm không tan được nửa a) viết pthh b) tính khối lượng đồng sau phản ứng C) lọc bỏ chất rắn lấy dd thu được cho tác dụng với dd NaOH và thu được kết tủa đung nóng đến khối lượng không đổi thu được mgam chất rắn tìm m
Đọc tiếp
ngâm 1 lá kẻm trong 625 ml dd đồng 2 sunfat 0,1 m cho đến khi kẻm không tan được nửa
a) viết pthh
b) tính khối lượng đồng sau phản ứng
C) lọc bỏ chất rắn lấy dd thu được cho tác dụng với dd NaOH và thu được kết tủa đung nóng đến khối lượng không đổi thu được mgam chất rắn tìm m
\(n_{CuSO_4}=0,1.0,625=0,0625mol\\ a)Zn+CuSO_4\rightarrow ZnSO_4+Cu\)
\(b)n_{Cu}=n_{CuSO_4}=0,0625mol\\
m_{Cu}=0,0625.64=4g\\
c)ZnSO_4+2NaOH\rightarrow Zn\left(OH\right)_2+Na_2SO_4\\
Zn\left(OH\right)_2\xrightarrow[]{t^0}ZnO+H_2O\\
n_{ZnO}=n_{Zn\left(OH\right)_2}=n_{ZnSO_4}=0,0625mol\\
m=m_{ZnO}=0,0625.81=5,0625g\)
Đúng 1
Bình luận (0)
Ngâm một lá kẽm trong 100 ml dung dịch AgNO3 0,2M. Khi phản ứng kết thúc, khối lượng lá kẽm tăng thêm
A. 0,65 gam.
B. 0,86 gam.
C. 1,51 gam.
D. 2,16 gam.
Đáp án C
nAgNO3 = 0,1.0,2 = 0,02 mol
Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
Mol 0,01 ¬ 0,02 → 0,02
=> mThanh KL tăng = mAg – mZn = 108.0,02 – 65.0,01 = 1,51g
Đúng 0
Bình luận (0)
Ngâm một lá đồng trong 20ml dd AgNO3 .Phản ứng xong láy lá đồng ra , rửa nhẹ , làm khô , khối lượng lá đồng tăng thêm 1,52g
a)Xác định nồng độ mol của dd AgNO3 đã dùng
b)Tính nồng độ % của dd thu được sau phản ứng , biết khối lượng riêng của dd này là 1,1g/ml và thể tích của dd sau phản ứng thay đổi không đáng để
Ngâm một lá kẽm trong 25,5 gam dung dịch muối AgNO3 20% cho đến khi phản ứng kết thúc
a) tính khối lượng Zn đã phản ứng
b) lấy lá kẽm ra khỏi dung dịch làm khô hỏi lá kẽm tăng hay giảm
mAgNO3=5,1g
=> nAgNO3=0,03mol
PTHH: Zn+ 2AgNO3=>Zn(NO3)2+2Ag
0,06 <-0,03 ->0,03 ->0,06
mZn đã dùng:m=0,06.65=3,9g
Đúng 0
Bình luận (0)