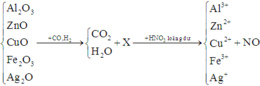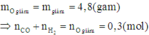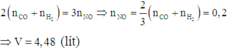khử 6,96g một oxit sắt bằng lượng dư khí CO, thu được hh khí A và chất rắn B. Dẫn toàn bộ A đi từ từ qua lượng dư dd Ca(OH)2 thì thấy khối lượng dd sau pứ giảm 6,72g so với ban đầu. Cho toàn bộ B pứ với 100ml dd hh gồm AgNO3 1,2M và Cu(NO3)2 0,6M thì thu được m (g) chất rắn C
biết các pứ xảy ra hoàn toàn
Xác định CTPT của oxt sắt và tính giá trị m (g)