Đốt cháy hoàn toàn 6 g một chất hữu cơ X trong oxi dư. Sau phản ứng, dẫn hh lần lượt qua bình 1 chứa P2O5 khan và bình 2 chứa Ca(OH)2 (đều lấy dư) thì thấy khối lượng bình 1 tăng 3,6 g còn bình 2 tăng 8,8 g. Xác định CTPT và viết CTCT của X, biết tỉ khối của X so với nitơ oxit là 2.

Những câu hỏi liên quan
Đốt cháy hết 9,2 gam một chất hữu cơ X bằng khí O2 vừa đủ, thu đuợc hỗn hợp khí và hơi. Dẫn toàn bộ sản phẩm thu được lần lượt qua bình 1 chứa H2SO4 đậm đặc dư và bình 2 chứa dung dịch nước vôi trong dư thì bình 1 tăng m1 gam, còn bình 2 tăng 17,6 gam. Cũng đốt cháy một lượng chất X như trên, nhưng dẫn hỗn hợp khí sau khi đốt cháy lần luợt qua bình 1 chứa CaO dư và bình 2 chứa P2O5 dư thì thấy bình 1 tăng lên 28,4 gam, còn bình 2 tăng lên m2 gam. Công thức phân tử của chất X là: A. C3H6O2 B. C2...
Đọc tiếp
Đốt cháy hết 9,2 gam một chất hữu cơ X bằng khí O2 vừa đủ, thu đuợc hỗn hợp khí và hơi. Dẫn toàn bộ sản phẩm thu được lần lượt qua bình 1 chứa H2SO4 đậm đặc dư và bình 2 chứa dung dịch nước vôi trong dư thì bình 1 tăng m1 gam, còn bình 2 tăng 17,6 gam. Cũng đốt cháy một lượng chất X như trên, nhưng dẫn hỗn hợp khí sau khi đốt cháy lần luợt qua bình 1 chứa CaO dư và bình 2 chứa P2O5 dư thì thấy bình 1 tăng lên 28,4 gam, còn bình 2 tăng lên m2 gam. Công thức phân tử của chất X là:
A. C3H6O2
B. C2H6O
C. C2H6O2
D. C3H8O
Gọi công thức phân tử của X là CxHyOz .
Sản phẩm cháy gồm CO2 và H2O.
Ở lần thí nghiệm thứ nhất, bình 1 chứa H2SO4 đậm đặc dư hấp thụ H2O và bình 2 chứa dung dịch nước vôi trong dư hấp thụ CO2.
Ở lần thí nghiệm thứ hai, bình 1 chứa CaO dư hấp thụ CO2 và toàn bộ hơi nước, bình 2 chứa P2O5 dư không hấp thụ gì vì toàn bộ lượng khí đã được hấp thụ ở bình 1. Do đó m2 = 0. Theo định luật bảo toàn khối lượng ta có
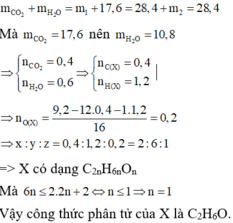
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 6,0 gam một chất hữu cơ X. Sau phản ứng dẫn hỗn hợp sản phẩm cháy qua lần lượt các bình: - Bình 1: đựng dung dịch H2SO4 đặc nóng. - Bình 2: đựng dung dịch nước vôi trong (Ca(OH)2) dư. Thấy khối lượng bình 1 tăng 7,2 gam. Bình 2 xuất hiện 30 gam kết tủa. Công thức đơn giản nhất của X là: A. C3H8O. B. C3H6O. C. C2H6O. D. C3H8.
Đọc tiếp
Đốt cháy hoàn toàn 6,0 gam một chất hữu cơ X. Sau phản ứng dẫn hỗn hợp sản phẩm cháy qua lần lượt các bình:
- Bình 1: đựng dung dịch H2SO4 đặc nóng.
- Bình 2: đựng dung dịch nước vôi trong (Ca(OH)2) dư.
Thấy khối lượng bình 1 tăng 7,2 gam. Bình 2 xuất hiện 30 gam kết tủa.
Công thức đơn giản nhất của X là:
A. C3H8O.
B. C3H6O.
C. C2H6O.
D. C3H8.
Đáp án A
Đốt cháy X tạo CO2 và H2O
Bình 1 giữ lại H2O => mH2O = 7,2g => nH = 2nH2O = 0,8 mol
Bình 2 giữ lại CO2 : nCaCO3 = nCO2 = 0,3 mol
Có : mC + mH + mO = mX => nO = 0,1mol
=> nC : nH : nO = 0,3 : 0,8 : 0,1 = 3 : 8 : 1
Vậy CTĐG nhất của X là C3H8O
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 1 lượng hỗn hợp 2 este. Dẫn sản phẩm cháy lần lượt qua bình (1) đựng
P
2
O
5
dư và bình (2) đựng dung dịch
Ca
(
OH
)
2
dư, thấy khối lượng bình (1) tăng 6,21 gam, còn bình (2) thì được 34,5 gam kết tủa. Các este trên thuộc loại este nào sau đây A. Este không no B. Este thơm C....
Đọc tiếp
Đốt cháy hoàn toàn 1 lượng hỗn hợp 2 este. Dẫn sản phẩm cháy lần lượt qua bình (1) đựng P 2 O 5 dư và bình (2) đựng dung dịch Ca ( OH ) 2 dư, thấy khối lượng bình (1) tăng 6,21 gam, còn bình (2) thì được 34,5 gam kết tủa. Các este trên thuộc loại este nào sau đây
A. Este không no
B. Este thơm
C. Este no, đơn chức, mạch hở
D. Este đa chức
Đốt cháy hoàn toàn a gam hỗn hợp các hidrocacbon trong oxi dư, sau phản ứng dẫn hỗn hợp sản phẩm qua lần lượt bình 1 đựng CuSO4 khan dư; bình 2 đựng dung dịch NaOH dư. Biết khối lượng bình 1 và bình 2 tăng lên lần lượt 6,3 gam và 17,6 gam. Xác định giá trị của a
Ta có: \(n_{H_2O}=\dfrac{6,3}{18}=0,35\left(mol\right)\Rightarrow n_H=0,35.2=0,7\left(mol\right)\)
\(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)=n_C\)
⇒ a = mC + mH = 0,4.12 + 0,7.1 = 5,5 (g)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 1 lượng hỗn hợp 2 este. Dẫn sản phẩm cháy lần lượt qua bình (1) đựng P2O5 dư và bình (2) đựng dung dịch Ca(OH)2 dư, thấy khối lượng bình (1) tăng 6,21 gam, còn bình (2) thì được 34,5 gam kết tủa. Các este trên thuộc loại este nào dưới đây? A. Este no, đơn chức, mạch hở. B. Este không no. C. Este thơm. D. Este đa chức.
Đọc tiếp
Đốt cháy hoàn toàn 1 lượng hỗn hợp 2 este. Dẫn sản phẩm cháy lần lượt qua bình (1) đựng P2O5 dư và bình (2) đựng dung dịch Ca(OH)2 dư, thấy khối lượng bình (1) tăng 6,21 gam, còn bình (2) thì được 34,5 gam kết tủa. Các este trên thuộc loại este nào dưới đây?
A. Este no, đơn chức, mạch hở.
B. Este không no.
C. Este thơm.
D. Este đa chức.
Đốt cháy hoàn toàn 1 lượng hỗn hợp 2 este. Dẫn sản phẩm cháy lần lượt qua bình (1) đựng P2O5 dư và bình (2) đựng dung dịch Ca(OH)2 dư, thấy khối lượng bình (1) tăng 6,21 gam, còn bình (2) thì được 34,5 gam kết tủa. Các este trên thuộc loại este nào dưới đây? A. Este no, đơn chức, mạch hở B. Este không no C. Este thơm D. Este đa chức
Đọc tiếp
Đốt cháy hoàn toàn 1 lượng hỗn hợp 2 este. Dẫn sản phẩm cháy lần lượt qua bình (1) đựng P2O5 dư và bình (2) đựng dung dịch Ca(OH)2 dư, thấy khối lượng bình (1) tăng 6,21 gam, còn bình (2) thì được 34,5 gam kết tủa. Các este trên thuộc loại este nào dưới đây?
A. Este no, đơn chức, mạch hở
B. Este không no
C. Este thơm
D. Este đa chức
Đốt cháy hoàn toàn 5,4 gam hợp chất hữu cơ thơm X (trong phân tử chỉ chứa C, H, O) sản phẩm thu được lần lượt cho qua bình 1 đựng H2SO4 đặc, bình 2 đựng dung dịch Ca(OH)2 dư sau phản ứng thấy bình 1 tăng 3,6 gam, bình 2 tạo thành 35 gam kết tủa. X tác dụng được với Na sinh ra H2 và MX 120. Số công thức cấu tạo của X là: A. 4 B. 1 C. 2 D. 3
Đọc tiếp
Đốt cháy hoàn toàn 5,4 gam hợp chất hữu cơ thơm X (trong phân tử chỉ chứa C, H, O) sản phẩm thu được lần lượt cho qua bình 1 đựng H2SO4 đặc, bình 2 đựng dung dịch Ca(OH)2 dư sau phản ứng thấy bình 1 tăng 3,6 gam, bình 2 tạo thành 35 gam kết tủa. X tác dụng được với Na sinh ra H2 và MX < 120. Số công thức cấu tạo của X là:
A. 4
B. 1
C. 2
D. 3
Đáp án A
nCO2=nCaCO3=35/100=0,35 mol
nH2O=3,6/18=0,2 mol
=>mO=mX-mC-mH=5,4 -12.0,35-1.2.0,2=0,8 g
=> nO=0,05 mol
nC:nH:nO=0,35:0,4:0,05=7:8:1
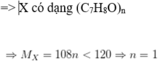
=> CTPT của X là C7H8O
X phản ứng với Na suy ra X có nhóm -OH => Các CTCT của X là
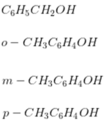
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 1 lượng hỗn hợp 2 este. Dẫn sản phẩm cháy lần lượt qua bình (1) đựng P2O5 dư và bình (2) đựng dung dịch Ca(OH)2 dư, thấy khối lượng bình (1) tăng 6,21 gam, còn bình (2) thi được 34,5 gam kết tủa. Các este trên thuộc loại este nào sau đây ? A. Este no, đơn chức, mạch hở B. Este không no C. Este thơm D. Este đa chức
Đọc tiếp
Đốt cháy hoàn toàn 1 lượng hỗn hợp 2 este. Dẫn sản phẩm cháy lần lượt qua bình (1) đựng P2O5 dư và bình (2) đựng dung dịch Ca(OH)2 dư, thấy khối lượng bình (1) tăng 6,21 gam, còn bình (2) thi được 34,5 gam kết tủa. Các este trên thuộc loại este nào sau đây ?
A. Este no, đơn chức, mạch hở
B. Este không no
C. Este thơm
D. Este đa chức
Đốt cháy hoàn toàn 1 lượng hỗn hợp 2 este. Dẫn sản phẩm cháy lần lượt qua bình (1) đựng P2O5 dư và bình (2) đựng dung dịch Ca(OH)2 dư, thấy khối lượng bình (1) tăng 6,21 gam, còn bình (2) thi được 34,5 gam kết tủa. Các este trên thuộc loại este nào sau đây ? A. Este no, đơn chức, mạch hở B. Este không no C. Este thơm D. Este đa chức
Đọc tiếp
Đốt cháy hoàn toàn 1 lượng hỗn hợp 2 este. Dẫn sản phẩm cháy lần lượt qua bình (1) đựng P2O5 dư và bình (2) đựng dung dịch Ca(OH)2 dư, thấy khối lượng bình (1) tăng 6,21 gam, còn bình (2) thi được 34,5 gam kết tủa. Các este trên thuộc loại este nào sau đây ?
A. Este no, đơn chức, mạch hở
B. Este không no
C. Este thơm
D. Este đa chức
Đáp án A
- Đốt cháy hỗn hợp este thì
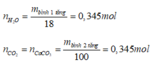
- Nhận thấy rằng
![]()
nên trong X chỉ chứa các este no, đơn chức, mạch hở.
Đúng 0
Bình luận (0)







