Cho m gam hỗn hợp gồm Al và Mg có cùng số mol tác dụng hết với O2 thì khối lượng chất rắn thu được có giá trị m+2(g). Tìm m.

Những câu hỏi liên quan
Cho 11,6 gam hỗn hợp X gồm Mg, Al và Zn tác dụng hoàn toàn với dung dịch AgNO3 dư thấy khối lượng chất rắn tăng 64 gam. Nếu cho 11,6 gam X tác dụng hết với oxi thì thu được m gam chất rắn. Giá trị của m là: A. 17,2 B. 14,4 C. 22,8 D. 16,34
Đọc tiếp
Cho 11,6 gam hỗn hợp X gồm Mg, Al và Zn tác dụng hoàn toàn với dung dịch AgNO3 dư thấy khối lượng chất rắn tăng 64 gam. Nếu cho 11,6 gam X tác dụng hết với oxi thì thu được m gam chất rắn. Giá trị của m là:
A. 17,2
B. 14,4
C. 22,8
D. 16,34
Đáp án A
Vì AgNO3 dư nên chất rắn sau phản ứng chỉ là Ag.
![]()
Các kim loại trong hỗn hợp X đều có hóa trị không đổi nên theo định luật bảo toàn mol electron, ta có:
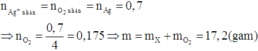
Đúng 0
Bình luận (0)
Cho m gam hỗn hợp H gồm
A
l
,
M
g
O
,
A
l
C
l
3
,
M
g
(
N
O...
Đọc tiếp
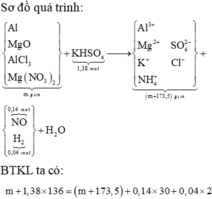
Cho m gam hỗn hợp H gồm A l , M g O , A l C l 3 , M g ( N O 3 ) 2 tác dụng vừa đủ với dung dịch chứa 1 , 38 m o l K H S O 4 , kết thúc phản ứng thu được 0 , 14 m o l N O ; dung dịch X chứa ( m + 173,5) gam muối trung hòa. Cho dung dịch X tác dụng với dung dịch NaOH thì lượng kết tủa thu được là lớn nhất, nung kết tủa đến khối lượng không đổi thu được 29 gam chất rắn. Phần trăm khối lượng A l C l 3 trong H có giá trị gần nhất với giá trị nào sau đây?
A. 33
B. 22
C. 34
D. 25
Cho 27,25 gam hỗn hợp X gồm Mg, Al, Fe, Cu tác dụng với O2 thu được m gam hỗn hợp chất rắn Y. Cho toàn bộ Y tác dụng với dung dịch H2SO4 đặc, nóng, thu được dung dịch Z (chứa 5 muối, với tổng khối lượng muối là 96,85 (gam) và 10,64 lít (đktc) khí SO2 duy nhất. Giá trị của m là A. 38,85. B. 31,25. C. 34,85. D. 20,45.
Đọc tiếp
Cho 27,25 gam hỗn hợp X gồm Mg, Al, Fe, Cu tác dụng với O2 thu được m gam hỗn hợp chất rắn Y. Cho toàn bộ Y tác dụng với dung dịch H2SO4 đặc, nóng, thu được dung dịch Z (chứa 5 muối, với tổng khối lượng muối là 96,85 (gam) và 10,64 lít (đktc) khí SO2 duy nhất. Giá trị của m là
A. 38,85.
B. 31,25.
C. 34,85.
D. 20,45.
Cho hỗn hợp X gồm 4,08g Mg và 2,7g Al tác dụng vừa đủ với V lít (đktc) hỗn hợp khí Y gồm Cl2 và O2(có tỉ khối so với H2 là 23,8), thu được m gam hỗn hợp rắn Z. Giá trị m là
\(n_{Mg}=\dfrac{4,08}{24}=0,17\left(mol\right)\)
\(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
Gọi số mol Cl2 và O2 là a, b
Mg0-2e-->Mg+2
0,17->0,34
Al0-3e-->Al+3
0,1->0,3
Cl20 +2e--> 2Cl-
a--->2a
O20 +4e --> 2O2-
b--->4b
Bảo toàn e: 2a + 4b = 0,64
Có \(\dfrac{71a+32b}{a+b}=23,8.2=47,6\)
=> a = 0,08; b = 0,12
=> mZ = 4,08 + 2,7 + 0,08.71 + 0,12.32 = 16,3 (g)
Đúng 1
Bình luận (0)
Cho m gam hỗn hợp H gồm Al, MgO, AlCl3, Mg(NO3)2 tác dụng vừa đủ với dung dich chứa 1,38 mol KHSO4, kết thúc phản ứng thu được 0,14 mol NO; 0,04 mol H2; dung dịch X chứa (m + 173,5) gam muối trung hòa. Cho dung dịch X tác dụng với dung dịch NaOH thì lượng kết tủa thu được là lớn nhất, nung kết tủa đến khối lượng không đổi thu được 29 gam chất rắn. Phần trăm khối lượng AlCl3 trong H có giá trị gần nhất với A. 33% B. 22% C. 34% D. 25%
Đọc tiếp
Cho m gam hỗn hợp H gồm Al, MgO, AlCl3, Mg(NO3)2 tác dụng vừa đủ với dung dich chứa 1,38 mol KHSO4, kết thúc phản ứng thu được 0,14 mol NO; 0,04 mol H2; dung dịch X chứa (m + 173,5) gam muối trung hòa. Cho dung dịch X tác dụng với dung dịch NaOH thì lượng kết tủa thu được là lớn nhất, nung kết tủa đến khối lượng không đổi thu được 29 gam chất rắn. Phần trăm khối lượng AlCl3 trong H có giá trị gần nhất với
A. 33%
B. 22%
C. 34%
D. 25%
Cho m gam hỗn hợp H gồm Al, MgO, AlCl3, Mg(NO3)2 tác dụng vừa đủ với dung dịch chứa 1,38 mol KHSO4, kết thúc phản ứng thu được 0,14 mol NO; 0,04 mol H2; dung dịch X chứa ( m + 173,5) gam muối trung hòa. Cho dung dịch X tác dụng với dung dịch NaOH thì lượng kết tủa thu được là lớn nhất, nung kết tủa đến khối lượng không đổi thu được 29 gam chất rắn. Phần trăm khối lượng AlCl3 trong H có giá trị gần nhất với giá trị nào sau đây? A. 33. B. 22. C. 34. D. 25.
Đọc tiếp
Cho m gam hỗn hợp H gồm Al, MgO, AlCl3, Mg(NO3)2 tác dụng vừa đủ với dung dịch chứa 1,38 mol KHSO4, kết thúc phản ứng thu được 0,14 mol NO; 0,04 mol H2; dung dịch X chứa ( m + 173,5) gam muối trung hòa. Cho dung dịch X tác dụng với dung dịch NaOH thì lượng kết tủa thu được là lớn nhất, nung kết tủa đến khối lượng không đổi thu được 29 gam chất rắn. Phần trăm khối lượng AlCl3 trong H có giá trị gần nhất với giá trị nào sau đây?
A. 33.
B. 22.
C. 34.
D. 25.
Đáp án A
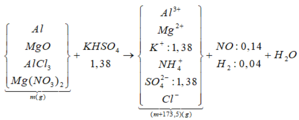
Sinh khí H2 ⇒ dung dịch X không chứa NO3–. Al là kim loại mạnh ⇒ chú ý có NH4+!
► Ta có sơ đồ phản ứng sau:
A. 6,912.
Đúng 0
Bình luận (0)
Cho m gam hỗn hợp H gồm Al, MgO, AlCl3, Mg(NO3)2 tác dụng vừa đủ với dung dịch chứa 1,38 gam KHSO4, kết thúc phản ứng thu được 0,14 mol NO; 0,04 mol H2; dung dịch X chứa (m + 173,5) gam muối trung hòa. Cho dung dịch X tác dụng với dung dịch NaOH thì lượng kết tủa thu được là lớn nhất, nung kết tủa đến khối lượng không đổi thu được 29 gam chất rắn. Phần trăm khối lượng AlCl3 trong H có giá trị gần nhất với giá trị nào sau đây? A. 33. B. 22. C. 34. D. 25.
Đọc tiếp
Cho m gam hỗn hợp H gồm Al, MgO, AlCl3, Mg(NO3)2 tác dụng vừa đủ với dung dịch chứa 1,38 gam KHSO4, kết thúc phản ứng thu được 0,14 mol NO; 0,04 mol H2; dung dịch X chứa (m + 173,5) gam muối trung hòa. Cho dung dịch X tác dụng với dung dịch NaOH thì lượng kết tủa thu được là lớn nhất, nung kết tủa đến khối lượng không đổi thu được 29 gam chất rắn. Phần trăm khối lượng AlCl3 trong H có giá trị gần nhất với giá trị nào sau đây?
A. 33.
B. 22.
C. 34.
D. 25.
Cho m gam hỗn hợp H gồm
Al
,
MgO
,
AlCl
3
,
Mg
(
NO
3
)
2
tác dụng vừa đủ với dung dịch chứa
1
,
38
mol...
Đọc tiếp
Cho m gam hỗn hợp H gồm Al , MgO , AlCl 3 , Mg ( NO 3 ) 2 tác dụng vừa đủ với dung dịch chứa 1 , 38 mol KHSO 4 , kết thúc phản ứng thu được 0 , 14 mol NO ; 0 , 04 mol H 2 ; dung dịch X chứa ( m + 173,5) gam muối trung hòa. Cho dung dịch X tác dụng với dung dịch NaOH thì lượng kết tủa thu được là lớn nhất, nung kết tủa đến khối lượng không đổi thu được 29 gam chất rắn. Phần trăm khối lượng AlCl3 trong H có giá trị gần nhất với giá trị nào sau đây
A. 33
B. 22
C. 34
D. 25
Cho m (gam) hỗn hợp 2 kim loại Mg và Al có cùng số mol phản ứng với oxi. sau phản ứng xảy ra hoàn toàn thu được hỗn hợp chất rắn có khối lượng tăng so với khối lượng ban đầu là 4 (gam). tính m
Ta có :
$m_{O_2\ pư} = m_{tăng} = 4(gam) \Rightarrow n_{O_2} = \dfrac{4}{32} = 0,125(mol)$
Gọi $n_{Mg} = n_{Al} = a(mol)$
$2Mg + O_2 \xrightarrow{t^o} 2MgO$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
Theo PTHH : $n_{O_2} = 0,5a + 0,75a = 0,125 \Rightarrow a = 0,1(mol)$
$\Rightarrow m = 0,1.24 + 0,1.27 = 5,1(gam)$
Đúng 0
Bình luận (0)