Đốt cháy hoàn toàn 6,72 lít hỗn hợp khí X gồm một hiđrocacbon CxHy và các bon oxit thì cần dùng vừa đủ 13,44 lít khí O2 thu được 22 g CO2 và 72 g hơi nước tìm công thức phân tử của cxhy và phần trăm theo thể tích của mỗi khí trong hỗn hợp X
Đốt cháy hoàn toàn 6,72 lít (điều kiện tiêu chuẩn) hỗn hợp khí x gồm hiđrocacbon CxHy và Cacbon oxit CO thì cần dùng vừa đủ 13,44 lít khí O2 (điều kiện tiêu chuẩ)n thu được 22 g CO2 và 7,2 g hơi nước tìm công thức phân tử của cxhy và phần trăm theo thể tích của mỗi khi trong hỗn hợp X
CxHy:a(mol)
CO:b(mol)
=>a+b\(=\dfrac{6,72}{22,4}\)=0,3(mol)
nCO2=\(\dfrac{22}{44}\)=0,5(mol)
nH2O=\(\dfrac{7,2}{18}\)=0,4(mol)
nO2=\(\dfrac{13,44}{22,4}\)=0,6(mol)
Bảo toàn C: ax + b = 0,5
Bảo toàn H: ay = 0,8
Bảo toàn O: b + 0,6.2 = 0,5.2 + 0,4
=> b = 0,2 (mol)
=> a = 0,1 (mol)
=> x = 3 ; y = 8 => CTPT: C3H8
%VC3H8=\(\dfrac{0,1}{0,3}\).100%=33,33%
%VCO=\(\dfrac{0,2}{0,3}\).100%=66,67%
Đốt cháy hoàn toàn 1 lít hỗn hợp khí gồm ankin X và hiđrocacbon Y cần dùng 2,25 lít khí O2, thu được 1,5 lít khí CO2 (các thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất). Công thức phân tử của X và Y lần lượt là:
A. C2H2 và CH4
B. C3H4 và C2H6
C. C2H2 và C2H4
D. C3H4 và CH4
Hỗn hợp M chứa hai chất hữu cơ thuộc cùng dãy đồng đẳng và hơn kém nhau 2 nguyên tử cacbon. Nếu làm bay hơi 7,28 g M thì thể tích hơi thu được đúng bằng thể tích của 2,94 g khí N 2 ở cùng điều kiện. Để đốt cháy hoàn toàn 5,20 g hỗn hợp M cần dùng vừa hết 5,04 lít O 2 (đktc). Sản phẩm cháy chỉ gồm C O 2 và hơi nước với thể tích bằng nhau.
Hãy xác định công thức phân tử và phần trăm khối lượng từng chất trong hỗn hợp M.
Số mol 2 chất trong 7,28g M: 
Số mol 2 chất trong 5,2g M: 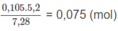
Theo định luật bảo toàn khối lượng:
m C O 2 + m H 2 O = m M + m O 2 = 12.4(g)
Theo đầu bài, số mol C O 2 = số mol H 2 O = n.
44n + 18n = 12,4 ⇒ n = 0,2 (mol)
Các chất trong hỗn hợp có chứa C, H và có thể có O. Chất thứ nhất là C X H Y O Z (a mol) và chất thứ 2 là C X + 2 H Y + 4 O Z (b mol).
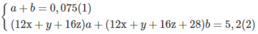
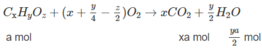
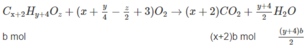
xa + (x + 2)b = 0,2 (3)
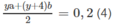
Giải hệ phương trình :
Từ (3) ta có x(a + b) + 2b = 0,200
2b = 0,200 - 0,0750x
b = 0,100 - 0,0375x
0 < b < 0,075 ⇒ 0 < 0,100 - 0,0375x < 0,0750
⇒ 0,660 < X < 2,66
Trong khoảng này có 2 số nguyên là 1 và 2.
Nếu x = 1.
b = 0,100 - 3.75. 10 - 2 = 0,0625
a = 0,0750 - 0,0625 = 0,0125.
Thay giá trị của a và b vào (4) ta có :
0125y + 0,0625(y + 4) = 0,400
⇒ y = 2.
Thay x = 1, y = 2; a = 0,0125, b = 0,0625 vào (2):
(14 + 16z).0,0125 + (42 + 16z).0,0625 = 5,20
⇒ z = 2.
C
H
2
O
2
chiếm: 
C 3 H 6 O 2 chiếm: 100% - 11,1% = 88,9%.
Nếu x = 2 .
b = 0,100 - 0,0375 X 2 = 0,0250
a = 0,0750 - 0,0250 = 0,05
từ đó tìm tiếp, ta được y = 4 và z = 2.
% khối lượng của
C
2
H
4
O
2
: 
% khối lương của C 4 H 8 O 2 : 100% - 57,7% = 42,3%.
Đốt cháy hoàn toàn 6g hidrocacbon (CxHy)A thu được 17,6g CO2 biết tỉ khối hơi của A với hidrocacbon là15 a/ tìm số g các nguyên tố trong A b/ tìm coing thức phân tử A c/ đốt cháy 1,5g A cần bao nhiêu lít khí O2 (đktc)
a, Ta có: \(n_C=n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)\)
\(\Rightarrow m_C=0,4.12=4,8\left(g\right)\)
\(\Rightarrow m_H=6-4,8=1,2\left(g\right)\)
b, Ta có: \(n_H=\dfrac{1,2}{1}=1,2\left(mol\right)\)
\(\Rightarrow x:y=0,4:1,2=1:3\)
→ CTPT của A có dạng là (CH3)n.
Mà: MA = 15.2 = 30 (g/mol)
\(\Rightarrow n=\dfrac{30}{12+3}=2\)
Vậy: CTPT của A là C2H6.
c, Ta có: \(n_A=\dfrac{1,5}{30}=0,05\left(mol\right)\)
PT: \(2C_2H_6+7O_2\underrightarrow{t^o}4CO_2+6H_2O\)
Theo PT: \(n_{O_2}=\dfrac{7}{2}n_{C_2H_6}=0,175\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,175.22,4=3,92\left(l\right)\)
Đốt cháy hoàn toàn 0,3 mol hỗn hợp X gồm hiđrocacbon A và hợp chất hữu cơ B có công thức CxHyOz ( x ≥ 2 ), cần dùng vừa đủ 14,56 lít O2 (đktc), thu được 8,96 lít CO2 (đktc) và 9,9 gam H2O. Xác định công thức phân tử của A và B
Hỗn hợp G gồm hai este được tạo thành từ cùng một ancol và hai axit cacboxylic là đồng đẳng kế tiếp. Đốt cháy hoàn toàn G cần vừa đủ 5,12 gam khí O2, thu được 3,136 lít khí CO2 (đktc) và 2,52 gam H2O. Phần trăm số mol của este có phân tử khối nhỏ hơn trong G là
A. 80%.
B. 40%.
C. 20%.
D. 60%.
Chọn đáp án C
đốt cháy G cần 0 , 16 m o l O 2 → t 0 0 , 14 m o l C O 2 + 0 , 14 m o l H 2 O
n C O 2 = n H 2 O chứng tỏ G là hỗn hợp este no, đơn chức, mạch hở dạng CnH2nO2.
G chứa 2O nên bảo toàn O có 2 n G + 2 n O 2 = 2 n C O 2 + n H 2 O
→ nG = 0,05 mol.
→ n = 0,14 ÷ 0,05 = 2,8
→ G gồm C2H4O2 và C3H6O2.
Sơ đồ chéo hoặc giải hệ có n C 2 H 4 O 2 = 0 , 01 m o l và n C 3 H 6 O 2 = 0 , 04 m o l
→ % s ố m o l e s t e c ó P T K n h ỏ h ơ n = 0 , 01 : 0 , 05 = 20 %
Hỗn hợp M gồm hai hiđrocacbon đồng đẳng kế tiếp X, Y (MX < MY). Đốt cháy hoàn toàn m
gam M cần dùng vừa đủ 17,36 lít O2 (đktc), thu được CO2 và 11,7 gam H2O. Công thức phân tử của
X là
Hỗn hợp X gồm ankan Y và hai amin no, đơn chức, mạch hở, kế tiếp nhau trong dãy đồng đẳng. Đốt cháy hoàn toàn 3,95 gam X cần vừa đủ 8,12 lít O2 (đktc), thu được 0,57 mol hỗn hợp khí và hơi gồm N2, H2O và CO2. Công thức phân tử của Y là
A. CH4.
B. C2H6.
C. C3H8.
D. C4H10.
Đốt cháy hoàn toàn 0,01 mol chất hữu cơ X cần vừa đủ 0,616 lít O2. Sau thí nghiệm thu được hỗn hợp sản phẩm Y gồm : CO2, N2 và hơi H2O. Làm lạnh để ngưng tụ hơi H2O chỉ còn 0,56 lít hỗn hợp khí Z (có tỉ khối hơi với H2 là 20,4). Biết thể tích các khí đều đo ở đktc. Công thức phân tử X là
A. C2H5ON hoặc C2H7O2N
B. C2H5O2N
C. C2H7O2N
D. C2H5ON