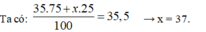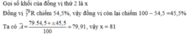Nguyên tố photpho có hai đồng vị, trong đó đồng vị thứ nhất là chiếm 3% về số nguyên tử; đồng vị thứ hai nhiều hơn đồng vị thứ nhất là 1 nơtron.
a. (1,0 điểm) Tính nguyên tử khối trung bình của photpho.
b. (1,0 điểm) Tính thành phần phần trăm về khối lượng của photpho trong hợp chất khí với hiđro?