Đốt cháy 28,6 gam hỗn hợp gồm Al, Zn, Mg thu được 44,6 gam hỗn hợp oxit. Hòa tan hết oxit trong dung dịch HCl thu được dung dịch D. Cô cạn dung dịch D thu m gam chất muối khan là
A. 99,6 gam
B. 74,7 gam
C. 49,8 gam
D. 100,8 gam
Đốt cháy 28,6 gam hỗn hợp gồm Al, Zn, Mg thu được 44,6 gam hỗn hợp oxit. Hòa tan hết oxit trong dung dịch HCl thu được dung dịch D. Cô cạn dung dịch D thu m gam chất muối khan là
A. 99,6 gam
B. 74,7 gam
C. 49,8 gam
D. 100,8 gam
Trong oxit, mO=44,6-28,6=16 gam =>nO=1 mol
Bảo toàn điện tích trong muối =1.2=2 mol
=>m Muối=28,6+2.35,5=99,6 gam
Đáp án là A
Oxi hóa hoàn toàn 28,6 gam hỗn hợp X gồm Al, Zn, Mg bằng oxi hóa dư thu được 44,6 gam hỗn hợp oxit Y. Hòa tan hết Y trong dung dịch HCl thu được dung dịch Z. Cô cạn dung dịch Z được hỗn hợp muối khan là
A. 49,8 gam.
B. 100,8 gam.
C. 74,7 gam.
D. 99,6 gam.
Oxi hóa hoàn toàn 28,6 gam hỗn hợp X gồm Al , Zn và Mg bằng oxi dư , thu được 44,6 gam hỗn hợp oxit Y. Hòa tan hoàn toàn Y bằng lượng vừa đủ dung dịch HCl 1M , thu được dung dịch Z. Cô cạn Z , thu được m gam muối khan . Tính giá trị của V và m.
Bảo toàn khối lượng :
\(m_{O_2}=44.6-28.6=16\left(g\right)\)
\(n_{O_2}=\dfrac{16}{32}=0.5\left(mol\right)\)
Bảo toàn O :
\(n_{H_2O}=2n_{O_2}=2\cdot0.5=1\left(mol\right)\)
Bảo toàn H :
\(n_{HCl}=2\cdot n_{H_2O}=2\cdot1=2\left(mol\right)\)
\(V_{dd_{HCl}}=\dfrac{2}{1}=2\left(l\right)\)
Bảo toàn khối lượng :
\(m_{Muối}=44.6+2\cdot36.5-1\cdot18=99.6\left(g\right)\)
\(n_O=\dfrac{44,6-28,6}{16}=1\left(mol\right)\)
\(n_{HCl}=n_{Cl^-}=n_O=2\left(mol\right)\)
\(m_{muối}=m_{KL}+m_{Cl^-}=28,6+2.35,5=99,6\left(g\right)\)
\(V_{HCl}=\dfrac{2}{1}=2\left(l\right)\)
Đốt cháy hết 2,86 gam hỗn hợp kim loại gồm Al, Fe, Cu được 4,14 gam hỗn hợp 3 oxit. Để hoà tan hết hỗn hợp oxit này, phải dùng đúng 0,4 lít dung dịch HCl và thu được dung dịch X. Cô cạn dung dich X thì khối lượng muối khan là bao nhêu ?
A. 9,45g
B. 7,49g
C. 8,54 g
D. 6,45 g
Theo định luật bảo toàn khối lượng, ta có:
m o x i t = m K L + m O / o x i t
⇔ m O / o x i t = m o x i t - m K L
=44-2,86 = 1,28g
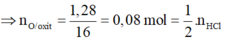
⇒ = n H C l = 0,08.2 = 0,16 mol
Áp dụng định luật bảo toàn khối lượng, ta có khối lượng của muối khan thu được là:
m m u o i = m K L + m C l
= 2,86 + 0,16.35,5 = 8,54g
⇒ Chọn C.
Hỗn hợp rắn A gồm Mg, Al và Cu. Đốt cháy m gam rắn A cần dùng 2,24 lít (đktc) hỗn hợp gồm O 2 và O 3 có tỉ khối so với He bằng 9,6 thu được hỗn hợp rắn B gồm các oxit. Hòa tan hoàn toàn B cần dùng 200 ml dung dịch HCl 0,6M và H 2 SO 4 xM. Cô cạn dung dịch sau phản ứng thu được (3m+5,94) gam muối khan. Giá trị của m là
A. 6,4 gam
B. 7,8 gam
C. 8,6 gam
D. 12,4 gam
Hòa tan hết m gam hỗn hợp gồm Mg, Al và Zn trong dung dịch H N O 3 loãng (dùng dư), kết thúc phản ứng thu được dung dịch X có khối lượng tăng m gam. Cô cạn cẩn thận dung dịch X thu được a gam hỗn hợp Y chứa các muối khan, trong đó phần trăm khối lượng của oxi chiếm 60,111% Nung nóng toàn bộ Y đến khối lượng không đổi thu được 18,6 gam hỗn hợp các oxit. Giá trị của a là
A. 70,12
B. 64,68
C. 68,46
D. 72,10
Đáp án B
m k l d d tan g = m ( g ) = m h h b a n d a u ⇒ không có sản phẩm khử khí.
![]()
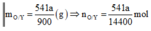
![]()
⇒ ∑ n N O 3 = 9 n N H 4 N O 3 = n O / 3
![]()
![]()
![]()
![]()
![]()
![]()
Tăng giảm khối lượng
![]()
⇒ a = 64 , 68 ( g )
Hòa tan hết m gam hỗn hợp gồm Mg, Al và Zn trong dung dịch H N O 3 loãng (dùng dư), kết thúc phản ứng thu được dung dịch X có khối lượng tăng m gam. Cô cạn cẩn thận dung dịch X thu được a gam hỗn hợp Y chứa các muối khan, trong đó phần trăm khối lượng của oxi chiếm 60,111% Nung nóng toàn bộ Y đến khối lượng không đổi thu được 18,6 gam hỗn hợp các oxit. Giá trị của a là
A. 70,12
B. 64,68
C. 68,46
D. 72,10
Hòa tan hết m gam hỗn hợp gồm Mg, Al và Zn trong dung dịch HNO3 loãng (dùng dư), kết thúc phản ứng thu được dung dịch X có khối lượng tăng m gam. Cô cạn cẩn thận dung dịch X thu được a gam hỗn hợp Y chứa các muối khan, trong đó phần trăm khối lượng của oxi chiếm 60,111%. Nung nóng toàn bộ Y đến khối lượng không đổi thu được 18,6 gam hỗn hợp các oxit. Giá trị của a là
A. 70,12
B. 64,68
C. 68,46
D. 72,10
Chọn B.
Nhận xét: Hòa tan hết m gam…,kết thúc thu được…tăng cũng m gam nên phản ứng giữa các kim loại với HNO3 chỉ thu được sản phẩm khử duy nhất là muối NH4NO3 (không có khí thoát ra)
Sơ đồ phản ứng:
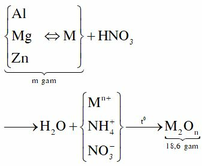
Ta có: Tổng số mol electron cho
của kim loại = tổng số mol điện tích
của các kim loại (M → Mn+ + ne)
Nên gọi số mol NH4NO3 là x mol thì

Vậy m = 12,84gam và a = 18,6 + 512x = 64,68gam
Hòa tan hết m gam hỗn hợp gồm Mg, Al và Zn trong dung dịch HNO3 loãng (dùng dư), kết thúc phản ứng thu được dung dịch X có khối lượng tăng m gam. Cô cạn cẩn thận dung dịch X thu được a gam hỗn hợp Y chứa các muối khan, trong đó phần trăm khối lượng của oxi chiếm 60,111%. Nung nóng toàn bộ Y đến khối lượng không đổi thu được 18,6 gam hỗn hợp các oxit. Giá trị của a là
A. 70,12
B. 64,68
C. 68,46
D. 72,10