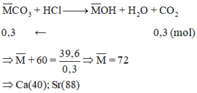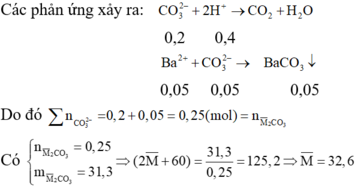Cho 7,2 gam hỗn hợp A gồm hai muối cacbonat của hai kim loại kế tiếp nhau trong nhóm IIA tác dụng với dung dịch HCl dư. Hấp thụ khí CO2 vào 450ml dung dịch Ba(OH)2 0,2M thu được 15,76 gam kết tủa. Xác định công thức 2 muối
A. BeCO3 và MgCO3
B. MgCO3 và CaCO3
C. CaCO3 và SrCO3
D.Đáp án khác