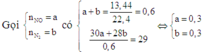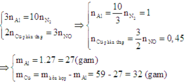Hỗn hợp X gồm Na, Al và Fe, hỗn hợp Y gồm Al và kim loại R. Biết rằng, khối lượng của Al có trong X và Y bằng nhau, tổng khối lượng của Na và Fe có trong X gấp 2 lần khối lượng của R có trong Y. Hòa tan hoàn toàn lần lượt X, Y băng lượng dư dung dịch H2SO4 loãng thì cả 2 trường hợp đều thu được V lít khí H2 (đktc). Kim loại R là
A. Ca.
B. Be.
C. Zn.
D. Mg.