Ngâm một thanh sắt vào 100 ml dung dịch AgNO3 1M, sau khi phản ứng kết thúc, lấy thanh sắt ra khỏi dung dịch, rửa sạch, sấy khô thấy khối lượng thanh sắt tăng thêm m gam. Giá trị của m là
A. 8
B. 5,2
C. 10,8
D. 13,6
Ngâm một thanh sắt vào 100 ml dung dịch AgNO3 1M, sau khi phản ứng kết thúc, lấy thanh sắt ra khỏi dung dịch, rửa sạch, sấy khô thấy khối lượng thanh sắt tăng thêm m gam. Giá trị của m là
A. 8
B. 5,2
C. 10,8
D. 13,6
Ngâm một đinh sắt trong 200 ml dung dịch C u S O 4 x M. Sau khi phản ứng kết thúc lấy đinh sắt ra khỏi dung dịch rửa nhẹ, làm khô thấy khối lượng đinh sắt tăng thêm 1,6gam. Giá trị của x là
A. 0,5 M
B. 0,75 M
C. 1 M
D. 1,5 M
n C U S O 4 = x.0,2 mol
F e + C u S O 4 → F e S O 4 + C u
x.0,2 x.0,2 x.0,2 (mol)
Khi nhúng thanh Fe vào dung dịch C u S O 4 , thanh Fe lúc sau có khối lượng tăng lên 1,6 gam là:
m C u b a m v a o - m F e tan = 1,6 g
⇔ 0,2x.64 - 0,2x.56 = 1,6
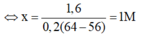
⇒ Chọn C.
Ngâm một đinh sắt sạch trong 200ml dung dịch C u S O 4 . Sau khi phản ứng kết thúc, lấy đinh sắt ra khỏi dung dịch rửa sạch nhẹ bằng nước cất và sấy khô rồi đem cân thấy khối lượng đinh sắt tăng 0,8 gam so với ban đầu. Nồng độ mol của dung dịch C u S O 4 đã dùng là giá trị nào dưới đây?
A. 0,05M
B. 0,0625M
C. 0,50M
D. 0,625M.
Gọi a là số mol C u S O 4 tham gia phản ứng
Phương trình hóa học:
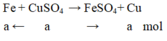
Theo đề bài ta có: m C u b á m v à o – m F e tan r a = m K L t ă n g
64a – 56a = 0,8 ⇒ a = 0,01 mol
Nồng độ dung dịch C u S O 4 là: C M = n V = 0,01 0,2 = 0,5 M
⇒ Chọn C.
Ngâm một đinh sắt sạch trong 200 ml dung dịch C u S O 4 sau khi phản ứng kết thúc, lấy đinh sắt ra khỏi dung dịch rửa nhẹ làm khô nhận thấy khối lượng đinh sắt tăng thêm 0,8 gam. Nồng độ mol/lít của dung dịch C u S O 4 đã dùng là:
A. 0,3M.
B. 0,5M.
C. 0,4M.
D. 0,25M.
Ngâm một đinh sắt sạch trong 200 ml dung dịch CuS O 4 sau khi phản ứng kết thúc, lấy đinh sắt ra khỏi dung dịch rửa nhẹ làm khô nhận thấy khối lượng đinh sắt tăng thêm 0,8 gam. Nồng độ mol/lít của dung dịch CuS O 4 đã dùng là:
A. 0,3M
B. 0,5M
C. 0,4M
D. 0,25M
Ngâm một thanh Kẽm trong 100 ml dung dịch F e N O 3 2 xM. Sau khi phản ứng kết thúc lấy thanh kẽm ra khỏi dung dịch rửa nhẹ, làm khô thấy khối lượng thanh kẽm giảm 1,35 gam. Giá trị của x là
A. 1
B. 1,5
C. 0,15
D. 0,2
Ngâm một đinh sắt trong 200 ml dung dịch CuSO4 x(M). Sau khi phản ứng kết thúc lấy đinh sắt ra khỏi dung dịch rửa nhẹ, làm khô đinh sắt tăng thêm 3,2 gam. Giá trị của X là
A. 0,40.
B. 0,8.
C. 2,0.
D. 0,2.
Ngâm một đinh sắt trong 200 ml dung dịch CuSO4 x(M). Sau khi phản ứng kết thúc lấy đinh sắt ra khỏi dung dịch rửa nhẹ, làm khô đinh sắt tăng thêm 3,2 gam. Giá trị của X là
A. 0,40
B. 0,8
C. 2,0
D. 0,2
Đáp án C
Phản ứng: Fe + CuSO4 → FeSO4 + Cu.
Nhận xét: cứ 1 mol CuSO4 phản ứng thì làm mất 1 mol Fe và tạo thêm 1 mol Cu
→ Khối lượng thanh sắt tăng thêm tương ứng 64 – 56 = 8 gam.
Theo đó, để thanh sắt tăng thêm 3,2 gam thì tương ứng số mol CuSO4 phản ứng là 3,2 : 8 = 0,4 mol.
Vậy, giá trị của x = 0,4 ; 0,2 = 2,0
Bài 3: Ngâm một đinh sắt sạch trong 200ml dung dịch CuSO4. Sau khi phản ứng kết thúc, lấy đinh sắt ra khỏi dung dịch rửa sạch nhẹ bằng nước cất và sấy khô rồi đem cân thấy khối lượng đinh sắt tăng 0,8 gam so với ban đầu. Nồng độ mol của dung dịch CuSO4 đã dùng là giá trị nào dưới đây?
Fe + CuSO4 → FeSO4 + Cu
1mol 1 mol => tăng 8 gam
x mol x mol tăng 0,8gam
=> x= 0,8:8= 0,1 mol
=> CM ( dung dịch CuSO4) = 0,1:0,2= 0,5 M
Bài 3 :
Pt : \(Fe+CuSO_4\rightarrow FeSO_4+Cu|\)
1 1 1 1
x 0,1 x
Gọi x là số mol của Fe
Vì khối lượng của sắt tăng so với ban đầu nên ta có phương trình :
\(m_{Cu}-m_{Fe}=0,8\left(g\right)\)
64x - 56x = 0,8
8x = 0,8
⇒x = \(\dfrac{0,8}{8}=0,1\)
\(n_{CuSO4}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
200ml = 0,2l
\(C_{M_{ddCuSO4}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
Chúc bạn học tốt