Nhiệt phân hoàn toàn 36 gam Fe(NO3)2 (chân không), khối lượng chất rắn thu được sau phản ứng là:
A. 14,4 g
B. 16 g
C. 15,4667 g
D. Đ/a khác
Nhiệt phân hoàn toàn 17,4 gam hỗn hợp chứa Fe(NO3)2 và AgNO3 trong không khí thu được 4,032 lít hỗn hợp khí ( đktc ). Tính khối lượng chất rắn sau phản ứng
Nhiệt phân hoàn toàn 48,25 gam hỗn hợp KClO3 và Fe(NO3)2 (trong chân không) thì thu được hỗn hợp chất rắn A và 0,6 mol hỗn hợp khí. Khối lượng mỗi chất rắn trong hỗn hợp A là:
A. 7,45 gam KCl và 16 gam Fe2O3
B. 3,725 gam KCl, 6,92 gam KClO4 và 16 gam Fe2O3
C. 3,725 gam KCl, 6,92 gam KClO4 và 16 gam FeO
D. 7,45 gam KCl và 16 gam FeO.
Đáp án A
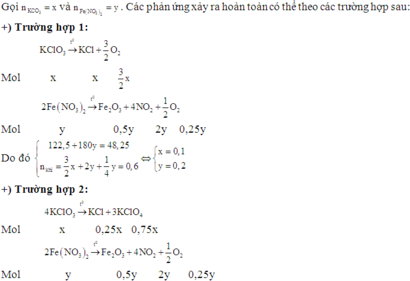
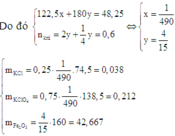
Nhận xét: Với bài tập trắc nghiệm, các bạn có thể quan sát các đáp án và tìm nhanh đáp án như sau: Khi viết phản ứng nhiệt phân Fe(NO3)2 ta thấy chắc chắn hỗn hợp rắn thu được phải chứa Fe2O3.
Khi đó đáp án đúng là A hoặc B

Mà ![]() nên đáp án B không đúng.
nên đáp án B không đúng.
Vậy đáp án đúng là A.
Chú ý: Khi nhiệt phân muối KClO3, phản ứng có thể xảy ra theo 2 hướng:
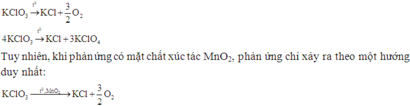
Cho 2,24 g Fe vào 200 ml dung dịch Cu(NO3)2 0,1M và AgNO3 0,1M. Khuấy đều cho đến phản ứng hoàn toàn. Khối lượng (gam) chất rắn thu được là:
A. 4,0
B. 1,232
C. 8,040
D. 12,320
Cho 4,58 gam hỗn hợp A gồm Zn, Fe và Cu vào cốc đựng 85 ml dung dịch C u S O 4 1M. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch B và kết tủa C. Nung C trong không khí đến khối lượng không đổi được 6 gam chất rắn D. Thêm dung dịch NaOH dư vào dung dịch B, lọc kết tủa thu được, rửa sạch rồi nung ở nhiệt độ cao đến khối lượng không đổi thu được 5,2 gam chất rắn E. Các phản ứng xảy ra hoàn toàn. % khối lượng mỗi kim loại trong hỗn hợp A (theo thứ tự Zn, Fe, Cu) là
A. 28,38%; 36,68% và 34,94%
B. 14,19%; 24,45% và 61,36%
C. 28,38%; 24,45% và 47,17%
D. 42,58%; 36,68% và 20,74%
Nhiệt phân hỗn hợp X gồm Cu(NO3)2 và AgNO3 thu được m gam hỗn hợp khí A và ( m + 15,04) gam chất rắn B. Hấp thụ toàn bộ hỗn hợp khí A vào bình chứa nước đến khi phản ứng xảy ra hoàn toàn thu được 600 ml dung dịch D có pH = 1 và có 0,112 lít (đktc) một khí duy nhất thoát ra khỏi bình. Mặt khác cũng lượng hỗn hợp X ở trên được hòa tan hết vào nước thu được dung dịch Y, nhúng một thanh Fe vào dung dịch Y đến khi phản ứng xảy ra hoàn toàn rút thanh Fe ra cân lại thấy khối lượng thanh Fe tăng thêm 3,84 gam so với ban đầu. Hiệu suất phản ứng nhiệt phân Cu(NO3)2 và AgNO3 theo thứ tự là
A. 25% và 50%.
B. 50% và 25%.
C. 40% và 60%.
D. 60% và 40%.
Cho 4,58 gam hỗn hợp A gồm Zn, Fe và Cu vào cốc đựng 85ml dung dịch CuSO4 1M. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch B và kết tủa C. Nung C trong không khí đến khối lượng không đổi được 6 gam chất rắn D. Thêm dung dịch NaOH dư vào dung dịch B, lọc kết tủa thu được, rửa sạch rồi nung ở nhiệt độ cao ngoài không khí đến khối lượng không đổi thu được 5,2 gam chất rắn E. Các phản ứng xảy ra hoàn toàn. % khối lượng mỗi kim loại trong hỗn hợp A (theo thứ tự Zn, Fe, Cu) là:
A. 28,38%; 36,68% và 34,94%
B. 14,19%; 24,45% và 61,36%
C. 28,38%; 24,45% và 47,17%
D. 42,58%; 36,68% và 20,74%
Đáp án A
Các phản ứng có thể xảy ra:
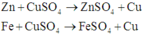
Trong 3 kim loại Zn, Fe và Cu thì Fe có khối lượng mol nhỏ nhất
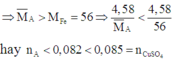
Do đó B chứa Cu2+ dư
Khi đó C chứa Cu trong A và Cu sinh ra sau phản ứng. Nên D chứa CuO.
B chứa Zn2+, Fe2+ và Cu2+ dư. Khi cho B tác dụng với dung dịch NaOH dư thì kết tủa thu được chứa Fe(OH)2 và Cu(OH)2 .
Do đó E chứa Fe2O3 và CuO.
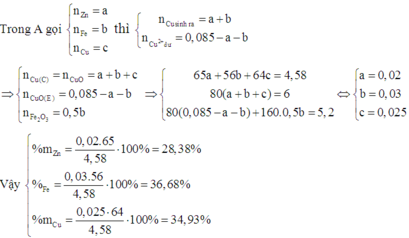
nhiệt phân hoàn toàn hỗn hợp y gồm cu(no3)2 và Mg(NO3)2 trong bình kín không chứa không khí, dến khối lượng không đổi thì sau phản ứng thu được hỗn hợp khí , khối lượng chất rắn giảm là 3,24g. Hấp thụ hoàn toàn X vào nước để được 600ml dd A. DD A có pH bằng A. 2 B. 3 C. 1 D. 4
giúp em nhanh ạ
Nhiệt phân hoàn toàn 15,8 g KMnO4 thu được v lít khí Oxi a Tính v b đốt cháy 5,6 gam sắt trong V lít khí Oxi nói trên sản phẩm thu được là oxit sắt từ fe3 o4 tính khối lượng chất rắn thu được sau phản ứng
PTHH: \(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\)
\(n_{KMnO_4}=\dfrac{m_{KMnO_4}}{M_{KMnO_4}}=\dfrac{15,8}{158}=0,1\left(mol\right)\)
a. Theo PTHH: \(n_{O_2}=\dfrac{1}{2}n_{KMnO_4}=\dfrac{1}{2}0,1=0,05\left(mol\right)\)
\(\Rightarrow V_{O_2}=n_{O_2}.22,4=0,05.22,4=1,12\left(l\right)\)
b. PTHH: \(3Fe+2O_2\xrightarrow[]{t^o}Fe_3O_4\)
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Ta có: \(\dfrac{1}{n_{O_2}}=\dfrac{1}{0,05}\)
\(\dfrac{1}{n_{Fe}}=\dfrac{1}{0,1}\)
\(\Rightarrow\dfrac{1}{n_{O_2}}>\dfrac{1}{n_{Fe}}\)
Vậy Fe dư
Theo PTHH: \(n_{Fe_3O_4}=\dfrac{0,1.1}{3}=\dfrac{1}{30}\left(mol\right)\)
\(\Rightarrow m_{Fe_3O_4}=n_{Fe_3O_4}.M_{Fe_3O_4}=\dfrac{1}{30}.232\approx7,73g\)
Tiến hành nhiệt phân hỗn hợp chứa BaCO3, Fe(NO3)2, Mg(NO3)2 trong chân không đến khối lượng không đổi, thu được rắn X. Hòa tan X vào lượng nước dư, thu được hỗn hợp chất rắn Y. Dẫn luồng khí H2 dư qua ống sứ chứa Y (nung nóng), thu được hỗn hợp rắn Z. Biết các phản ứng xảy ta hoàn toàn. Trong Z chứa
A. 1 đơn chất và 1 hợp chất
B. 2 hợp chất
C. 1 đơn chất và 2 hợp chất
D. 2 đơn chất