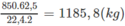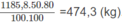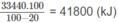Một loại khí thiên nhiên có thành phần trăm về thể tích các khí như sau: 85,0% metan; 10,0% etan; 2,0% nitơ và 3,0% cacbon đioxit.
Nếu chuyển được toàn bộ hiđrocacbon trong 1,000.103 m3 khí trên (đktc) thành axetilen, sau đó thành vinyl clorua với hiệu suất toàn bộ quá trình bằng 65,0% thì sẽ thu được bao nhiêu kilogam vinyl clorua?