Để khử hoàn toàn 16,0 gam Fe2O3 bằng khí CO (ở nhiệt độ cao), phản ứng tạo Fe và khí CO2. Thể tích khí CO (đktc) cần dùng là
A. 6,72
B. 2,24
C. 4,48
D. 3,36
Một hỗn hợp rắn chứa 0,1 mol CuO và 0,1 mol Fe2O3. Người ta dùng khí CO để khử hoàn toàn hỗn hợp trên ở nhiệt độ phù hợp. Thể tích khí CO (đktc) cần cho thí nghiệm trên là
A. 4,48 lít.
B. 6,72 lít.
C. 8,24 lít.
D. 8,96 lít.
PTHH: CuO + CO --to--> Cu + CO2
______0,1---------------------->0,1
Fe2O3 + 3CO --> 2Fe + 3CO2
_0,1----------------------->0,3
=> VCO2 = (0,1+0,3).22,4 = 8,96(l)
=> D
Cho khí CO khử hoàn toàn hỗn hợp X gồm Fe, Fe2O3, Fe3O4 thấy có 4,48 lít CO2 (đktc). Thể tích khí CO (đktc) đã tham gia phản ứng là:
A. 1,12 lít
B. 2,24 lít
C. 3,36 lít
D. 4,48 lít.
Khử hoàn toàn 8,0 gam bột Fe2O3 thành Fe ở nhiệt độ cao thì thể tích khí CO tối thiểu (đktc) cần là
A. 1,12 lít
B. 3,36 lít
C. 6,72 lít
D. 2,24 lít
Khử hoàn toàn 8,0 gam bột Fe2O3 thành Fe ở nhiệt độ cao thì thể tích khí CO tối thiểu (đktc) cần là:
A. 1,12 lít.
B. 3,36 lít
C. 6,72 lít.
D. 2,24 lít.
Cho V lít khí CO phản ứng vs fe2o3 ở nhiệt độ cao tạo thành phe và co2. Nếu cho lượng fe sau phản ứng tan hết trong h2so4 loãng đc 20,16 lít khí hidro đktc.
a) tính V CO đã pư đkt.
b) nếu hòa tan hết c rắn sau pư khử bđ phải dùng hết 94,9 g HCl thì khối lượng fe2o3 đã dùng nđ là bn?
c) nếu sau pư bđ vs cùg kl fe2o3 ns trên toàn bộ khí sau pư khử td vừa đủ vs 3,36 l oxi đktc thì V CO đã dùng nđ ở đkt bn lít?
Khử hết 16 gam hỗn hợp gồm FeO, Fe2O3, Fe3O4 bằng CO ở nhiệt độ cao, sau phản ứng thu được 11,2 gam Fe. Thể tích khí CO(đktc) đa tham gia phản ứng là
A. 2,24 lít
B. 3,36 lít
C. 6,72 lít
D. 8,96 lít
Đáp án C
Qui hỗn hợp về dạng: Fe, O. Phản ứng của oxit + CO thực chất là:
CO + [O] → CO2
Bảo toàn nguyên tố: mFe(oxit) = mFe sau pứ = 11,2g
=> mO(oxit) = mOxit – mFe = 16 – 11,2 = 4,8g => nO = 4,8 : 16 = 0,3 mol
=> nCO = nO = 0,3 mol
=> VCO = 0,3.22,4 = 6,72 lit
: Khử hoàn toàn 12,8 gam Fe2O3 bằng khí hiđro ở nhiệt độ cao.
a. Tính thể tích hiđro cần dùng ở đktc?
b. Tính khối lượng Fe thu được sau phản ứng?
c. Nếu đem toàn bộ lượng Fe thu được ở trên tác dụng với 14,6 gam axit HCl thì thu được bao nhiêu lít H2 (đktc)?
Để giải bài toán này, ta cần biết phương trình phản ứng giữa oxit sắt (Fe2O3) và khí hidro (H2):
Fe2O3 + 3H2 → 2Fe + 3H2O
Theo đó, mỗi mol Fe2O3 cần 3 mol H2 để khử hoàn toàn thành Fe.
a) Thể tích khí hiđro cần dùng:
Ta cần tìm số mol khí hidro cần dùng để khử hoàn toàn 12,8 gam Fe2O3.Khối lượng mol của Fe2O3 là:M(Fe2O3) = 2x56 + 3x16 = 160 (g/mol)
Số mol Fe2O3 là:n(Fe2O3) = m/M = 12.8/160 = 0.08 (mol)
Theo phương trình phản ứng, mỗi mol Fe2O3 cần 3 mol H2 để khử hoàn toàn thành Fe.Vậy số mol H2 cần dùng là:n(H2) = 3*n(Fe2O3) = 0.24 (mol)
Thể tích khí hidro cần dùng ở đktc là:V(H2) = n(H2)22.4 = 0.2422.4 = 5.376 (lít)
Vậy thể tích khí hiđro cần dùng ở đktc là 5.376 lít.
b) Khối lượng Fe thu được sau phản ứng:
Theo phương trình phản ứng, mỗi mol Fe2O3 tạo ra 2 mol Fe.Vậy số mol Fe thu được là:n(Fe) = 2*n(Fe2O3) = 0.16 (mol)
Khối lượng Fe thu được là:m(Fe) = n(Fe)M(Fe) = 0.1656 = 8.96 (gam)
Vậy khối lượng Fe thu được sau phản ứng là 8.96 gam.
c) Thể tích khí hiđro thu được khi Fe tác dụng với HCl:
Ta cần tìm số mol H2 thu được khi Fe tác dụng với HCl.Theo phương trình phản ứng, mỗi mol Fe tác dụng với 2 mol HCl để tạo ra H2 và muối sắt (FeCl2).Số mol HCl cần dùng để tác dụng với Fe là:n(HCl) = m(HCl)/M(HCl) = 14.6/36.5 = 0.4 (mol)
Vậy số mol H2 thu được là:n(H2) = 2n(Fe) = 2(m(Fe)/M(Fe)) = 2*(8.96/56) = 0.16 (mol)
Thể tích khí hiđro thu được ở đktc là:V(H2) = n(H2)22.4 = 0.1622.4 = 3.584 (lít)
Vậy thể tích khí hiđro thu được ở đktc là 3.584 lít.

Khử hoàn toàn một oxit sắt ở nhiệt độ cao cần vừa đủ V lít khí CO dư (đktc), sau phản ứng thu được 0,84 gam Fe và 0,02 mol khí CO2. Công thức của X và giá trị V lần lượt là
A. Fe3O4 và 0,224
B. FeO và 0,224
C. Fe2O3 và 0,448
D. Fe3O4 và 0,448
Đáp án : D
FexOy + yCO -> xFe + yCO2
=> nFe : nCO2 = 0,015 : 0,02 = x : y
=> x : y = 3 : 4
Oxit sắt là : Fe3O4
nCO = nCO2 = 0,02 mol => V = 0,448 lit
Khử hoàn toàn một oxit sắt X ở nhiệt độ cao cần vừa đủ V lít khí CO (ở đktc), sau phản ứng thu được 0,84 gam Fe và 0,02 mol khí CO2. Oxit sắt X và giá trị của V lần lượt là:
A. Fe3O4 và 0,224
B. Fe3O4 và 0,448
C. FeO và 0,224
D. Fe2O3 và 0,448
Đáp án B
Đặt công thức oxit sắt là FexOy
FexOy+ yCO → xFe + yCO2
nFe= 0,84/56= 0,015 mol
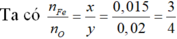
→Công thức oxit là Fe3O4
Ta có: nCO= nCO2= 0,02 mol
→ V= 0,02.22,4= 0,448 lít