a. Tính số phân tử chứa trong 0,2kg nước.
b. Tính số phân tử chứa trong 1 kg không khí nếu như không khí có 22% là oxi và 78% là khí nitơ.
a. Tính số phân tử chứa trong 0,2kg nước.
b. Tính số phân tử chứa trong 1 kg không khí nếu như không khí có 22% là oxi và 78% là khí nitơ.
a. 1 mol chất có chưa NA phân tử, n mol chất có N phân tử
Do đó: N = n . N A = m μ H 2 O . N A = 200 18 .6 , 02.10 23 ≈ 6 , 68.10 24 phân tử
b. Số phân tử chứa trong 1kg không khí
N = 22 % . m μ O 2 N A + 78 % m μ N 2 N A = m . N A . [ 22 % 32 + 78 % 28 ] ≈ 2 , 1.10 25 phân tử
Tính số phân tử chứa trong 1 kg không khí nếu như không khí có 22% là oxi và 78% là khínitơ
Tính số phân tử chứa trong không khí nếu coi không khí có là oxi và 78% là khí nito.
Khối lượng ôxi trong 1,2kg không khí:
m O 2 = 1200.22 100 = 264 g a m .
Khối lượng nitơ trong 1,2kg không khí:
m N 2 = 1200.78 100 = 936 g a m .
Số phân tử ôxi:
N = 264 32 .6 , 02.10 23 = 49 , 66.10 23 phân tử.
Số phân tử nitơ:
N ' = 936 28 .6 , 02.10 23 = 201 , 24.10 23 phân tử.
Suy ra số phân tử trong 1,2kg không khí:
N 0 = N + N ' = 250 , 9.10 25 phân tử.
Cho các phát biểu sau:
(1) Nitơ thuộc nhóm VA, chu kì 2
(2) Trong phân tử nitơ có chứa một kiên kết ba
(3) Trong điều kiện thường, nitơ là chất lỏng, không màu, mùi xốc, nhẹ hơn không khí
(4) Nitơ không duy trì sự cháy và nitơ tan nhiều trong nước
(5) Ở nhiệt độ thường, nitơ hoạt động hóa học mạnh và có thể tác dụng với nhiều chất
(6) Nitơ vừa có tính oxi hóa vừa có tính khử
Số phát biểu đúng là
A. 2
B. 3
C. 5
D. 4
Đáp án B
Các trường hợp thỏa mãn: 1-2-6
Cho các phát biểu sau:
(1) Nitơ thuộc nhóm VA, chu kì 2
(2) Trong phân tử nitơ có chứa một kiên kết ba
(3) Trong điều kiện thường, nitơ là chất lỏng, không màu, mùi xốc, nhẹ hơn không khí
(4) Nitơ không duy trì sự cháy và nitơ tan nhiều trong nước
(5) Ở nhiệt độ thường, nitơ hoạt động hóa học mạnh và có thể tác dụng với nhiều chất
(6) Nitơ vừa có tính oxi hóa vừa có tính khử
Số phát biểu đúng là
A. 2
B. 3
C. 5
D. 4
Đáp án B
Các trường hợp thỏa mãn: 1-2-6
Khí Z là hợp chất của khí nitơ và oxi, có tỉ khối so với khí H2 bằng 22
a) Tính khối lượng mol phân tử của khí Z
b) Lập công thức phân tử của khí Z
c) Tính tỉ khối của khí Z so với không khí (Mk = 22)
a) Khối lượng mol phân tử khí Z = 2 . 22 = 44 g/mol
b) Gọi công thức chung của hc là NxOy . Ta có :
14x + 16y = 44
=> x = 2 , y = 1
CTHC là : N2O
c) Tỉ khối của Z với kk là
\(\frac{d_Z}{d_{kk}}=\frac{44}{29}\)
a.MZ=\(M_{H_2}.22=2.22=44\)(g/mol)
b.Gọi CTHH của khí Z là NxOy
Ta có MN.x+MO.y=44=>x=2;y=1
Vậy CTHH của khí Z là N2O
c.Mkk là 29 nha bạn
\(d_{Z/kk}=\dfrac{M_Z}{M_{kk}}=\dfrac{44}{29}\approx1,52\)
Chúc bạn học tốt![]()
Đốt cháy hoàn toàn một amin no, mạch hở (X) bằng lượng không khí vừa đủ, thu được 10,56 gam CO2; 5,76 gam nước và 36,736 lít khí N2 (đktc). Biết rằng không khí chỉ gồm nitơ và oxi, trong đó oxi chiếm 20% thể tích không khí. Tổng số nguyên tử trong 1 phân tử X là:
A. 20
B. 24
C. 22
D. 12
Chọn đáp án B.
n C O 2 = 10 , 56 44 = 0 , 24 mol,
n H 2 O = 5 , 76 18 = 0 , 32 mol, n N 2 = 36 , 736 22 , 4 = 1 , 64 mol
⇒ n C : n H = 0 , 24 : 0 , 64 = 3 : 8
· Đặt CTTQ của X là C3xH8xNy
Amin no nên
k = 2 . 3 x + 2 + y - 8 x 2 = 0
⇒ 2 x - y = 2
Mà y ≤ x nên x ≤ 2 ⇒ x = 2 ; y = 2
=> CTPT của X là C6H16N2
=> Tổng số nguyên tử trong 1 phân tử X là 24
Đốt cháy hoàn toàn một amin no, mạch hở (X) bằng lượng không khí vừa đủ, thu được 10,56 gam CO2; 5,76 gam nước và 36,736 lít khí N2 (đktc). Biết rằng không khí chỉ gồm nitơ và oxi, trong đó oxi chiếm 20% thể tích không khí. Tổng số nguyên tử trong 1 phân tử X là:
A. 20.
B. 24.
C. 22.
D. 12.
Chọn đáp án B.
![]() mol,
mol,
![]() mol,
mol,
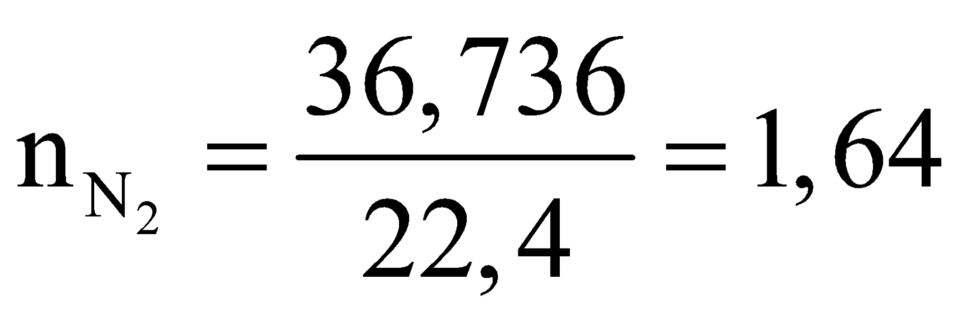 mol
mol
![]()
∙ Đặt CTTQ của X là C3xH8xNy
Amin no nên
![]()
Mà ![]() nên
nên ![]()
=> CTPT của X là C6H16N2
=> Tổng số nguyên tử trong 1 phân tử X là 24.
khí Z là tập hợp của khí nitơ và oxi,có tỉ khối với H2 bằng 22
a. tính khối lượng mol phân tử của khí Z
b. Lập công thức phân tử của khí Z
c.Tính tỉ khối của Z so với không khí (Mkk= 29 gam/mol)
a/ => MZ= 2 x 22 = 44( g/mol)
b/ Gọi CTPT của Z là NxOy
Ta có 14x + 16y = 44
=> Ta thấy x = 2 và y = 1 là phù hợp
=> CTPT N2O
c/dZ/kk= MZ / 29 = 44 / 29 = 1,52