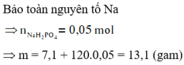Đốt cháy a gam photpho đỏ trong không khí lấy dư, rồi cho sản phẩm thu được vào 500,0 ml dung dịch H 3 P O 4 85,00% (D = 1,7 g/ml). Sau khi phản ứng xảy ra hoàn toàn nồng độ của dung dịch H 3 P O 4 xác định được là 92,60%. Tính giá trị của a.

Những câu hỏi liên quan
Đốt cháy hoàn toàn m gam photpho trong không khí (dư) rồi hòa tan toàn bộ sản phẩm thu được vào 500 ml dung dịch H3PO4 85% (D1,7g/ml) thì nồng độ H3PO4 trong dung dịch tăng thêm 4,1%. Giá trị của m là A. 18,6. B. 24,8. C. 31,0. D. 37,2.
Đọc tiếp
Đốt cháy hoàn toàn m gam photpho trong không khí (dư) rồi hòa tan toàn bộ sản phẩm thu được vào 500 ml dung dịch H3PO4 85% (D=1,7g/ml) thì nồng độ H3PO4 trong dung dịch tăng thêm 4,1%. Giá trị của m là
A. 18,6.
B. 24,8.
C. 31,0.
D. 37,2.
Đốt cháy m gam photpho trong không khí dư, cho toàn bộ sản phẩm cháy vào 500 ml dung dịch H3PO4 85% (D = 1,7g/ml) thì nông độ của axit trong dung dịch tăng thêm 7,6%. Tính khối lượng photpho đã đốt cháy?
\(4P+ 5O_2 \xrightarrow{t^o} 2P_2O_5\\ P_2O_5 + 3H_2O \to 2H_3PO_4\)
\(n_{P_2O_5} = 0,5n_P = 0,5a(mol)\)
\(n_{H_3PO_4} = n_P = a(mol)\)
\(m_{dung\ dịch} = 500.1,7 = 850(gam)\\ m_{H_3PO_4} = 500.1,7.85\% = 722,5(gam)\\\)
Sau khi thêm sản phẩm cháy vào :
\(m_{H_3PO_4} = 722,5 + 98a(gam)\\ m_{dung\ dịch} = m_{dd\ trước} + m_{P_2O_5} = 850 + 71a(gam)\)
Suy ra :
\(C\%_{H_3PO_4} = \dfrac{722,5+98a}{850+71a}.100\% = 85\% + 7,6\%\\ \Rightarrow a = 2\)
Suy ra: m = 2.31 = 62(gam)
Đúng 0
Bình luận (1)
Đốt cháy 4,65 gam photpho ngoài không khí rồi hoà tan sản phẩm vào 500 ml dung dịch NaOH 1,2 M. Tổng khối lượng chất tan trong dung dịch sau phản ứng là
A. 24,6 gam
B. 26,2 gam
C. 26,4 gam
D. 30,6 gam
Đáp án : D
2P -> P2O5
=> nP2O5 = 0,075 mol
,nNaOH = 0,6 mol >> nP2O5 => NaOH dư
6NaOH + P2O5 -> 2Na3PO4 + 3H2O
=> Sau phản ứng có : 0,15 mol Na3PO4 và 0,15 mol NaOH
=> mtan = 30,6g
Đúng 0
Bình luận (0)
Đốt cháy 4,65 gam photpho ngoài không khí rồi hoà tan sản phẩm vào 500 ml dung dịch NaOH 1,2 M. Tổng khối lượng chất tan trong dung dịch sau phản ứng là A. 24,6 gam B. 26,2 gam C. 26,4 gam D. 30,6 gam
Đọc tiếp
Đốt cháy 4,65 gam photpho ngoài không khí rồi hoà tan sản phẩm vào 500 ml dung dịch NaOH 1,2 M. Tổng khối lượng chất tan trong dung dịch sau phản ứng là
A. 24,6 gam
B. 26,2 gam
C. 26,4 gam
D. 30,6 gam
Đáp án D
2P -> P2O5
=> nP2O5 = 0,075 mol
nNaOH = 0,6 mol >> nP2O5 => NaOH dư
6NaOH + P2O5 -> 2Na3PO4 + 3H2O
=> Sau phản ứng có : 0,15 mol Na3PO4 và 0,15 mol NaOH
=> mtan = 30,6g
Đúng 0
Bình luận (0)
Đốt cháy 15,5 gam photpho trong oxi dư rồi hòa tan sản phẩm vào 200 gam nước. C% của dung dịch axit thu được là
A. 11,36%
B. 20,8%
C. 24,5%
D. 22,7%
Chọn đáp án B
Phản ứng đốt cháy trong Oxi dư: 4P + 5O2 → 2P2O5.
Sau đó hòa tan vào nước: P2O5 + 3H2O → 2H3PO4.
nP = 15,5 ÷ 31 = 0,5 mol ⇒ bảo toàn nguyên tố P có nH3PO4 = 0,5 mol;
và nP2O5 = 0,25 mol ⇒ mP2O5 = 0,25 × 142 = 35,5 gam.
||⇒ mdung dịch axit = 200 + 35,5 = 235,5 gam
⇒ C% = 0,5 × 98 ÷ 235,5 × 100% ≈ 20,8%. Chọn đáp án B
Đúng 0
Bình luận (0)
Đốt cháy 15,5 gam photpho trong oxi dư rồi hòa tan sản phẩm vào 200 gam nước. C% của dung dịch axit thu được là
A. 11,36%
B. 20,8%
C. 24,5%
D. 22,7%
Đốt cháy hoàn toàn 6,2 gam photpho trong khí O2 dư, toàn bộ sản phẩm sinh ra cho vào 500 ml dung dịch hỗn hợp NaOH 0,4M và KOH 0,6M, kết thúc phản ứng thu được dung dịch X. Biết các phản ứng xảy ra hoàn toàn. Tổng khối lượng muối có trong dung dịch X là A. 44,4g B. 39g C. 35,4g D. 37,2g
Đọc tiếp
Đốt cháy hoàn toàn 6,2 gam photpho trong khí O2 dư, toàn bộ sản phẩm sinh ra cho vào 500 ml dung dịch hỗn hợp NaOH 0,4M và KOH 0,6M, kết thúc phản ứng thu được dung dịch X. Biết các phản ứng xảy ra hoàn toàn. Tổng khối lượng muối có trong dung dịch X là
A. 44,4g
B. 39g
C. 35,4g
D. 37,2g
Đáp án C
2P -> P2O5 -> 2H3PO4
=> nH3PO4 = nP = 0,2 mol
,nOH = 0,5 mol => 2 < nOH : nH3PO4 = 2,5 < 3
Các phản ứng :
2MOH + H3PO4 -> M2HPO4 + 2H2O
3MOH + H3PO4 -> M3PO4 + 3H2O
=> Muối gồm : 0,1 mol M2HPO4 và 0,1 mol M3PO4
=> mmuối = mK + mNa + mHPO4 + mPO4 = 35,4g
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 6,2 gam photpho trong khí O2 dư, toàn bộ sản phẩm sinh ra cho vào 500 ml dung dịch hỗn hợp NaOH 0,4M và KOH 0,6M, kết thúc phản ứng thu được dung dịch X. Biết các phản ứng xảy ra hoàn toàn. Tổng khối lượng muối có trong dung dịch X là A. 44,4g B. 39g C. 35,4g D. 37,2g
Đọc tiếp
Đốt cháy hoàn toàn 6,2 gam photpho trong khí O2 dư, toàn bộ sản phẩm sinh ra cho vào 500 ml dung dịch hỗn hợp NaOH 0,4M và KOH 0,6M, kết thúc phản ứng thu được dung dịch X. Biết các phản ứng xảy ra hoàn toàn. Tổng khối lượng muối có trong dung dịch X là
A. 44,4g
B. 39g
C. 35,4g
D. 37,2g
Đáp án : C
2P -> P2O5 -> 2H3PO4
=> nH3PO4 = nP = 0,2 mol
,nOH = 0,5 mol => 2 < nOH : nH3PO4 = 2,5 < 3
Các phản ứng :
2MOH + H3PO4 -> M2HPO4 + 2H2O
3MOH + H3PO4 -> M3PO4 + 3H2O
=> Muối gồm : 0,1 mol M2HPO4 và 0,1 mol M3PO4
=> mmuối = mK + mNa + mHPO4 + mPO4 = 35,4g
Đúng 1
Bình luận (0)
Đốt cháy một lượng photpho (có khối lượng lớn hơn 2,48 gam) bằng oxi dư, lấy sản phẩm cho vào 75 gam dung dịch NaOH 8% rồi làm khô thu được m gam cặn khan X, trong đó có 7,1 gam
N
a
2
H
P
O
4
. Giá trị của m là A. 13,1. B. 12,6. C. 8414,2. D. 15,6.
Đọc tiếp
Đốt cháy một lượng photpho (có khối lượng lớn hơn 2,48 gam) bằng oxi dư, lấy sản phẩm cho vào 75 gam dung dịch NaOH 8% rồi làm khô thu được m gam cặn khan X, trong đó có 7,1 gam N a 2 H P O 4 . Giá trị của m là
A. 13,1.
B. 12,6.
C. 8414,2.
D. 15,6.