Cho hỗn hợp gồm 3 ankin đi qua bình đựng nước brom, thấy làm mất màu dung dịch chứa tối đa 16 gam brom. Tổng số mol của 3 ankin là:
A. 0,025
B. 0,05.
C. 0,075
D. 0,1.
Cho hỗn hợp gồm 3 anken đi qua bình đựng nước brom, thấy làm mất màu vừa đủ dung dịch chứa 16 gam brom. Tổng số mol của 3 anken là:
A. 0,025.
B. 0,05.
C. 0,075
D. 0,1.
- Số mol anken = số mol brom = 0,1 mol.
- Chọn đáp án D.
Dẫn 1,155 gam hỗn hợp khí gồm C2H2 và một ankin X thuộc dãy đồng đẳng của C2H2 với số mol bằng nhau đi qua dung dịch nước brom, lượng brom tham gia phản ứng là 11,2 gam. Công thức phân tử của ankin X là?
Giải thích các bước giải: Gọi CT của ankin X là CmH2m-2
nBr2n=0,07 ( mol)
CnH2n-2 + 2Br -> CnH2n-2Br2
0,035 <= 0,07 ( mol)
2 ankin có số mol bằng nhau, đều bằng : n=0,0175 mol
=> mhỗn.hợp =0,0175.26+ 0,0175.(14m-2)=1,155 ( gam)
=> m=3 => C3H4
tham khảo
Đáp án: C3H4
Giải thích các bước giải: Gọi CT c̠ủa̠ ankin X Ɩà CmH2m-2
\(n_{Br2}\)=0,07(mol)
CnH2n-2 + 2Br -> CnH2n-2Br2
0,035 <= 0,07( mol)
2 ankin có số mol bằng nhau, đều bằng : n=0,0175 mol
=>\(m_{hỗn.hợp}\)=0,0175.26+ 0,0175.(14m-2)=1,155( gam)
=> m=3 => C3H4
Dẫn 5,6 lít (đktc) khí metan và etilen đi qua bình đựng dung dịch nước brom, đã làm mất màu hoàn toàn dung dịch có chứa 4 gam brom. Thể tích khí metan (đktc) trong hỗn hợp là
A. 0,56 lít.
B. 5,04 lít.
C. 0,28 lít.
D. 3,36 lít
Dẫn 2 khí qua dung dịch nước brom chỉ có C 2 H 4 phản ứng
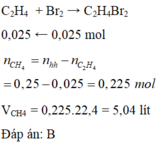
Hỗn hợp X gồm C3H6, C4H10, C2H2 và H2. Nung bình kín chứa m gam X và một ít bột Ni đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp Y. Đốt cháy hoàn toàn Y, thu được V lít CO2 (đktc) và 0,675 mol H2O. Biết hỗn hợp Y làm mất màu tối đa 150 ml dung dịch Br2 1M. Cho 11,2 lít X (đktc) đi qua bình đựng dung dịch brom dư thì có 64 gam Br2 phản ứng. Giá trị của V là
A. 17,92
B. 15,68
C. 13,44
D. 16,80
Đáp án : C
X gồm a mol C3H6 ; b mol C4H10 ; c mol C2H2 ; d mol H2
,nH2O = 3a + 5b + c + d = 0,675 mol
,nCO2 = 3a + 4b + 2c
,nBr2 = nC3H6 + 2nC2H2 – nH2 = a + 2c – d = 0,15 (*)
Trong 0,5 mol X giả sử có lượng chất gấp t lần trong m(g)
=> 0,5 = t.(a + b + c + d)
,nBr2(2) = t.(a + 2c) = 0,4
=> a – 4b + 6c – 4d = 0 (**)
Lấy 4(*) – (**) => 3a + 4b + 2c = 0,6 mol = nCO2
=>V = 13,44 lit
Hỗn hợp X gồm 0,5 mol một ankin A và 0,7 mol H 2 . Nung nóng X với bột Ni xúc tác, sau một thời gian thu được hỗn hợp Y, có tỉ khối so với hiđro bằng 13,375. Hỗn hợp Y phản ứng tối đa với 96 gam brom trong dung dịch. Ankin A là
A. But-1-in.
B. But-2-in.
C. Propin.
D. Axetilen.
Hỗn hợp X gồm 0,5 mol một ankin A và 0,7 mol H2. Nung nóng X với bột Ni xúc tác, sau một thời gian thu được hỗn hợp Y, có tỉ khối so với hiđro bằng 13,375. Hỗn hợp Y phản ứng tối đa với 96 gam brom trong dung dịch. Ankin A là
A. Propin
B. Axetilen
C. But-1-in
D. But-2-in
Đáp án : A
,nBr2 = 0,6 mol = npi(Y)
=> nH2 pứ = npi(X) – npi(Y) = 0,5.2 – 0,6 = 0,4 mol
=> nY = nX – nH2 pứ = 1,2 – 0,4 = 0,8 mol
=> mY = mX = 21,4g
=> MA = 40g (C3H4)
Cho hỗn hợp khí A gồm 0,1 mol axetilen, 0,2 mol etilen, 0,1 mol etan và 0,36 mol hidro đi qua ống sứ đựng Ni làm xúc tác, đun nóng, thu được hỗn hợp khí B. Dẫn hỗn hợp khí B qua bình đựng nước brom dư, khối lượng bình tăng 1,64 gam và có hỗn hợp khí C thoát ra khỏi bình brom. Khối lượng của hỗn hợp khí C bằng bao nhiêu?
A. 13,26 gam
B. 10,28 gam
C. 9,58 gam
D. 8,2 gam
Bài toán trên có thể tóm tắt theo sơ đồ sau:
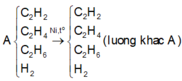
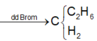
Yêu cầu cần tính khối lượng khí thoát ra trong khi biết khối lượng đầu và khối lượng bị giữ lại, vì thế đơn giản là áp dụng bảo toàn khối lượng ta được:
![]()
![]()
![]()
Hỗn hợp X gồm ankan, anken và ankađien. Đốt cháy hoàn toàn hỗn hợp X thì thu được CO2 và H2O theo tỷ lệ mol 1 : 1. Hãy cho biết 0,2 mol hỗn hợp X có thể làm mất màu dung dịch chứa tối đa bao nhiêu gam dung dịch brom 16%?
A. 200,0 gam
B. 150,0 gam
C. 120,0 gam
D. 250,0 gam
Đốt cháy hoàn toàn hỗn hợp X thì
thu được CO2 và H2O theo tỷ lệ mol 1 : 1
⇒ n ankan = n ankađien
⇒ n Br2 = 2n ankanđien + n anken
= nX = 0,2
m dung dịch = 0,2 . 160 : 16%
= 200g
Đáp án A.
Hỗn hợp Z gồm 3 hiđrocacbon là C3H8, CxHy và CxH2x có tỉ lệ mol tương ứng là 1:2:3. Dẫn V lit hỗn hợp Z vào bình đựng dung dịch brom (dư) thấy số mol brom phản ứng tối đa là 0,18 mol và còn lại hỗn hợp khí T thoát ra khỏi bình chỉ chứa 2 hiđrocacbon có thể tích bằng 50% thể tích của hỗn hợp Z ban đầu. Mặt khác, nếu đốt cháy hoàn toàn 16,128 lit hỗn hợp Z trên bằng lượng oxi vừa đủ rồi dẫn toàn bộ sản phẩm cháy lần lượt đi qua bình 1 chứa dung dịch H2SO4 đặc (dư), sau đó dẫn tiếp qua bình 2 chứa 2,0 lit dung dịch Ba(OH)2 1,19M. Kết quả thấy bình 1 tăng 56,16 gam, còn ở bình 2 thì thu được 394 gam kết tủa. Giả thiết các phản ứng xảy ra hoàn toàn và các thể tích khí đều đo ở điều kiện tiêu chuẩn.
Xác định công thức phân tử của 2 hiđrocacbon và tính phần trăm khối lượng của 2 hiđrocacbon đó trong hỗn hợp Z.
Gọi: \(\left\{{}\begin{matrix}n_{C_3H_8}=a\left(mol\right)\\n_{C_xH_y}=2a\left(mol\right)\\n_{C_xH_{2x}}=3a\left(mol\right)\end{matrix}\right.\) (trong 16,128 (l))
\(\Rightarrow a+2a+3a=\dfrac{16,128}{22,4}=0,72\left(mol\right)\Rightarrow a=0,12\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{C_3H_8}=0,12\left(mol\right)\\n_{C_xH_y}=0,24\left(mol\right)\\n_{C_xH_{2x}}=0,36\left(mol\right)\end{matrix}\right.\)
Ta có: m bình 1 tăng = mH2O \(\Rightarrow n_{H_2O}=\dfrac{56,16}{18}=3,12\left(mol\right)\)
BTNT H, có: 0,12.8 + 0,24y + 0,36.2x = 3,12.2 (1)
Ta có: \(n_{Ba\left(OH\right)_2}=2.1,19=2,38\left(mol\right)\), \(n_{BaCO_3}=\dfrac{394}{197}=2\left(mol\right)\)
BTNT Ba, có: \(n_{Ba\left(HCO_3\right)_2}=2,38-2=0,38\left(mol\right)\)
BTNT C, có: 0,12.3 + 0,24.x + 0,36.x = nCO2 = nBaCO3 + 2nBa(HCO3)2 = 2 + 0,38.2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=4\\y=10\end{matrix}\right.\)
Vậy: CTPT cần tìm là C4H10 và C4H8.
Hỗn hợp T gồm 2 hidrocacbon → T gồm C3H8 và C4H10.
→ Chỉ C4H8 pư với Br2.
Ta có: \(n_{C_4H_8}=n_{Br_2}=0,18\left(mol\right)\)
\(\Rightarrow n_{C_3H_8}=\dfrac{0,18}{3}=0,06\left(mol\right)\)
\(n_{C_4H_{10}}=\dfrac{0,18}{3}.2=0,12\left(mol\right)\)
⇒ mZ = mC3H8 + mC4H10 + mC4H8 = 0,06.44 + 0,12.58 + 0,18.56 = 19,68 (g)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{C_3H_8}=\dfrac{0,06.44}{19,68}.100\%\approx13,41\%\\\%m_{C_4H_{10}}=\dfrac{0,12.58}{19,68}.100\%\approx35,37\%\%\\\%m_{C_4H_8}\approx51,22\%\end{matrix}\right.\)