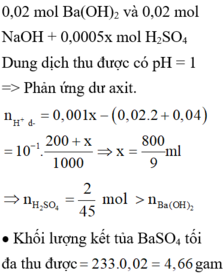200ml dung dịch A gồm CuSO4 1M và Fe2(SO4)3 0,5M phản ứng với dung dịch NaOH dư . Khối lượng kết tủa sau phản ứng là ?

Những câu hỏi liên quan
200ml dung dịch A gồm CuSO4 1M và Fe2(SO4)3 0,5M phản ứng với dung dịch NaOH dư. Tìm lượng kết tủa sau phản ứng : D. 41g B. 45g C. 40g D. 41g
Đọc tiếp
200ml dung dịch A gồm CuSO4 1M và Fe2(SO4)3 0,5M phản ứng với dung dịch NaOH dư. Tìm lượng kết tủa sau phản ứng :
D. 41g
B. 45g
C. 40g
D. 41g
Đáp án D
n Cu(OH)2 = 0,2 mol; n Fe(OH)3 = 2n Fe2(SO4)3 = 0,2 mol
m↓ = mCu(OH)2 + mFe(OH)3 = 0,2.98 + 0,2.107 = 41g
Đúng 0
Bình luận (0)
Cho m gam Zn vào 200ml dung dịch CuSO4 1M và Fe2(SO4)3 0,5M sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X có khối lượng tăng lên 6,62 gam. Giá trị của m là : A. 14,30 B. 13,00 C. 16,25 D. 11,70
Đọc tiếp
Cho m gam Zn vào 200ml dung dịch CuSO4 1M và Fe2(SO4)3 0,5M sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X có khối lượng tăng lên 6,62 gam. Giá trị của m là :
A. 14,30
B. 13,00
C. 16,25
D. 11,70
Cho 11,2 g fe vào 100 ml dung dịch A gồm CuSO4 có nồng độ x M và Fe2(SO4)3 1M sau phản ứng hoàn toàn thu được dung dịch x và 6,4 g chất rắn y .ngâm y trong dung dịch HCL dư không có khí thoát ra cho dung dịch NaOH đến dư vào dung dịch x lọc kết tủa nung trong không khí đến khối lượng không đổi thu được 40 gam chất rắn tính x
Câu 10: Cho 200ml dung dịch AlCl3 1M tác dụng với dung dịch NaOH 0,5M. Sau phản ứng thu được một kết tủa keo, lấy kết tủa đem nung đến khối lượng không đổi thu được 5,1 gam chất rắn. Tính thể tích dung dịch NaOH đã tham gia phản ứng.
\(n_{AlCl_3}=0.2\cdot1=0.2\left(mol\right)\)
\(n_{NaOH}=0.5V\left(mol\right)\)
\(n_{Al_2O_3}=\dfrac{5.1}{102}=0.05\left(mol\right)\)
\(2Al\left(OH\right)_3\underrightarrow{^{^{t^0}}}Al_2O_3+3H_2O\)
\(0.1...............0.05\)
TH1 : Al(OH)3 không bị hòa tan.
\(AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3+3NaCl\)
\(0.1...........0.3................0.1\)
\(\Leftrightarrow V=\dfrac{0.3}{0.5}=0.6\left(l\right)\)
TH2 : Al(OH)3 bị hòa tan một phần
\(AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3+3NaCl\)
\(0.2...........0.6................0.2\)
\(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\)
\(0.5V-0.6...0.5V-0.6\)
\(n_{Al\left(OH\right)_3}=0.2+0.5V-0.6=0.1\left(mol\right)\)
\(\Rightarrow V=1\left(l\right)\)
Đúng 4
Bình luận (1)
Cho m gam hỗn hợp gồm Mg và Al vào 200 ml dung dịch Fe2(SO4)3 0,4M và CuSO4 0,8M. Sau khi kết thúc phản ứng, thu được dung dịch X và 20,19 gam rắn Y. Cho dung dịch NaOH dư vào X, thấy lượng NaOH phản ứng là 36,8 gam. Giá trị của m là A. 9,24 B. 9,51 C. 8,52 D. 10,14
Đọc tiếp
Cho m gam hỗn hợp gồm Mg và Al vào 200 ml dung dịch Fe2(SO4)3 0,4M và CuSO4 0,8M. Sau khi kết thúc phản ứng, thu được dung dịch X và 20,19 gam rắn Y. Cho dung dịch NaOH dư vào X, thấy lượng NaOH phản ứng là 36,8 gam. Giá trị của m là
A. 9,24
B. 9,51
C. 8,52
D. 10,14
Cho 200ml dung dịch hỗn hợp gồm Ba(OH)2 0,1 M và NaOH 0,1M phản ứng với X ml dung dịch H2SO4 0,5M thu được (200 + x) ml dung dịch có pH 1. Sau phản ứng khối lượng kết tủa tối đa thu được là A. 9,32 gam B. 2,33 gam C. 12,94 gam D. 4,66 gam
Đọc tiếp
Cho 200ml dung dịch hỗn hợp gồm Ba(OH)2 0,1 M và NaOH 0,1M phản ứng với X ml dung dịch H2SO4 0,5M thu được (200 + x) ml dung dịch có pH = 1. Sau phản ứng khối lượng kết tủa tối đa thu được là
A. 9,32 gam
B. 2,33 gam
C. 12,94 gam
D. 4,66 gam
Cho 200ml dung dịch hỗn hợp gồm Ba(OH)2 0,1 M và NaOH 0,1M phản ứng với X ml dung dịch H2SO4 0,5M thu được (200 + x) ml dung dịch có pH 1. Sau phản ứng khối lượng kết tủa tối đa thu được là: A. 9,32 gam. B. 2,33 gam. C. 12,94 gam. D. 4,66 gam.
Đọc tiếp
Cho 200ml dung dịch hỗn hợp gồm Ba(OH)2 0,1 M và NaOH 0,1M phản ứng với X ml dung dịch H2SO4 0,5M thu được (200 + x) ml dung dịch có pH = 1. Sau phản ứng khối lượng kết tủa tối đa thu được là:
A. 9,32 gam.
B. 2,33 gam.
C. 12,94 gam.
D. 4,66 gam.
0,02 mol Ba(OH)2 và 0,02 mol NaOH + 0,0005x mol H2SO4
Dung dịch thu được có pH = 1 => Phản ứng dư axit.
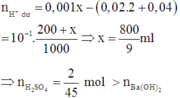
Khối lượng kết tủa BaSO4 tối đa thu được =233.0,02=4,66 gam
=> Chọn đáp án D.
Đúng 0
Bình luận (0)
Cho 200ml dung dịch hỗn hợp gồm Ba(OH)2 0,1 M và NaOH 0,1M phản ứng với x ml dung dịch H2SO4 0,5M thu được (200 + x) ml dung dịch có pH = 1. Sau phản ứng khối lượng kết tủa tối đa thu được là
Cho NH3 dư vào 100ml dung dịch gồm CuSO4 1M ; ZnCl2 0,5M và AgNO3 1M . Tính lượng kết tủa tạo ra sau phản ứng :
A. 9,8g
B. 4,9g
C. 18g
D. 0g
Dung dịch NH3 có khả năng hòa tan hiđroxit hay muối ít tan của một số kim loại (Ag, Cu, Zn), tạo thành các dung dịch phức chất.
CuSO4 + 2NH3 + 2H2O → Cu(OH)2 + (NH4)2SO4
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2
Vậy sau phản ứng không thu được kết tủa
Đáp án D.
Đúng 0
Bình luận (0)