tiến hành 2 thí nghiệm như sau, thí nghiệm nào có tốc độ phản ứng lớn hơn ? Hãy cho biết, người ta sử dụng yếu tố nào để làm tăng tốc độ phản ứng viết pthh?
Thí nghiệm (1) Zn + dd HCl 2M ở 25 độ C
Thí nghiệm (2) Zn + dd HCl 4 M ở nhiệt độ 25 độ C
Tiến hành 2 thí nghiệm như sau, thí nghiệm nào có tốc độ phản ứng lớn hơn ? Hãy cho biết, người ta sử dụng yếu tố nào để làm tăng tốc độ phản ứng? viết pt phản ứng ?
Ống nghiệm 1 : 10ml dd H2SO4 0,1M + 1 đinh sắt
Ống nghiệm 2 : 10ml dd H2SO4 0,1M + bột sắt có khối lượng tương đương
thí nghiện 2 có phản ứng nhanh hơn do bề mặt chất phảnứng thoáng hơn khiến cho tốc độ nhanh hơn
Tiến hành 2 thí nghiệm như sau, thí nghiệm nào có tốc độ phản ứng lớn hơn ? Hãy cho biết, người ta sử dụng yếu tố nào để làm tăng tốc độ phản ứng? viết pt phản ứng ?
Thí nghiệm 1 : Ống nghiệm 1 có chưa 20ml HCl, thêm vào 10g bột đá vôi
Thí nghiệm 2 : ống nghiệm 2 có chứa 20ml HCl, thêm 10g đá vôi dạng viên
thí nghiệm 2 phản ứng nhanh hơn do bề mặt tiếp xúc của thí nghiệm 2 nhiều hơn thí nghiệm 1
Trong phòng thí nghiệm, có thể điều chế oxi từ muối kali clorat. Người ta sử dụng cách nào sau đây nhằm mục đích tăng tốc độ phản ứng ?
A. Nung kaliclorat ở nhiệt độ cao
B. Nung hỗn hợp kali clorat và mangan đioxit ở nhiệt độ cao
C. Dùng phương pháp dời nước để thu khí oxi
D. Dùng phương pháp dời không khí để thu khí oxi
Chọn đáp án B.
Trong thí nghiệm điều chế khí oxi từ muối kali clorat người ta thường nung hỗn hợp kali clorat và mangan đioxit ở nhiệt độ cao nhằm mục đích tăng tốc độ phản ứng vì mangan đioxit có vai trò là chất xúc tác → Làm phản ứng nhanh đạt tới trạng thái cân bằng
Trong phòng thí nghiệm, có thể điều chế khí oxi từ muối kali clorat. Người ta sử dụng cách nào sau đây nhằm mục đích tăng tốc độ phản ứng ?
A. Nung kaliclorat ở nhiệt độ cao.
B. Nung hỗn hợp kali clorat và mangan đioxit ở nhiệt độ cao.
C. Dùng phương pháp dời nước để thu khí oxi.
D. Dùng phương pháp dời không khí để thu khí oxi.
Đáp án B
2KClO3 → M n O 2 , t ° 2KCl + 3O2
Sử dụng MnO2 làm chất xúc tác
Ba thí nghiệm được tiến hành với những khối lượng Zn bằng nhau và với 50 cm 3 dung dịch loãng H 2 SO 4 2M. PTHH của phản ứng :
Zn + H 2 SO 4 → Zn SO 4 + H 2
Bảng dưới đây cho biết các điều kiện của mỗi thí nghiệm :
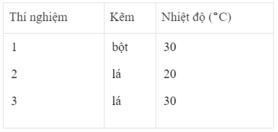
Khí hiđro thu được trong mỗi thí nghiệm được ghi lại theo những khoảng cách nhất định về thời gian cho đến khi phản ứng kết thúc, được biểu diễn bằng đồ thị sau :
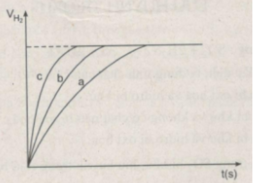
Hãy quan sát đồ thị trên để cho biết các đường cong a, b, c biểu thị cho những thí nghiệm nào ?
Đồ thị biểu diễn các phản ứng :
Đường cong c biểu diễn cho thí nghiệm 1, phản ứng xảy ra nhanh nhất
Đường cong b biểu diễn cho thí nghiệm 3, phản ứng xảy ra nhanh trung bình.
Đường cong a biểu diễn cho thí nghiệm 2, phản ứng xảy ra chậm nhất.
Người ta có thể điều chế một số chất khí bằng những phản ứng hoá học sau : Dung dịch H 2 SO 4 loãng tác dụng với Zn.
- Hãy cho biết tên chất khí được sinh ra trong mỗi phản ứng trên và viết PTHH của các phản ứng.
- Bằng thí nghiệm nào có thể khẳng định được chất khí sinh ra trong mỗi thí nghiệm ?
Khí H 2 cháy trong không khí kèm theo tiếng nổ nhỏ.
H 2 SO 4 + Zn → Zn SO 4 + H 2
H 2 + 1/2 O 2 → H 2 O
Thực hiện thí nghiệm hòa tan đá vôi (CaCO3) bằng dung dịch HCl, biện pháp nào sau đây có thể làm tăng tốc độ phản ứng?
A. Tăng thể tích của dung dịch HCl
B. Giảm nồng độ của dung dịch HCl
C. Hạ nhiệt độ xuống
D. Nghiền nhỏ đá vôi
. Có một hỗn hợp gồm Fe và FeO. Người ta tiến hành 2 thí nghiệm sau:
* Thí nghiệm 1: Cho khí CO (dư) đi qua a gam hỗn hợp ở nhiệt độ cao, thu được 11,2 gam Fe.
* Thí nghiệm 2: Ngâm a gam hỗn hợp trong dung dịch HCl dư, sau phản ứng thu được 2,24 lít khí H2 (đktc).
a) Viết các phương trình phản ứng xảy ra.
b) Tính thành phần % theo khối lượng của mỗi chất trong hỗn hợp đầu.
a) PTHH:
FeO + CO --to--> Fe + CO2 (1)
Fe + 2HCl ---> FeCl2 + H2 (2)
b) \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
=> nFe = 0,1 (mol)
=> mFe (từ FeO) = 11,2 - 0,1.56 = 5,6 (g)
=> \(n_{FeO}=n_{Fe\left(FeO\right)}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
\(\rightarrow m_{hh}=0,1.72+0,1.56=12,8\left(g\right)\\ \Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{5,6}{12,8}.100\%=43,75\%\\\%m_{FeO}=100\%-43,75\%=56,25\%\end{matrix}\right.\)
Người ta có thể điều chế một số chất khí bằng những phản ứng hoá học sau : Dung dịch HCl đặc tác dụng với MnO 2
- Hãy cho biết tên chất khí được sinh ra trong mỗi phản ứng trên và viết PTHH của các phản ứng.
- Bằng thí nghiệm nào có thể khẳng định được chất khí sinh ra trong mỗi thí nghiệm ?
Khí Cl 2 khí clo ẩm có tính tẩy màu.
4HCl + MnO 2 → Mn Cl 2 + Cl 2 + 2 H 2 O