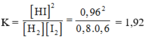18. Cho phản ứng: H2 (k) + I2 (k) 2 HI (k)
a) Viết biểu thức của định luật tác dụng khối lượng cho phản ứng trên, biết rằng bậc phản ứng riêng của phản ứng theo H2 và I2 đều bằng 1.
b) Ở 508o C nếu nồng độ của H2 là 0,04 M và I2 là 0,05 M thì tốc độ của phản ứng là 3,2.10−4 mol/l.s. Nếu nồng độ đầu của mỗi chất đều bằng 0,04 M thì cần bao lâu để 50% lượng H2 phản ứng?
c) Tốc độ phản ứng thay đổi ra sao khi tăng áp suất của hệ lên gấp đôi nhưng nhiệt độ của hệ vẫn giữ nguyên không đổi? 19. Kh...
Đọc tiếp
18. Cho phản ứng: H2 (k) + I2 (k) = 2 HI (k)
a) Viết biểu thức của định luật tác dụng khối lượng cho phản ứng trên, biết rằng bậc phản ứng riêng của phản ứng theo H2 và I2 đều bằng 1.
b) Ở 508o C nếu nồng độ của H2 là 0,04 M và I2 là 0,05 M thì tốc độ của phản ứng là 3,2.10−4 mol/l.s. Nếu nồng độ đầu của mỗi chất đều bằng 0,04 M thì cần bao lâu để 50% lượng H2 phản ứng?
c) Tốc độ phản ứng thay đổi ra sao khi tăng áp suất của hệ lên gấp đôi nhưng nhiệt độ của hệ vẫn giữ nguyên không đổi? 19. Khi tăng nhiệt độ từ 50o C lên 100o C, vận tốc của phản ứng tăng lên 243 lần. Hãy cho biết khi tăng nhiệt độ từ 50o C lên 80o C vận tốc phản ứng tăng lên bao nhiêu lần?
20. Phản ứng H2 + I2 à 2HI có năng lượng hoạt hoá bằng 171,71 kJ/mol. Tốc độ phản ứng thay đổi như thế nào khi có mặt chất xúc tác năng lượng hoạt hoá bằng 130,68 kJ/mol ở 300K? Biết hằng số khí lý tưởng R = 8,314 J/K.mol.