Viết phương trình hóa học của các phản ứng xảy ra trong mỗi trường hợp sau:
a) Toluen tác dụng với hiđro có xúc tác Ni, áp suất cao, đun nóng.
b) Đun nóng benzen với hỗn hợp HNO3 đặc và H2SO4 đặc
Viết phương trình hoá học của các phản ứng xảy ra trong mỗi trường hợp sau:
Toluen tác dụng với hiđro có xúc tác Ni, áp suất cao, đun nóng.
Viết phương trình hoá học của các phản ứng xảy ra trong mỗi trường hợp sau: Đun nóng benzen với hỗn hợp HNO3 đặc và H2SO4 đặc.
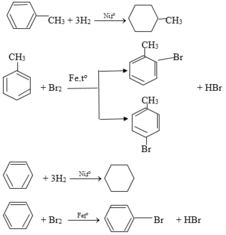
Toluen và benzen cùng phản ứng được với chất nào sau đây: (1) dung dịch brom trong CCl4; (2) dung dịch kali pemanganat; (3) hiđro có xúc tác Ni, đun nóng; (4)Br2 có bột Fe, đun nóng? Viết phương trình hoá học của các phương trình xảy ra.
Toluen và benzen cùng phản ứng hidro có xúc tác Ni
Đun nóng; Br2 có bột Fe đun nóng
Viết các phương trình hóa học ( ghi điều kiện phản ứng) xảy ra trong mỗi trường hợp sau: a) Kẽm tác dụng với lưu huỳnh
b) Canxi tác dụng với brom
c) Đồng tác dụng với H 2 S O 4 đặc, đun nóng
Viết phương trình hoá học của các phản ứng xảy ra trong các trường hợp sau và cho biết các phản ứng đó thuộc loại phản ứng nào (phản ứng thế, phản ứng cộng, phản ứng tách).
-Etilen tác dụng với hiđro có Ni làm xúc tác và đun nóng.
-Đun nóng axetilen ở 600oC với bột than làm xúc tác thu được benzen.
-Dung dịch ancol etylic để lâu ngoài không khí chuyển thành dung dịch axit axetic (giấm ăn).
Viết phương trình hóa học của phản ứng xảy ra khi:
Propilen tác dụng với hidro, đun nóng (xúc tác Ni).
Hãy viết phương trình hóa học và ghi rõ điều kiện của các phản ứng sau:
1. Trùng hợp etilen.
2. Axit axetic tác dụng với magie.
3. Oxi hóa rượu etylic thành axit axetic.
4. Đun nóng hỗn hợp rượu etylic và axit axetic có axit sunfuric đặc làm xúc tác
Đun nóng hỗn hợp gồm 8,05 gam rượu etylic và 36 g axit axetic có H2SO4 đặc xúc tác thu được 12,32 gam etyl axetat. a, viết chương trình phản ứng xảy ra b, sau phản ứng chất nào còn dư và dư bao nhiêu gam c, tính hiệu suất phản ứng este hóa nói trên. M.n giúp tớ vớiiii Tớ đang thi r
nC2H5OH = 8.05/46 = 0.175 (mol)
nCH3COOH = 36/60 = 0.6 (mol)
nCH3COOC2H5 = 12.32/88 = 0.14 (mol)
C2H5OH + CH3COOH <-H2SO4đ,t0-> CH3COOC2H5 + H2O
1.......................1
0.175................0.6
LTL : 0.175/1 < 0.6/1
=> CH3COOH dư
mCH3COOH (dư) = ( 0.6 - 0.175) * 60 = 25.5 (g)
nCH3COOC2H5 = nC2H5OH = 0.175 (mol)
H% = 0.14/0.175 * 100% = 80%
Viết phương trình hóa học khi H 2 S O 4 đặc, đun nóng tác dụng với Cu. Có hiện tượng gì để biết phản ứng đã xảy ra?