Câu 4: Cho 139,2 gam MnO 2 tác dụng với dung dịch HCl đặc dư thu được bao nhiêu lít khí Cl 2 (đktc)?
Câu 5: Thể tích của dung dịch NaOH 1M cần dùng để tác dụng hoàn toàn với 6,72 lít khí Cl 2 (đktc) là ?
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở đktc. Giá trị của m là được 8,96 lít khí. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở đktc. Giá trị của m là
A. 7,80.
B. 14,55.
C. 6,45.
D. 10,2.
Câu 1.Đốt cháy hoàn toàn 2 gam một mẩu than có lẫn tạp chất, thu được 3,36 lít khí CO2 ở đktc. Thành phần % theo khối lượng của cacbon có trong mẩu than là bao nhiêu?
Câu 2.Cần dùng bao nhiêu gam Al tác dụng với dung dịch HCl, thì thu được 6,72 lít khí hiđro (đktc)?
Câu 1:
\(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: C + O2 --to--> CO2
0,15<-----------0,15
=> \(\%C=\dfrac{0,15.12}{2}.100\%=90\%\)
Câu 2:
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,2<-------------------0,3
=> mAl = 0,2.27 = 5,4 (g)
Câu 1.
\(n_{CO_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(C+O_2\underrightarrow{t^o}CO_2\)
0,15 0,15
\(m_C=0,15\cdot12=1,8g\)
\(\%C=\dfrac{1,8}{2}\cdot100\%=90\%\)
Câu 2.
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
0,2 0,3
\(m_{Al}=0,2\cdot27=5,4g\)
Cho a gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí. Mặt khác, ở cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích các khí đo ở đktc. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 7,8.
B. 6,45.
C. 10,2.
D. 14,55.
Cho a gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí. Mặt khác, ở cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích các khí đo ở đktc. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 7,8
B. 6,45
C. 10,2.
D. 14,55.
Đáp án A
Gọi số mol Mg và Al lần lượt là x và y mol.
X phản ứng với HCl :
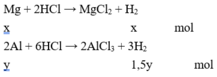
→ x + 1,5y = 0,4.
X tác dụng với NaOH chỉ có Al phản ứng :
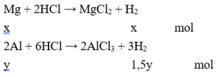
Giải hệ phương trình được x = 0,1 và y = 0,2.
a = 0,1.24 + 0,2.27 = 7,8 gam.
Cho m (gam) hỗn hợp Al, Mg tác dụng với dung dịch HCl dư thu được 12,32 lít khí (đktc). Mặt khác, cũng m (gam) hỗn hợp trên cho tác dụng với dung dịch NaOH dư thu được 6,72 lít khí (đktc). Tính giá trị của m
A. 28,2 gam
B. 22,8 gam
C. 14,1 gam
D. 11,4 gam
Cho m gam bột sắt vào 200 ml dung dịch CuSO4 1M, sau phản ứng hoàn toàn thu được chất rắn X. Chia X thành 2 phần không bằng nhau:
Phần 1: cho tác dụng với dung dịch HCl dư thấy thoát ra 2,24 lít khí H2 (đktc).
Phần 2: cho tác dụng với dung dịch HNO3 loãng dư, thu được 6,72 lít khí NO (đktc). NO là sản phẩm khử duy nhất của HNO3.
Giá trị của m gần nhất với giá trị nào sau đây?
A. 28,2
B. 30,8
C. 26,4
D. 24,0
Đáp án A
- P1: hỗn hợp rắn X + HCl → H2 => chứng tỏ Fe dư, Cu2+ phản ứng hết.
Fe + 2HCl → FeCl2 + H2
=> nFe(1) = nH2 = 2,24: 22,4 = 0,1 mol
- P2: X + HNO3 → NO => Cả Fe và Cu đều phản ứng
Giả sử số mol ở phần 2 gấp k lần phần 1. Gọi số mol Cu phần 1 là a
Bảo toàn electron: 3nFe(2) + 2nCu(2) = 3nNO = 3.6,72: 22,4 = 0,9 mol
=> 3.0,1k + 2.ak = 0,9 (*)
Bảo toàn nguyên tố Cu: nCuSO4 = nCu(1) + nCu(2) => 0,2 = a + ak => a = 0 , 2 k + 1
Thay vào (*) =>0,3k + 2k. 0 , 2 k + 1 = 0,9
=> k = 2,097
- Vì Fe dư sau phản ứng nên: nFe pứ = nCuSO4 = 0,2 mol
=> nFe = nFe pứ + nFe(1) + nFe(2) = 0,3 + 0,1k = 0,5097 mol
=> mFe = 28,5432g (Gần nhất với giá trị 28,2g)
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở đktc. Giá trị của m là
A. 7,80.
B. 14,55.
C. 6,45.
D. 10,2.
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở đktc. Giá trị của m là
A. 7,80.
B. 14,55.
C. 6,45.
D. 10,2.
Đáp án A
Cách 1:
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
0,3 (mol)
Mg + 2HCl → MgCl2 + H2↑ (2)
0,1 ← (0,4- 0,3) (mol)
Chỉ có Al tác dụng với dd NaOH
Al + NaOH + H2O → NaAlO2 + 3/2. H2↑ (3)
0,2 ← 0,3 (mol)
nH2(1+2) = 8,96: 22,4 = 0,4 (mol) ; nH2 (3) = 6,72 : 22,4 = 0,3 (mol)
=> m = 0,2. 27 + 0,1.24 = 7,8 (g)
Cách 2: nAl = 2/3 nH2 sinh ra do t/d với NaOH = 2/3. 0,3 = 0,2 (mol)
nMg = nH2 sinh ra do t/d với HCl - nH2 sinh ra do t/d với NaOH = 0,4 – 0, 3= 0,1 (mol)
=> m = 0,2.27 + 0,1.24 = 7,8 (g)
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở đktc. Giá trị của m là
A. 7,80.
B. 14,55.
C. 6,45.
D. 10,2.
Đáp án A
Phương pháp:
Cách 1: Viết PTHH, tính toán theo PTHH
Cách 2: Bảo toàn electron
Hướng dẫn giải:
Cách 1:
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
0,3 (mol)
Mg + 2HCl → MgCl2 + H2↑ (2)
0,1 ← (0,4- 0,3) (mol)
Chỉ có Al tác dụng với dd NaOH
Al + NaOH + H2O → NaAlO2 + 3/2. H2↑ (3)
0,2 ← 0,3 (mol)
nH2(1+2) = 8,96: 22,4 = 0,4 (mol) ; nH2 (3) = 6,72 : 22,4 = 0,3 (mol)
=> m = 0,2. 27 + 0,1.24 = 7,8 (g)
Cách 2: nAl = 2/3 nH2 sinh ra do t/d với NaOH = 2/3. 0,3 = 0,2 (mol)
nMg = nH2 sinh ra do t/d với HCl - nH2 sinh ra do t/d với NaOH = 0,4 – 0, 3= 0,1 (mol)
=> m = 0,2.27 + 0,1.24 = 7,8 (g)