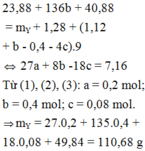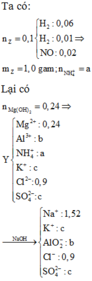Cho m g hỗn hợp gồm Al và Fe có tỉ lệ số mol tương ứng 2:1 vào cốc đựng dung dịch HCl dư Sau khi khí bay ra hết, phản ứng hoàn toàn, thấy khối lượng cốc tăng thêm 10,2g.Tính m

Những câu hỏi liên quan
Cho m g hỗn hợp gồm Al và Fe có tỉ lệ số mol tương ứng 2:1 vào cốc đựng dung dịch HCl dư Sau khi khí bay ra hết, phản ứng hoàn toàn, thấy khối lượng cốc tăng thêm 10,2g.Tính m
Gọi 2a là mol Al; a là mol Fe
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(\rightarrow n_{H2}=3a+a=4a\left(mol\right)\)
m tăng= m kim loại- mH2
\(\rightarrow27.2a+56a-2.4a=10,2\)
\(\Leftrightarrow a=0,1\)
\(\rightarrow m=m_{Al}+m_{Fe}=11\left(g\right)\)
Một hỗn hợp Y có khối lượng m gam gồm 3 kim loại Mg, Zn, Fe biết tỷ lệ số mol của Mg, Zn, Fe trong hỗn hợp Y lần lượt là 1 : 2 : 3 . Cho hỗn hợp Y vào dung dịch HCl dư đến phản ứng xảy ra hoàn toàn thấy khối lượng dung dịch HCl tăng thêm (m - 2,4) gam. Tính giá trị của m.
Đọc tiếp
Một hỗn hợp Y có khối lượng m gam gồm 3 kim loại Mg, Zn, Fe biết tỷ lệ số mol của Mg, Zn, Fe trong hỗn hợp Y lần lượt là 1 : 2 : 3 . Cho hỗn hợp Y vào dung dịch HCl dư đến phản ứng xảy ra hoàn toàn thấy khối lượng dung dịch HCl tăng thêm (m - 2,4) gam. Tính giá trị của m.
Đặt \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Zn}=2a\left(mol\right)\\n_{Fe}=3a\left(mol\right)\end{matrix}\right.\)
Ta có: \(m_{t\text{ăng}}=m_{KL}-m_{H_2}\)
\(\Rightarrow m-m_{H_2}=m-2,4\\ \Leftrightarrow m_{H_2}=2,4\left(g\right)\Rightarrow n_{H_2}=\dfrac{2,4}{2}=1,2\left(mol\right)\)
PTHH:
`Mg + 2HCl -> MgCl_2 + H_2`
`Zn + 2HCl -> ZnCl_2 + H_2`
`Fe + 2HCl -> FeCl_2 + H_2`
Theo PTHH:
\(n_{H_2}=n_{Mg}+n_{Zn}+n_{Fe}=a+2a+3a=6a\left(mol\right)\\ \Rightarrow6a=1,2\Leftrightarrow a=0,2\left(mol\right)\\ \Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,2\left(mol\right)\\n_{Zn}=0,2.2=0,4\left(mol\right)\\n_{Fe}=0,2.3=0,6\left(mol\right)\end{matrix}\right.\)
Vậy \(m=0,2.24+0,4.65+0,6.56=64,4\left(g\right)\)
Đúng 1
Bình luận (0)
Một hỗn hợp Y có khối lượng m gam gồm 3 kim loại Mg, Zn, Fe biết tỷ lệ số mol của Mg, Zn, Fe trong hỗn hợp Y lần lượt là 1 : 2 : 3 . Cho hỗn hợp Y vào dung dịch HCl dư đến phản ứng xảy ra hoàn toàn thấy khối lượng dung dịch HCl tăng thêm (m - 2,4) gam. Tính giá trị của m.
Đọc tiếp
Một hỗn hợp Y có khối lượng m gam gồm 3 kim loại Mg, Zn, Fe biết tỷ lệ số mol của Mg, Zn, Fe trong hỗn hợp Y lần lượt là 1 : 2 : 3 . Cho hỗn hợp Y vào dung dịch HCl dư đến phản ứng xảy ra hoàn toàn thấy khối lượng dung dịch HCl tăng thêm (m - 2,4) gam. Tính giá trị của m.
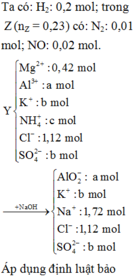
Cho 23,88 gam hỗn hợp X gồm Mg, MgO, Mg(NO3)2 và Al tan hoàn toàn trong dung dịch chứa KHSO4 và 1,12 mol HCl loãng. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y chỉ chứa m gam hỗn hợp các muối trung hòa và hỗn hợp 5,152 lít khí Z gồm H2, N2 và NO có tỉ lệ số mol tương ứng là 20 : 1 : 2. Cho NaOH dư vào Y thì thấy có 1,72 mol NaOH phản ứng đồng thời xuất hiện 24,36 gam kết tủa. Giá trị của m là: A. 98,83 gam B. 104,24 gam C. 104,26 gam D. 110,68 gam
Đọc tiếp
Cho 23,88 gam hỗn hợp X gồm Mg, MgO, Mg(NO3)2 và Al tan hoàn toàn trong dung dịch chứa KHSO4 và 1,12 mol HCl loãng. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y chỉ chứa m gam hỗn hợp các muối trung hòa và hỗn hợp 5,152 lít khí Z gồm H2, N2 và NO có tỉ lệ số mol tương ứng là 20 : 1 : 2. Cho NaOH dư vào Y thì thấy có 1,72 mol NaOH phản ứng đồng thời xuất hiện 24,36 gam kết tủa. Giá trị của m là:
A. 98,83 gam
B. 104,24 gam
C. 104,26 gam
D. 110,68 gam
Cho 20,96 gam hỗn hợp X gồm Mg, MgO, Mg(NO3)2 và Al tan hoàn toàn trong dung dịch chứa KHSO4 và 0,9 mol HCl loãng. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y chỉ chứa m gam hỗn hợp các muối trung hòa và hỗn hợp 2,016 lít khí Z gồm H2, N2 và NO có tỉ lệ mol tương ứng là 6:1:2. Cho NaOH dư vào Y thì thấy có 1,52 mol NaOH phản ứng đồng thời xuất hiện 13,92 gam kết tủa. Giá trị của m là: A. 94,16 gam. B. 88,12 gam. C. 82,79 gam. D. 96,93 gam.
Đọc tiếp
Cho 20,96 gam hỗn hợp X gồm Mg, MgO, Mg(NO3)2 và Al tan hoàn toàn trong dung dịch chứa KHSO4 và 0,9 mol HCl loãng. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y chỉ chứa m gam hỗn hợp các muối trung hòa và hỗn hợp 2,016 lít khí Z gồm H2, N2 và NO có tỉ lệ mol tương ứng là 6:1:2. Cho NaOH dư vào Y thì thấy có 1,52 mol NaOH phản ứng đồng thời xuất hiện 13,92 gam kết tủa. Giá trị của m là:
A. 94,16 gam.
B. 88,12 gam.
C. 82,79 gam.
D. 96,93 gam.
Cho 19 gam hỗn hợp gồm kim loại M ( hóa trị không đổi ) và Zn (có tỉ lệ mol tương ứng là 1,25:1) và bình đựng 4,48 lít khí Cl2 (đktc), sau các phản ứng hoàn toàn thu được hỗn hợp chất rắn X. Cho X tan hết trong dung dịch HCl (dư) thấy có 5,6 lít khí H2 thoát ra (đktc). Kim loại M là A. Mg B. Al C. Ca D. Na
Đọc tiếp
Cho 19 gam hỗn hợp gồm kim loại M ( hóa trị không đổi ) và Zn (có tỉ lệ mol tương ứng là 1,25:1) và bình đựng 4,48 lít khí Cl2 (đktc), sau các phản ứng hoàn toàn thu được hỗn hợp chất rắn X. Cho X tan hết trong dung dịch HCl (dư) thấy có 5,6 lít khí H2 thoát ra (đktc). Kim loại M là
A. Mg
B. Al
C. Ca
D. Na
Đáp án A
M → Mn+ + ne
1,25 → 1,25nx
Zn → Zn2+ + 2e
x → 2x
Cl2 + 2e → 2Cl-
0,2 → 0,4
2H+ + 2e → H2
0,5 ← 0,25
BT e ⇒1,25nx + 2x = 0,4 + 0,5 = 0,9 (1)
Mặt khác: 1,25M + 65M = 19 (2)
(1)(2) ⇒ (1,25M +65)/(1,25n + 2) = 19/0,9 ⇒ n = 2; M = 24(Mg)
Đúng 0
Bình luận (0)
Cho 19 gam hỗn hợp gồm kim loại M ( hóa trị không đổi ) và Zn (có tỉ lệ mol tương ứng là 1,25:1) và bình đựng 4,48 lít khí Cl2 (đktc), sau các phản ứng hoàn toàn thu được hỗn hợp chất rắn X. Cho X tan hết trong dung dịch HCl (dư) thấy có 5,6 lít khí H2 thoát ra (đktc). Kim loại M là: A. Mg B. Al C. K D. Na
Đọc tiếp
Cho 19 gam hỗn hợp gồm kim loại M ( hóa trị không đổi ) và Zn (có tỉ lệ mol tương ứng là 1,25:1) và bình đựng 4,48 lít khí Cl2 (đktc), sau các phản ứng hoàn toàn thu được hỗn hợp chất rắn X. Cho X tan hết trong dung dịch HCl (dư) thấy có 5,6 lít khí H2 thoát ra (đktc). Kim loại M là:
A. Mg
B. Al
C. K
D. Na
Đáp án A
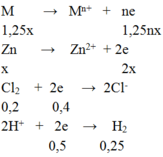
Bảo toàn e ⇒1,25nx + 2x = 0,4 + 0,5 = 0,9 (1)
Mặt khác: 1,25M + 65M = 19 (2)
Từ (1) và (2) ⇒ (1,25M +65M)/(1,25n + 2) = 19/0,9 ⇒ n = 2; M = 24(Mg)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam hỗn hợp Mg, Fe (tỉ lệ khối lượng tương ứng là 6 : 7) vào dung dịch HCl dư, sau phản ứng thu được dung dịch X chứa 3 chất tan có tỉ lệ mol là 2 : 1 : 1 và 672 ml khí H2 (dktc). Nhỏ dung dịch AgNO3 dư vào dung dịch X , sau khi phản ứng hoàn toàn thu được khí NO (sản phẩm khử duy nhất của N+5) và x gam kết tủa. Giá trị của x là A. 10,045 B. 10,315 C. 11,125 D. 8,61
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp Mg, Fe (tỉ lệ khối lượng tương ứng là 6 : 7) vào dung dịch HCl dư, sau phản ứng thu được dung dịch X chứa 3 chất tan có tỉ lệ mol là 2 : 1 : 1 và 672 ml khí H2 (dktc). Nhỏ dung dịch AgNO3 dư vào dung dịch X , sau khi phản ứng hoàn toàn thu được khí NO (sản phẩm khử duy nhất của N+5) và x gam kết tủa. Giá trị của x là
A. 10,045
B. 10,315
C. 11,125
D. 8,61
Cho 2 mẫu Zn có khối lượng bằng nhau vào cốc 1 đựng dung dịch HCl dư, cốc 2 đựng dung dịch hỗn hợp HCl và CuSO4 dư. Để phản ứng xẩy ra hoàn toàn ở cốc 1 thu được V1 lít khí, cốc 2 thu được V2 lít khí (các khí đo ở cùng điều kiện). So sánh V1 và V2? A. V1 V2 B. V1 V2 C. V1 V2 D. V1 ½ V2
Đọc tiếp
Cho 2 mẫu Zn có khối lượng bằng nhau vào cốc 1 đựng dung dịch HCl dư, cốc 2 đựng dung dịch hỗn hợp HCl và CuSO4 dư. Để phản ứng xẩy ra hoàn toàn ở cốc 1 thu được V1 lít khí, cốc 2 thu được V2 lít khí (các khí đo ở cùng điều kiện). So sánh V1 và V2?
A. V1 = V2
B. V1 < V2
C. V1 > V2
D. V1 < ½ V2
Chọn đáp án C
Chú ý : Vì ở cốc 2 có Zn phản ứng với Cu2+ nên V1 >V2
Tuy nhiên các bạn cũng chú ý là ở cốc 2 có ăn mòn điện hóa nên tốc độ nhanh hơn
Đúng 0
Bình luận (0)