Trộn 200ml dung dịch CuSO4 1M vào 300ml dung dịch NaOH 1M sau phản ứng hoàn toàn thu được A gam kết tủa X và B gam kết tủa Y
a) Viết phương trình hoá học
b) Tính A
c) Tính B
Giúp mình với, mình đang cần gấp.
0 câu trả lời
rót 300ml dung dịch CuSO4 1M vào 100ml dung dịch BaCl2 2M
a) tính khối lượng kết tủa thu được
b) cần bao nhiêu gam dung dịch NaOH 15% để làm kết tủa hoàn toàn dung dịch thu được sau phản ứng
a) \(\left\{{}\begin{matrix}n_{CuSO_4}=0,3.1=0,3\left(mol\right)\\n_{BaCl_2}=0,1.2=0,2\left(mol\right)\end{matrix}\right.\)
PTHH: \(CuSO_4+BaCl_2\rightarrow BaSO_4\downarrow+CuCl_2\)
Ban đầu: 0,3 0,2
Sau pư: 0,1 0 0,2 0,2
=> \(m_{kt}=m_{BaSO_4}=0,2.233=46,6\left(g\right)\)
b) \(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2\downarrow+Na_2SO_4\)
0,1-------->0,2
\(CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2\downarrow+2NaCl\)
0,2------>0,4
=> \(m_{ddNaOH}=\dfrac{\left(0,2+0,4\right).40}{15\%}=160\left(g\right)\)
Cho Mg vào 200ml dung dịch A chứa CuSO4 0,5M và FeSO4 1M. Sau khi các phản ứng xảy ra hoàn toàn thu được 12 gam chất rắn X và dung dịch Y. Cho dung dịch Y tác dụng với dung dịch Ba(OH)2 lấy dư đến khi kết thúc các phản ứng thu được kết tủa E. Nung E trong không khí đến khối lượng không đổi thu được b gam chất rắn. Tính b.
Tính toán theo PTHH :
Mg + CuSO4 → Cu + MgSO4
Mg + FeSO4 → Fe + MgSO4
Ba(OH)2 + MgSO4 → BaSO4 + Mg(OH)2
Ba(OH)2 + FeSO4 → BaSO4 + Fe(OH)2
Mg(OH)2 → MgO + H2O
2 Fe(OH)2 + ½ O2 → Fe2O3 + 2 H2O
Giả sư dung dịch muối phản ứng hết
=> n Fe = n FeSO4 = 0,2 . 1= 0,2 mol => m Fe = 0,2 . 56 = 11,2 g
=> n Cu =n CuSO4 = 0,2 . 0,5 = 0,1 mol => m Cu = 0,1 . 64 = 6,4 g
=> m chất rắn = 11,2 + 6,4 = 17,6 g > 12 g > 6,4
=> kim loại Fe dư sau phản ứng Vì CuSO4 phản ứng trước sau đó mới đến FeSO4 phản ứng
CuSO4 đã hết và phản ứng với 1 phần FeSO4
12 g = m Cu + m Fe phản ứng = 6,4 g + m Fe phản ứng
=> m Fe = 5,6 g => n Fe = 0,1 mol => n FeSO4 dư = 0,2 – 0,1 = 0,1 mol
Theo PTHH : n Mg = 0,1 + 0,1 = 0,2 mol ( bắng số mol CuSO4 và FeSO4 phản ứng )
Theo PTHH : n Mg = n MgSO4 = n Mg(OH)2 = n MgO = 0,2 mol
n FeSO4 dư = n Fe(OH)2 = n Fe2O3 . 2 = 0,1 mol
=> n Fe2O3 = 0,1 mol
=> m chất rắn = m Fe2O3 + m MgO = 0,1 . 160 + 0,2 . 40 = 24 g
trộn 300ml dung dịch hỗn hợp gồm Na2CO3 0,1M và NaHCO3 0,15M với 250ml dung dịch BaCl2 0,1M. Sau phản ứng thu được m gam kết tủa và dung dịch X
a. Tính m?
b. Cho từ 200ml dung dịch H2SO4 0,1M vào dung dịch X. Sau phản ứng hoàn toàn thu được Vlít khí (đo ở đktc). Tính V?
mong mọi người lm nhanh giúp mik vs ạ
Hoà tan hết a gam Al vào 450 ml dung dịch NaOH 1M thu được 13,44 lít H2 (đktc) và dung dịch X. Hoà tan hết b gam Al vào 400 ml dung dịch HCl 1M thu được 3,36 lít H2 (đktc) và dung dịch Y. Trộn dung dịch X với dung dịch Y đến phản ứng hoàn toàn thì thu được m gam kết tủa. Giá trị m là?
A. 7,8.
B. 3,9.
C. 35,1.
D. 31,2.
Cho 175 ml dung dịch Ba(OH)2 1M vào 100 ml dung dịch Mg(HCO3)2 1M. Sau phản ứng hoàn toàn, thu được m gam kết tủa.
a. Viết phương trình hóa học của các phản ứng.
b. Tìm giá trị của m.
Ba(OH)2 + Mg(HCO3)2 → BaCO3↓ + MgCO3↓ + 2H2O
0,1 ← 0,1
Dư: 0,075
Câu 3. (3 điểm) Hoà tan hoàn toàn 13,5 gam CuCl2 với 200 gam dung dịch NaOH 2,5%. Sau phản ứng thu được dung dịch X và kết tủa Y. Nung kết tủa Y đến khi khối lượng không đổi thu được m gam chất rắn .
a) Viết các phương trình hoá học xảy ra và nêu hiện tượng?
b) Tính m?
c) Tính nồng độ phần trăm của các chất có trong dung dịch X?
bạn xem lại xem 13.5(g) hay 13.8g nhé ^^ ,cho tròn số ý mà
CuCl2+2NaOH->Cu(OH)2+2NaCl
nCuCl2=13.5:138=0.1(mol)
nNaOH=20:40=0.5(mol)
theo pthh:nNaOH=2nCuCl2
theo bài ra,nNaOH=5 nCuCl2->NaOH dư tính theo CuCl2
theo pthh,nCu(OH)2=nCuCl2->nCu(OH)2=0.1(mol)
mCu(OH)2=0.1*98=9.8(g)
b)PTHH:Cu(OH)2+2HCl->CuCl2+2H2O
theo pthh:nHCl=2nCu(OH)2->nHCl=0.1*2=0.2(mol)
mHCl=0.2*36.5=7.3(g)
mDD HCl=7.3*100:10=73(g)
\(a,PTHH:CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2\downarrow+2NaCl\\ Cu\left(OH\right)_2\rightarrow^{t^o}CuO+H_2O\)
Hiện tượng: Dung dịch màu xanh nhạt dần, xuất hiện kết tủa màu xanh lơ
Phản ứng phân hủy Cu(OH)2 sinh ra chất rắn CuO màu đen và nước
\(b,n_{CuCl_2}=\dfrac{13,5}{135}=0,1\left(mol\right)\\ m_{NaOH}=\dfrac{200\cdot2,5\%}{100\%}=5\left(g\right)\\ \Rightarrow n_{NaOH}=\dfrac{5}{40}=0,125\left(mol\right)\)
Vì \(\dfrac{n_{CuCl_2}}{1}>\dfrac{n_{NaOH}}{2}\) nên CuCl2 dư
\(\Rightarrow\dfrac{1}{2}n_{NaOH}=n_{Cu\left(OH\right)_2}=n_{CuO}=0,0625\left(mol\right)\\ \Rightarrow m=m_{CuO}=0,0625\cdot80=5\left(g\right)\)
\(c,n_{NaCl}=n_{NaOH}=0,125\left(mol\right)\\ \Rightarrow m_{NaCl}=0,125\cdot58,5=7,3125\left(g\right)\\ m_{Cu\left(OH\right)_2}=0,0625\cdot98=6,125\left(g\right)\\ \Rightarrow m_{dd_{Cu\left(OH\right)_2}}=13,5+200-7,3125=206,1875\left(g\right)\\ \Rightarrow C\%_{Cu\left(OH\right)_2}=\dfrac{6,125}{206,1875}\cdot100\%\approx2,97\%\)
Sục V lít CO2 ở (đktc) vào 300ml dung dịch hỗn hợp NaOH 1M và Ba(OH)2 1M, đến phản ứng hoàn toàn thu được dung dịch X và m gam kết tủa. Cho dung dịch BaCl2 vào dung dịch X thu được kết tủa. Trong các giá trị sau của V, giá trị nào thoả mãn?
A. 20,16
B. 11,25
C. 13,44.
D. 6,72.
Đáp án B
Ta có :
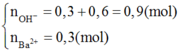
Vì cho BaCl2 vào X có kết tủa nên X có dư
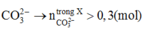
Tất nhiên ta có thể thử đáp án. Tuy nhiên, tôi sẽ biện luận với 2 trường hợp có thể xảy ra với X vẫn thỏa mãn đầu bài là :
+ Nếu X chỉ chứa
![]()
![]()
+ Nếu X chứa
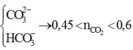
![]()
Sục V lít CO2 ở (đktc) vào 300ml dung dịch hỗn hợp NaOH 1M và Ba(OH)2 1M, đến phản ứng hoàn toàn thu được dung dịch X và m gam kết tủa. Cho dung dịch BaCl2 vào dung dịch X thu được kết tủa. Trong các giá trị sau của V, giá trị nào thoả mãn?
A. 20,16
B. 11,25.
C. 13,44.
D. 6,72.


| CHÚ Ý |
| Với bài toán sục khí CO2 vào dung dịch kiềm. Nếu quá trình tạo muối có sinh ra dưới dạng muối tan và kết tủa. Ví dụ như BaCO3 và Na2CO3 thì khi tiếp tục sục khí CO2 vào thì Na2CO3 sẽ phản ứng với CO2 trước. Khi hết Na2CO3 rồi thì kết tủa BaCCO3 mới bị hòa tan. |
Trộn 400 ml dung dịch NaOH 1M với 100 ml dung dịch FeCl3 1M thu được m gam kết tủa và dung
dịch X.
1.Viết phương trình phản ứng? Tính m?
2.Tính nồng độ mol của mỗi chất trong dung dịch X?
\(n_{NaOH}=1.0,4=0,4(mol);n_{FeCl_3}=1.0,1=0,1(mol)\\ a,PTHH:3NaOH+FeCl_3\to Fe(OH)_3\downarrow+3NaCl\\ \text {Vì }\dfrac{n_{NaOH}}{3}>\dfrac{n_{FeCl_3}}{1} \text {nên }NaOH\text { dư}\\ \Rightarrow n_{Fe(OH)_3}=0,1(mol)\\ \Rightarrow m_{Fe(OH)_3}=107.0,1=10,7(g)\\ b,n_{NaCl}=3n_{FeCl_3}=0,3(mol)\\ \Rightarrow C_{M_{NaCl}}=\dfrac{0,3}{0,4+0,1}=0,6M\)