gt đốt 2g Zn trong không khí hỏi kl của Zn tăng hay giảm khi pư xảy ra
giải giúp em với nhé mọi người
thầy ơi giải giúp e câu này với: cho Zn tới dư vào dd gồm HCl;0.05 mol NaNO3 0.1 mol KNO3. sau khi
pư kết thúc thu đc dd X chứa m gam muối ;0.125 hh 2 khí Y gồm 2 khí không màu trong đó 1 khí hóa nâu trong không khí
.tỉ khối hơi của y so với H2 là 12.2. a: tính khối lượng zn đã tham gia pư b: tính (m) sau khi pư kết thúc
Hỗn hợp khí Y gồm H2 (x mol) và NO (y mol, hóa nâu trong kk).
Ta có: x + y = 0,125 mol và 2x + 30y = 12,2.2.0,125 = 3,05. Giải hệ thu được: x = 0,025 và y = 0,1 mol.
Zn + 2HCl ---> ZnCl2 + H2 (1)
x x x
3Zn + 8H+ + 2NO3- ---> 3Zn2+ + 2NO + 4H2O (2)
1,5y 1,5y y
a) Số mol Zn đã tham gia phản ứng = x + 1,5y = 0,175 mol. Khối lượng Zn = 65.0,175 = 11,375 gam.
b) Muối sau phản ứng gồm ZnCl2 (x mol) và Zn(NO3)2 (=số 1/2 số mol NO3- = 0,075 mol). Nên m = 135.0,025 + 189.0,075 = 17,55 gam.
Giúp mk với mk đang cần gấp ạ Nhúng 1 thanh Zn vào 500ml dd AgNo3 2M. Sau pư thấy KL thanh Zn giảm 4,4g. Tính CM AgNo3 và CM Zn(No3)2 tạo thành. Biết thể tích sau dd pư k thay đổi.
n CuSO4 (bđ) = 0,4 . 0,5 = 0,2 (mol)
2Al + 3CuSO4 →→ Al2(SO4)3 + 3Cu
Cứ 1 mol Cu tạo thành thì khối lượng CR tăng 138g
0,01 mol ←← (11,38 - 10 ) g
mCu= 0,01 . 64 = 0,64 (g)
2Al + 3CuSO4 →→ Al2(SO4)3 + 3Cu
0,01 ←← 13001300 ←← 0,01 (mol)
Sau pư thể tích dd ko đổi => V = 0,5 l
CM(CuSO4)= 0,2−0,010,50,2−0,010,5= 0,38 (M)
CM(Al2(SO4)3)= 13000,513000,5 = 0,007(M)
Thầy cho em hỏi 2 ý của vấn đề ăn mòn kim loại: 2 trường hợp dưới đây có xảy ra ăn mòn điện hóa?
- Cho hỗn hợp Zn, Cu tác dụng với khí Cl2
( nếu Zn + Cl2 ----> dung dịch ZnCl2 là dung dịch chất điện ly thì có ăn mòn đúng không ạ. Hay cần phải nói thêm
là Cu tiếp xúc trực tiếp với Zn hoặc nối dây thì mới ăn mòn điện hóa ạ?)
- Cho miếng gang (Fe,C) vào khí HCl (trong không khí ẩm thì gang bị ăn mòn, còn trong axit thì gang có bị không ạ?)
em cảm ơn thầy!
Điều kiện để xảy ra ăn mòn điện hóa là:
1) Các điện cực phải khác nhau.Ví dụ như Fe và Zn. Kim loại mạnh là cực âm và bị ăn mòn nhanh chóng
2) Các điện cực phải tiếp xúc với nhau (có thể trực tiếp hoặc gián tiếp qua dây dẫn) và cùng tiếp xúc với môi trường điện ly
Trường hợp thứ nhất của em, không phải là ăn mòn điện hóa vì không nói rõ Cu, Zn có tiếp xúc với nhau hay không, hơn nữa khí Cl2 thì không thể tạo ra dung dịch điện ly được.
Trường hợp thứ 2 cũng vậy, vì HCl là khí thì cũng không có dung dịch điện ly để xảy ra ăn mòn điện hóa, nếu là dung dịch HCl thì sẽ là ăn mòn điện hóa.
Đốt bột Zn trong không khí, sau khi kết thúc phản ứng, người ta cho vào hỗn hợp một lượng dư dung dịch HCl thì thấy có khí H 2 thoát ra.
Viết các phương trình hóa học đã xảy ra
Ngâm một lá Zn trong 100ml dung dịch AgNO3 0,1M, sau đó lấy thanh Zn ra rồi cho tiếp dung dịch HCl vào dung dịch vừa thu được thì không thấy hiện tượng gì. Hỏi khối lượng lá Zn tăng hay giảm bao nhiêu gam so với ban đầu:
A. Tăng 0,755g.
B. Giảm 0,567g.
C. Tăng 2,16g.
D. Tăng 1,08g.
Đáp án A
Vì khi cho HCl vào dung dịch vừa thu được không thấy hiện tượng gì nên trong dung dịch không còn Ag+
![]()
Do đó Ag+ đã phản ứng hết với Zn.
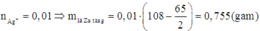
Cho m gam hỗn hợp kim loại Zn, Cu vào dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được 4,48 lít khí H2 (đktc) và 2g kim loại không tan. Giá trị của m là
A. 8,5.
B. 18.
C. 15.
D. 16.
Đáp án C
nZn = nH2 = 0,2 => m = mZn + mCu = 0,2.65 +2 = 15 => Chọn C.
Cho m gam hỗn hợp kim loại Zn, Cu vào dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được 4,48 lít khí H2 (đktc) và 2g kim loại không tan. Giá trị của m là
A. 8,5.
B. 18.
C. 15.
D. 16.
Đáp án C
nZn = nH2 = 0,2 => m = mZn + mCu = 0,2.65 +2 = 15 => Chọn C.
Cho m gam hỗn hợp kim loại Zn, Cu vào dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được 4,48 lít khí H2 (đktc) và 2g kim loại không tan. Giá trị của m là
A. 8,5.
B. 18.
C. 15.
D. 16
Chọn C
nZn = nH2 = 0,2 ⇒ m = mZn + mCu = 0,2.65 +2 = 15
cho 6,5g Zn tác dụng với dung dịch HCl dư. thu đc muối kẽm clorua ZnCl2 và khí H2
a) Viết PTHH PƯ xảy ra?
b)tính khối lượng HCl sau PƯ
c) dẫn toàn bộ lượng khí hidro trên tác dụng hết với bột đồng II oxit CuO ở nhiệt độ cao. tính khối lượng kl đồng Cu thu đc sau pư.
nZn = 6,5 : 65 = 0,1 (mol)
pthh: Zn+2HCl -> ZnCl2 + H2
0,1 0,1 0,1
=> mHCl = 0,1 . 36,5 = 3,65(g)
pthh : CuO + H2 -to-> Cu + H2O
0,1 0,1
=> mCu = 0,1 . 64 = 6,4 (g)