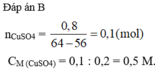Cho đinh sắt 4 vào dung dịch CuSO4 1M sau khi phản ứng sảy ra hoàn toàn với đinh sắt 4,16g . Tính mFe phản ứng, mCu sinh ra, V dung dịch CuSO4 cần dùng

Những câu hỏi liên quan
Ngâm một đinh sắt trong 200 ml dung dịch CuSO4 xM. Sau khi phản ứng xảy ra hoàn toàn, lấy đinh sắt ra khỏi dung dịch, rửa nhẹ, làm khô thấy khối lượng đinh sắt tăng thêm 1,6 gam. Giả sử tất cả lượng Cu sinh ra đều bám vào đinh sắt. Giá trị của x là A. 1,0. B. 2,0. C. 1,5. D. 0,5.
Đọc tiếp
Ngâm một đinh sắt trong 200 ml dung dịch CuSO4 xM. Sau khi phản ứng xảy ra hoàn toàn, lấy đinh sắt ra khỏi dung dịch, rửa nhẹ, làm khô thấy khối lượng đinh sắt tăng thêm 1,6 gam. Giả sử tất cả lượng Cu sinh ra đều bám vào đinh sắt. Giá trị của x là
A. 1,0.
B. 2,0.
C. 1,5.
D. 0,5.
Ngâm một đinh sắt đã được đánh sạch bề mặt vào 100 ml dung dịch CuSO4. Sau khi phản ứng hoàn toàn, lấy đinh sắt ra rửa nhẹ, sấy khô thấy khối lượng đinh sắt tăng thêm 1,6gam. Nồng độ mol ban đầu của dung dịch CuSO4 là: A. 1M B. 2M C. 3M D. 4M
Đọc tiếp
Ngâm một đinh sắt đã được đánh sạch bề mặt vào 100 ml dung dịch CuSO4. Sau khi phản ứng hoàn toàn, lấy đinh sắt ra rửa nhẹ, sấy khô thấy khối lượng đinh sắt tăng thêm 1,6gam. Nồng độ mol ban đầu của dung dịch CuSO4 là:
A. 1M
B. 2M
C. 3M
D. 4M
Đáp án B
Fe + Cu2+ → Fe2+ + Cu
Mol x → x
=> DmThanh KL(tăng) = mCu – mFe pứ = 64x – 56x = 1,6
=> x = 0,2 mol => nCuSO4 = nCu = 0,2 mol
=> CM(CuSO4) = 0,2 : 0,1 = 2M
Đúng 0
Bình luận (0)
Ngâm một đinh sắt trong 200ml dung dịch CuSO4 x(M). Sau khi phản ứng hoàn toàn, lấy đinh sắt ra khỏi dung dịch, rửa nhẹ, làm khô thấy khối lượng đinh sắt tăng thêm 3,2 gam. Giả sử tất cả lượng Cu sinh ra đều bám hết vào đinh sắt. Giá trị của x là A. 1,0 B. 1,5 C. 2,0 D. 0,5
Đọc tiếp
Ngâm một đinh sắt trong 200ml dung dịch CuSO4 x(M). Sau khi phản ứng hoàn toàn, lấy đinh sắt ra khỏi dung dịch, rửa nhẹ, làm khô thấy khối lượng đinh sắt tăng thêm 3,2 gam. Giả sử tất cả lượng Cu sinh ra đều bám hết vào đinh sắt. Giá trị của x là
A. 1,0
B. 1,5
C. 2,0
D. 0,5
Ngâm một đinh sắt trong 200ml dung dịch CuSO4 x(M). Sau khi phản ứng hoàn toàn, lấy đinh sắt ra khỏi dung dịch, rửa nhẹ, làm khô thấy khối lượng đinh sắt tăng thêm 3,2 gam. Giả sử tất cả lượng Cu sinh ra đều bám hết vào đinh sắt. Giá trị của x là A. 1,0. B. 1,5. C. 2,0. D. 0,5.
Đọc tiếp
Ngâm một đinh sắt trong 200ml dung dịch CuSO4 x(M). Sau khi phản ứng hoàn toàn, lấy đinh sắt ra khỏi dung dịch, rửa nhẹ, làm khô thấy khối lượng đinh sắt tăng thêm 3,2 gam. Giả sử tất cả lượng Cu sinh ra đều bám hết vào đinh sắt. Giá trị của x là
A. 1,0.
B. 1,5.
C. 2,0.
D. 0,5.
Ngâm một đinh sắt sạch trong 200 ml dung dịch
C
u
S
O
4
sau khi phản ứng kết thúc, lấy đinh sắt ra khỏi dung dịch rửa nhẹ làm khô nhận thấy khối lượng đinh sắt tăng thêm 0,8 gam. Nồng độ mol/lít của dung dịch
C
u
S
O
4
đã dùng là: A. 0,3M. B. 0,5M. C. 0,4M. D. 0,25M.
Đọc tiếp
Ngâm một đinh sắt sạch trong 200 ml dung dịch C u S O 4 sau khi phản ứng kết thúc, lấy đinh sắt ra khỏi dung dịch rửa nhẹ làm khô nhận thấy khối lượng đinh sắt tăng thêm 0,8 gam. Nồng độ mol/lít của dung dịch C u S O 4 đã dùng là:
A. 0,3M.
B. 0,5M.
C. 0,4M.
D. 0,25M.
Ngâm một đinh sắt sạch trong 200ml dung dịch
C
u
S
O
4
. Sau khi phản ứng kết thúc, lấy đinh sắt ra khỏi dung dịch rửa sạch nhẹ bằng nước cất và sấy khô rồi đem cân thấy khối lượng đinh sắt tăng 0,8 gam so với ban đầu. Nồng độ mol của dung dịch
C
u
S
O
4
đã dùng là giá trị nào dưới đây? A. 0,05M B. 0,0625M C. 0,50M D. 0,625M.
Đọc tiếp
Ngâm một đinh sắt sạch trong 200ml dung dịch C u S O 4 . Sau khi phản ứng kết thúc, lấy đinh sắt ra khỏi dung dịch rửa sạch nhẹ bằng nước cất và sấy khô rồi đem cân thấy khối lượng đinh sắt tăng 0,8 gam so với ban đầu. Nồng độ mol của dung dịch C u S O 4 đã dùng là giá trị nào dưới đây?
A. 0,05M
B. 0,0625M
C. 0,50M
D. 0,625M.
Gọi a là số mol C u S O 4 tham gia phản ứng
Phương trình hóa học:
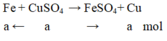
Theo đề bài ta có: m C u b á m v à o – m F e tan r a = m K L t ă n g
64a – 56a = 0,8 ⇒ a = 0,01 mol
Nồng độ dung dịch C u S O 4 là: C M = n V = 0,01 0,2 = 0,5 M
⇒ Chọn C.
Đúng 0
Bình luận (0)
Trong giờ thực hành hóa học, một học sinh nhúng một đinh sắt vào dung dịch muối đồng sunfat
C
u
S
O
4
. Sau một thời gian, lấy đinh sắt ra khỏi dung dịch muối. Thanh sắt bị phủ một lớp màu đỏ gạch và dung dịch có muối sắt (II) sunfat
F
e
S
O
4
. Hãy cho biết phản ứng trên thuộc loại phản ứng nào?
Đọc tiếp
Trong giờ thực hành hóa học, một học sinh nhúng một đinh sắt vào dung dịch muối đồng sunfat C u S O 4 . Sau một thời gian, lấy đinh sắt ra khỏi dung dịch muối. Thanh sắt bị phủ một lớp màu đỏ gạch và dung dịch có muối sắt (II) sunfat F e S O 4 . Hãy cho biết phản ứng trên thuộc loại phản ứng nào?
Câu 3: Cho đinh sắt sạch, dư vào V ml dung dịch CuSO4 0,5 M. Khi phản ứng kết thúc, thấy có 6,4 gam kim loại Cu bám vào đinh sắt. Biết toàn bộ kim loại Cu tạo thành đều bám vào đinh sắt và thể tích dung dịch không thay đổi. a. Tính khối lượng của sắt đã tham gia phản ứng và giá trị của V? b. Tính nồng độ mol/l của dung dịch sau phản ứng?
\(n_{CuSO_4}=n_{Cu}=\dfrac{6,4}{64}=0,1\left(mol\right)\)
\(V_{CuSO_4}=\dfrac{n}{C_M}=\dfrac{0,1}{0,5}=0,2\left(l\right)\)
PTHH :
Fe + CuSO4 --> FeSO4 + Cu
0,1 0,1 0,1 0,1
\(m_{Fe}=0,1.56=5,6\left(g\right)\)
\(b,\) \(C_{M\left(FeSO_4\right)}=\dfrac{n}{V}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
Đúng 2
Bình luận (0)
\(Fe+CuSO_4=FeSO_4+Cu\)
\(0,1\left(mol\right)\) \(0,1\left(mol\right)\) \(0,1\left(mol\right)\)
Số mol Đồng : \(n_{Cu}=\dfrac{m}{M}=\dfrac{6,4}{64}=0,1\left(mol\right)\)
Khối lượng Sắt đã tham gia phản ứng :
\(m_{Fe}=n_{Fe}.M=0,1.56=5,6\left(g\right)\)
Thể tích dung dịch \(CuSO_4\)
\(C_M=\dfrac{n}{V}\Rightarrow V=n.V=0,1.0,5=0,05\left(l\right)=50\left(ml\right)\)
Dựa vào phương trình phản ứng \(n_{FeSO_4}=0,1\left(mol\right)\)
Nồng độ dung dịch sau phản ứng :
\(C_M=\dfrac{n_{FeSO_4}}{V}=\dfrac{0,1}{0,05}=2\left(M\right)\)
Đúng 1
Bình luận (1)
ngâm đinh sắt nặng 50g vào dung dịch cuso4 1m. phản ứng xong thấy khối lượng đinh sắt nặng 51,6g.
a)tính thể tích dd cuso4.
b)tính khối lượng muối tạo thành.