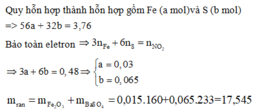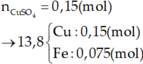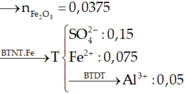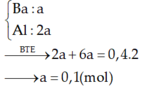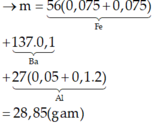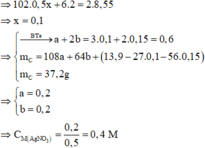Cho X là hỗn hợp của 3 chất gồm kim loại M, oxit và muối sunfat của kim loại M. Biết M có hóa trị II không đổi trong các hợp chất. Chia 29,6 gam X thành hai phần bằng nhau: – Phần 1: đem hòa tan tỏng dung dịch H2SO4loãng dư thu được dung dịch A, khí B. Lượng khí B này vừa đủ để khử hết 16 gam CuO. Sau đó cho dung dịch A tác dụng với dung dịch KOH dư, đến khi kết thúc phản ứng thu được kết tủa C. Nung C đến khối lượng không đổi thì thu được 14 gam chất rắn. – Phần 2: cho tác dụng với 200 ml dung...
Đọc tiếp
Cho X là hỗn hợp của 3 chất gồm kim loại M, oxit và muối sunfat của kim loại M. Biết M có hóa trị II không đổi trong các hợp chất. Chia 29,6 gam X thành hai phần bằng nhau:
– Phần 1: đem hòa tan tỏng dung dịch H2SO4loãng dư thu được dung dịch A, khí B. Lượng khí B này vừa đủ để khử hết 16 gam CuO. Sau đó cho dung dịch A tác dụng với dung dịch KOH dư, đến khi kết thúc phản ứng thu được kết tủa C. Nung C đến khối lượng không đổi thì thu được 14 gam chất rắn.
– Phần 2: cho tác dụng với 200 ml dung dịch CuSO4 1,5M. Sau khi kết thúc phản ứng tách bỏ chất rắn, cô cạn phần dung dịch thì thu được 46 gam muối khan.
a) Viết phương trình phản ứng xảy ra và xác định kim loại M.
b) Tính phần trăm khối lượng các chất trong X.