Trộn 300ml dung dịch CuCl2 0,2M với 200ml dung dịch AgNO3 0,7M
a) Tính khối lượng kết tủa
b) Tính nồng độ dung dịch thu được.
Giúp mình với!
Cảm ơn nhiều.
Trộn 200ml dung dịch CuCl2 với 300ml dung dịch NaOH có nồng độ 0.2M sau phản ứng lọc kết tủa và nung khối lượng không đổi a, viết phương trình phản ứng xảy ra b, tính khối lượng chất rắn thu được sau khi nung c, tính nồng độ mol dung dịch sau phản ứng
Trộn 200ml dung dịch cucl2 với 300ml dung dich naoh có nồng độ 0.2M .Sau phản ứng lọc kết tủa mang khối lượng không đổi
a) Viết Pt
b)Tính khối lượng chất rắn thu được sau phản ứng
c)Tính nồng độ mol các chất trong dung dịch phản ứng
Trộn 300ml dung dịch AgNO3 0,5M với 100ml dung dịch hỗn hợp KCl 0,2M và CuCl2 0,2M. khối lượng kết tủa là ?
\(n_{AgNO3}=0,5.0,3=0,15\left(mol\right)\)
\(n_{KCl}=0,2.0,1=0,02\left(mol\right)\)
\(n_{CuCL2}=0,2.0,1=0,02\left(mol\right)\)
\(PTH:AgNO_3+KCl\rightarrow AgCl+KNO_3\)
______ 0,02________0,02__0,02____________
Tỉ lệ :\(\frac{0,15}{1}>\frac{0,02}{1}\)
Nên KCl hết, AgNO3 dư, pt tính theo số mol KCl
\(\Rightarrow m_{AgCl}=0,02.\left(108+35,5\right)=2,87\left(g\right)\)
\(\Rightarrow n_{AgNO3+dư}=0,15-0,02=0,13\left(mol\right)\)
\(PTHH:2AgNO_3+CuCl_2\rightarrow2AgCl+Cu\left(NO_3\right)_2\)
______0,04 _________0,02_____ 0,04______________
Tỉ lệ :\(\frac{0,13}{2}>\frac{0,02}{1}\)
Nên AgNO3 còn dư, CuCl2 phản ứng hết, pt tính theo nCuCl2
\(\Rightarrow m_{AgCl}=0,04.\left(108+35,5\right)=5,74\left(g\right)\)
\(\Rightarrow\Sigma m_{AgCl}=2,87+5,74=8,61\left(g\right)\)
cho 200ml dung dịch H3PO4 tác dụng hết với 300ml dung dịch ZnCl2 2Ma, Viết PTHH xảy ra
b, Tính khối lượng kết tủa thu đc
c, Tách bỏ kết tủa. Tính nồng độ M của dung dịch thu được
PTHH 3ZnCl2+2H3PO4----->Zn3(PO4)2+6HCl
\(n_{ZnCl_2}\)=0,3.2=0,6(mol)
Theo phương trình =>\(\dfrac{1}{3}n_{ZnCl_2}=n_{Zn_3\left(PO_4\right)_2}=0,2\left(mol\right)\)
=>\(m_{Zn_3\left(PO_4\right)_2}\)=0,2.385=77(g)
Theo phương trình =>\(2n_{ZnCl_2}=n_{HCl}=1,2\left(mol\right)\)
=>\(C_{M_{HCl}}\)=\(\dfrac{1,2}{0,2+0,3}=2,4M\)
Trộn 200 ml dung Fe2(SO4)3 0,015M với 300ml dung dịch BaCl2 0,01M thu được 500ml dung dịch A. Tính khối lượng kết tủa thu được và nồng độ các ion trong dung dịch A.
X là dung dịch Al2(SO4)3, Y là dung dịch Ba(OH)2. Trộn 200ml dung dịch X với 300ml dung dịch Y thu được 8,55 gam kết tủa. Trộn 200ml dung dịch X với 500ml dung dịch Y thu được 12,045 gam kết tủa. Nồng độ mol/l của dung dịch X là
A. 0,075M
B. 0,100M
C. 0.150M
D. 0.050M
trộn 300ml dung dịch hỗn hợp KCl 0,2M: NaCl 0,3M và FeCl3 0,1M với lượng dư dung dịch AgNO3. khối lượng kết tủa thu được là ?
\(\Sigma CM_{hh}=0,6M\)
\(\Rightarrow n_{hh}=0,18\left(mol\right)\)
Bao toàn Cl
\(5n_{Cl\left(hh\right)}=2n_{Cl\left(kt\right)}=\frac{0,18.5}{3}=0,3\left(mol\right)\)
\(\Rightarrow m_{AgCl}=43,05\left(g\right)\)
Cho 300ml một dung dịch có hòa tan 5,85g NaCl tác dụng với 200ml dung dịch có hòa tan 34g AgNO3, người ta thu được một kết tủa và nước lọc.
a) Tính khối lượng chất kết tủa thu được.
b) Tính nồng độ mol chất còn lại trong nước lọc. Cho rằng thể tích nước lọc thu được không thay đổi đáng kể
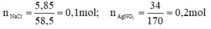
a) Phương trình hóa học của phản ứng:
NaCl + AgNO3 → AgCl↓ + NaNO3
Theo pt: nAgNO3 pư = nAgCl = nNaCl = 0,1 mol
b) Vdd = 300 + 200 = 500 ml
nAgNO3 dư = 0,2 – 0, 1 = 0,1 mol; nNaNO3 = nNaCl = 0,1 mol
CM(NaNO3) = CM(AgNO3) = 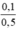 = 0,2 mol/l.
= 0,2 mol/l.
X là dung dịch Al2(SO4)3, Y là dung dịch Ba(OH)2. Trộn 200ml dung dịch X với 300ml dung dịch Y thu được 8,55 gam kết tủa. Trộn 200 ml dung dịch X với 500 ml dung dịch Y thu được 12,045 gam kết tủa. Nồng độ mol/l của dung dịch X là:
A. 0,075M
B. 0,100M
C. 0,150M
D. 0,050M.