d) X có số khối là 37 và số p kém lần số e là 3 hạt
Nguyên tử Y có số khối bằng 37 trong đó số hạt ko mang điện là 14 hạt Xác định p n e
Nguyên tử R có tổng số hạt là 58 tỉ số giữa nơtron và số khối là 11/20 Xác định p n e
nguyên tử Y : số khối A= p+n =37
số hạt không mang điện là n= 14 => p=23 =e
nguyên tử R có tổng hạt = 2p + n = 58
tỷ số giữa notron và số khối = n/ A = 11/20 =>\(\frac{n}{p+n}\)=\(\frac{11}{20}\) giải 2 pt trên bạn tìm ra n và p nhé
Tìm số proton,notron, electron và số khối của các nguyên tử sau : a) X có tổng số hạt là 18, số p= số n b)Y có số khối là 27 và số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt c)Z có số khối là 35, số proton kém số notron 1 hạt
Tìm số proton,notron, electron và số khối của các nguyên tử sau :
a) X có tổng số hạt là 18, số p= số n
\(\left\{{}\begin{matrix}2Z+N=18\\Z=N\end{matrix}\right.\)
=> Z=P=E=6
N=6
b)Y có số khối là 27 và số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt
\(\left\{{}\begin{matrix}Z+N=A=27\\2Z-N=12\end{matrix}\right.\)
=> Z=P=E= 13
N=14
c)Z có số khối là 35, số proton kém số notron 1 hạt
\(\left\{{}\begin{matrix}Z+N=A=35\\N-Z=1\end{matrix}\right.\)
=> Z=P=E= 17
N=18
a) S=P+E+N
P=E=N
=>P=E=N=18/3=6
=> A= P+N=6+6=12
=> Nguyên tử X có 6p,6e,6n. Số khối 12.
b) Nguyên tử Y:
A=P+N=27
Mặt khác:2P-N=12
=> Ta tìm được: P=E=13; N=14
=> Nguyên tử Y có 13p,13e,14n và số khối là 27.
c) Nguyên tử Z:
A=P+N=35
N=P+1
Ta tìm được: P=E=17; N=18
=> Nguyên tử Z có 17p,17e,18n và số khối là 35
Bài 3: Nguyên tử Z có tổng số hạt e, p, n là 54 và số khối là 37. Tìm Z và viết kí hiệu
nguyên tử Z.
\(\left\{{}\begin{matrix}P+N+E=54\\P+N=37\\P=E\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2P+N=54\\P+N=37\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P=E=Z=17\\N=20\end{matrix}\right.\\ \Rightarrow A=Z+N=17+20=37\left(đ.v.C\right)\\ \Rightarrow KH:^{37}_{17}Cl\)
Chúc em học tốt nha!
Nguyên tử X có tổng số hạt p, n, e là 34 và số khối là 23. Số lớp và số e lớp ngoài cùng lần lượt là
A. 3 và 1
B. 2 và 1
C. 4 và 1
D. 1 và 3

Khi đó X có cấu hình electron là 1s22s22p23s1.
Vậy số electron ngoài cùng của X là 1 và số lớp electron của X là 3.
Đáp án A
Nguyên tử X có tổng số hạt p, n, e là 34 và số khối là 23. Số lớp và số e lớp ngoài cùng lần lượt là
A. 3 và 1
B. 2 và 1
C. 4 và 1
D. 1 và 3
Đáp án A
Có hệ 2 Z + N = 34 Z + N = 23 ⇒ Z = 11 N = 12
Khi đó X có cấu hình electron là 1s22s22p23s1.
Vậy số electron ngoài cùng của X là 1 và số lớp electron của X là 3.
Hợp chất MX2 được tạo từ ion M2+ và X- có tổng số hạt cơ bản (p, n, e) là 186, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 54 hạt. Biết số hạt e trong ion M2+ nhiều hơn trong ion X- là 6 hạt và số khối của ion M2+ gấp 1,6 lần số khối của ion X-. Nhận xét nào sau đây về hợp chất MX2 là đúng?
A. Phản ứng được với dung dịch AgNO3 trong NH3 dư thu được kết tủa.
B. Hợp chất MX2 là muối axit, trong dung dịch làm quỳ tím chuyển thành màu hồng.
C. Hợp chất MX2 là chất điện li yếu.
D. Trong phản ứng oxi hóa khử, MX2 chỉ đóng vai trò là chất oxi hóa.
Bài toán không đơn thuần chỉ là tìm ra chất mà còn tích hợp cả kiến thức về tính chất hóa học của các chất. Nếu tìm được chất mà không nắm chắc tính chất hóa học của chất đó thì quá trình tìm chất trở nên vô nghĩa. Vì vậy để làm được bài này các bạn cần phải nắm chắc kiến thức về tính chất hóa học của các chất.
Gọi lần lượt là số proton, nơtron của M và X.
Theo giả thiết ta có:
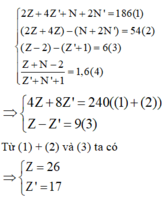
M là Fe và X là Cl.
Vậy hợp chất cần tìm là FeCl2
Xét các đáp án:
A: Đúng: kết tủa là AgCl
B: Sai: Dung dịch muối FeCl2 không làm thay đổi màu quỳ tím
C: Sai: FeCl2 là chất điện li mạnh
D: Sai: FeCl2 vừa thể hiện tính oxi hóa vừa thể hiện tính khử do Fe ở trạng thái oxi hóa trung gian
Đáp án A.
Hợp chất M2X có tổng số các hạt trong phân tử là 116, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 36. Khối lượng nguyên tử X lớn hơn M là 9. Tổng số hạt (p, n, e) trong X2- nhiều hơn trong M+ là 17 hạt. Số khối của M và X lần lượt là
A. 21 và 31.
B. 23 và 32.
C. 23 và 34.
D. 40 và 33.
Hợp chất M2X có tổng số các hạt trong phân tử là 116, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 36. Khối lượng nguyên tử X lớn hơn M là 9. Tổng số hạt (p, n, e) trong X2- nhiều hơn trong M+ là 17 hạt. Số khối của M và X lần lượt là
A. 21 và 31.
B. 23 và 32.
C. 23 và 34.
D. 40 và 33.
Nguyên tử X có tổng số hạt cơ bản là 10, biết số hạt n < số hạt e và nhỏ hơn 1,5 lần số hạt e
a, Xác định hạt p,n,e
b, tính khối lượng nguyên tử
c, Cho biết số e lớp ngoài cùng của X