Trộn 150g dung dịch Ba(OH)2 17,1% với 250g dung dịch FeSO4 15,2% đến phản ứng hoàn toàn thu được m gam kết tủa và dung dịch Y. Tính m và nồng độ phần trăm của dung dịch Y

Những câu hỏi liên quan
Hấp thụ hoàn toàn 5,6 lít CO2 vào dung dịch 85,5 gam dung dịch Ba(OH)2. Sau phản ứng lọc tách kết tủa thu được dung dịch có khối lượng 39,95 gam. Tính nồng độ phần trăm của dung dịch Ba(OH)2
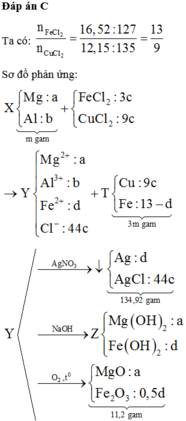
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch chứa FeCl2 16,51% và CuCl2 12,15%. Sau phản ứng, thu được 3m gam hỗn hợp kim loại và dung dịch Y. Cho Y phản ứng hoàn toàn với dung dịch AgNO3 dư, thu được 134,92 gam kết tủa. Mặt khác, cho Y phản ứng hoàn toàn với dung dịch NaOH dư, thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được 11,2 gam hỗn hợp rắn. Bỏ qua sự thủy phân của muối trong dung dịch. Nồng độ phần trăm của AlCl3 trong Y là A. 10,31%. B. 8,63%. C. 11,51%....
Đọc tiếp
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch chứa FeCl2 16,51% và CuCl2 12,15%. Sau phản ứng, thu được 3m gam hỗn hợp kim loại và dung dịch Y. Cho Y phản ứng hoàn toàn với dung dịch AgNO3 dư, thu được 134,92 gam kết tủa. Mặt khác, cho Y phản ứng hoàn toàn với dung dịch NaOH dư, thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được 11,2 gam hỗn hợp rắn. Bỏ qua sự thủy phân của muối trong dung dịch. Nồng độ phần trăm của AlCl3 trong Y là
A. 10,31%.
B. 8,63%.
C. 11,51%.
D. 8,45%.
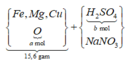
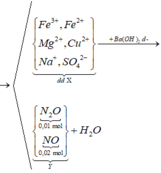
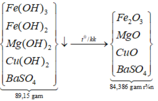
Hòa tan hoàn toàn 15,6 gam hỗn hợp Fe, Fe3O4, Fe2O3, Mg, MgO và CuO vào 200 gam dung dịch H2SO4 và NaNO3 thu được dung dịch X chỉ chứa muối sunfat trung hòa của kim loại, hỗn hợp khí Y gòm 0,01 mol N2O và 0,02 mol NO. Cho X phản ứng với dung dịch Ba(OH)2 dư, thu được 89,15 gam kết tủa. Lọc kết tủa nung trong không khí đến khối lượng không đổi, thu được 84,386 gam chất rắn. Nồng độ phần trăm của FeSO4 trong X có giá trị gần nhất với giá trị nào sau đây? A. 0,85. B. 1,06. C. 1,45. D. 1,86.
Đọc tiếp
Hòa tan hoàn toàn 15,6 gam hỗn hợp Fe, Fe3O4, Fe2O3, Mg, MgO và CuO vào 200 gam dung dịch H2SO4 và NaNO3 thu được dung dịch X chỉ chứa muối sunfat trung hòa của kim loại, hỗn hợp khí Y gòm 0,01 mol N2O và 0,02 mol NO. Cho X phản ứng với dung dịch Ba(OH)2 dư, thu được 89,15 gam kết tủa. Lọc kết tủa nung trong không khí đến khối lượng không đổi, thu được 84,386 gam chất rắn. Nồng độ phần trăm của FeSO4 trong X có giá trị gần nhất với giá trị nào sau đây?
A. 0,85.
B. 1,06.
C. 1,45.
D. 1,86.
Đặt khối lượng kim loại trong hỗn hợp ban đầu là m gam; số mol O trong hoonx hợp ban đầu là a mol; số mol H2SO4 là b mol.
![]()
Sơ đồ phản ứng:
![]()
![]()
Các quá trình tham gia phản ứng của H+: 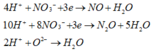
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
*Xét giai đoạn nung kết tủa đến khối lượng không đổi:
Sơ đồ phản ứng:
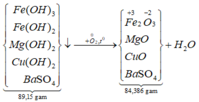
![]()
![]()
![]()
![]()
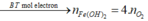
![]()
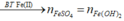
![]()
![]()
![]()
![]() = 85%.
= 85%.
Đáp án A.
Đúng 0
Bình luận (0)
Trộn đều 60,38 gam hỗn hợp X gồm BaO, BaCO3, NaHCO3 rồi chia X thành hai phần bằng nhau. Phần 1 cho vào nước dư thu được 21,67 gam kết tủa. Phần 2 nung ở nhiệt độ cao đến khối lượng không đổi thu được 26,13 gam hỗn hợp chất rắn Y. Cho toàn bộ hỗn hợp chất rắn Y vào 79,78 gam nước thu được m gam kết tủa và dung dịch Z (nước bay hơi không đáng kể). Giả thiết các phản ứng đều xảy ra hoàn toàn. a) Tìm giá trị của m và tính nồng độ phần trăm của mỗi chất tan có trong dung dich Z b) Lấy 50 gam dung dị...
Đọc tiếp
Trộn đều 60,38 gam hỗn hợp X gồm BaO, BaCO3, NaHCO3 rồi chia X thành hai phần bằng nhau. Phần 1 cho vào nước dư thu được 21,67 gam kết tủa. Phần 2 nung ở nhiệt độ cao đến khối lượng không đổi thu được 26,13 gam hỗn hợp chất rắn Y. Cho toàn bộ hỗn hợp chất rắn Y vào 79,78 gam nước thu được m gam kết tủa và dung dịch Z (nước bay hơi không đáng kể). Giả thiết các phản ứng đều xảy ra hoàn toàn.
a) Tìm giá trị của m và tính nồng độ phần trăm của mỗi chất tan có trong dung dich Z
b) Lấy 50 gam dung dịch Z cho tác dụng với 50 gam dung dịch Al2(SO4)3 13,68% đến khi các phản ứng xảy ra hoàn toàn thu được x gam kết tủa và dung dịch T. Tìm giá trị của x.
Gọi số mol của BaO, BaCO3, NaHCO3 trong 30,19g hh lần lượt là x, y, z
Có 153x + 197y + 84z = 30,19
Phần 1:
BaO + H2O → Ba(OH)2
x x
OH- + HCO3- → CO32- + H2O
Ba2+ + CO32- → BaCO3
n kết tủa = 0,11
Phần 2:
BaCO3 →BaO + CO2
y y
2NaHCO3 → Na2CO3 + H2O + CO2
z z/2 z/2
=> mCO2 + mH2O = 30,19 – 26,13 = 4,06
=> 44 (y + z/2) + 18 . z/2= 4,06
TH1: Ba tạo kết tủa hoàn toàn thành BaCO3 và NaHCO3 dư
=> nBaCO3 = nBaCO3 + nBaO = 0,11 => Không thỏa mãn
TH2: Ba(OH)2 dư và NaHCO3 hết
=> x + y = 0,11 và y + z = 0,11
=> x = 0,1; y = 0,05 và z = 0,06
a.
hh Y gồm BaO: 0,15 mol; Na2CO3: 0,03 mol
BaO + H2O → Ba(OH)2
0,15 0,15
Ba(OH)2 + Na2CO3 → BaCO3 + 2NaOH
0,15 0,03 0,03 0,06
=> m kết tủa = 0,03 . 197 = 5,91g
m dd = m chất rắn + mH2O – mBaCO3 = 26,13 + 79,78 – 5,91 = 100
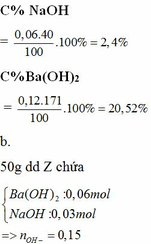
nAl2(SO4)3 = 0,02 => nAl3+ = 0,04; nSO42- = 0,06
Ba2+ + SO42- → BaSO4
0,06 0,06 0,06
nAl(OH)3 = 0,01 => mAl(OH)3 = 0,78g
m = 0,78 + 0,06 . 233 = 14,76g
Đúng 0
Bình luận (0)
Nung 21,69 gam hỗn hợp X gồm Al và Fe2O3 trong chân không đến phản ứng hoàn toàn, thu được hỗn hợp Y. Nghiền nhỏ, trộn đều rồi chia Y làm 2 phần: - Phần 1: Cho tác dụng với dung dịch NaOH dư, thu được 0,045 mol H2 và 3,36 gam chất rắn không tan. - Phần 2: Trộn với m gam KNO3 rồi hòa tan vào 100 gam dung dịch HCl, sau phản ứng thu được dung dịch T (chỉ chứa muối clorua) và hỗn hợp khí (gồm 0,12 mol NO, 0,03 mol H2). Cho T tác dụng với dung dịch AgNO3 dư, thu được 147,82 gam kết tủa. Nồng độ phần...
Đọc tiếp
Nung 21,69 gam hỗn hợp X gồm Al và Fe2O3 trong chân không đến phản ứng hoàn toàn, thu được hỗn hợp Y. Nghiền nhỏ, trộn đều rồi chia Y làm 2 phần:
- Phần 1: Cho tác dụng với dung dịch NaOH dư, thu được 0,045 mol H2 và 3,36 gam chất rắn không tan.
- Phần 2: Trộn với m gam KNO3 rồi hòa tan vào 100 gam dung dịch HCl, sau phản ứng thu được dung dịch T (chỉ chứa muối clorua) và hỗn hợp khí (gồm 0,12 mol NO, 0,03 mol H2). Cho T tác dụng với dung dịch AgNO3 dư, thu được 147,82 gam kết tủa. Nồng độ phần trăm của FeCl2 có trong dung dịch T là
A. 4,10%.
B. 3,67%.
C. 3,22%.
D. 4,68%.
Nung 21,69 gam hỗn hợp X gồm Al và Fe2O3 trong chân không đến phản ứng hoàn toàn, thu được hỗn hợp Y. Nghiền nhỏ, trộn đều rồi chia Y làm 2 phần: - Phần 1: Cho tác dụng với dung dịch NaOH dư, thu được 0,045 mol H2 và 3,36 gam chất rắn không tan. - Phần 2: Trộn với m gam KNO3 rồi hòa tan vào 100 gam dung dịch HCl, sau phản ứng thu được dung dịch T (chỉ chứa muối clorua) và hỗn hợp khí (gồm 0,12 mol NO, 0,03 mol H2). Cho T tác dụng với dung dịch AgNO3 dư, thu được 147,82 gam kết tủa. Nồng độ phần...
Đọc tiếp
Nung 21,69 gam hỗn hợp X gồm Al và Fe2O3 trong chân không đến phản ứng hoàn toàn, thu được hỗn hợp Y. Nghiền nhỏ, trộn đều rồi chia Y làm 2 phần:
- Phần 1: Cho tác dụng với dung dịch NaOH dư, thu được 0,045 mol H2 và 3,36 gam chất rắn không tan.
- Phần 2: Trộn với m gam KNO3 rồi hòa tan vào 100 gam dung dịch HCl, sau phản ứng thu được dung dịch T (chỉ chứa muối clorua) và hỗn hợp khí (gồm 0,12 mol NO, 0,03 mol H2). Cho T tác dụng với dung dịch AgNO3 dư, thu được 147,82 gam kết tủa. Nồng độ phần trăm của FeCl2 có trong dung dịch T là
A. 4,10%.
B. 3,67%.
C. 3,22%.
D. 4,68%.
Hòa tan hoàn toàn 15,6 gam hỗn hợp gồm Fe, Fe3O4, Fe2O3, Mg, MgO và CuO vào 200 gamdung dịch H2SO4 và NaNO3, thu được dung dịch X chỉ chứa muối sunfat trung hòa của kim loại, hỗnhợp khí Y gồm 0,01 mol N2O và 0,02 mol NO. Cho dung dịch X phản ứng với dung dịch Ba(OH)2 dư, thu được 89,15 gam kết tủa. Lọc kết tủa nung trong không khí đến khối lượng không đổi, thu được 84,386 gam chất rắn. Nồng độ phần trăm của FeSO4 trong X có giá trị gần nhất với giá trị nào sau đây? A. 0,85% B. 1,06% C. 1,45%...
Đọc tiếp
Hòa tan hoàn toàn 15,6 gam hỗn hợp gồm Fe, Fe3O4, Fe2O3, Mg, MgO và CuO vào 200 gamdung dịch H2SO4 và NaNO3, thu được dung dịch X chỉ chứa muối sunfat trung hòa của kim loại, hỗnhợp khí Y gồm 0,01 mol N2O và 0,02 mol NO. Cho dung dịch X phản ứng với dung dịch Ba(OH)2 dư, thu được 89,15 gam kết tủa. Lọc kết tủa nung trong không khí đến khối lượng không đổi, thu được 84,386 gam chất rắn. Nồng độ phần trăm của FeSO4 trong X có giá trị gần nhất với giá trị nào sau đây?
A. 0,85%
B. 1,06%
C. 1,45%
D. 1,86%
Cho Mg vào 200ml dung dịch A chứa CuSO4 0,5M và FeSO4 1M. Sau khi các phản ứng xảy ra hoàn toàn thu được 12 gam chất rắn X và dung dịch Y. Cho dung dịch Y tác dụng với dung dịch Ba(OH)2 lấy dư đến khi kết thúc các phản ứng thu được kết tủa E. Nung E trong không khí đến khối lượng không đổi thu được b gam chất rắn. Tính b.
Tính toán theo PTHH :
Mg + CuSO4 → Cu + MgSO4
Mg + FeSO4 → Fe + MgSO4
Ba(OH)2 + MgSO4 → BaSO4 + Mg(OH)2
Ba(OH)2 + FeSO4 → BaSO4 + Fe(OH)2
Mg(OH)2 → MgO + H2O
2 Fe(OH)2 + ½ O2 → Fe2O3 + 2 H2O
Giả sư dung dịch muối phản ứng hết
=> n Fe = n FeSO4 = 0,2 . 1= 0,2 mol => m Fe = 0,2 . 56 = 11,2 g
=> n Cu =n CuSO4 = 0,2 . 0,5 = 0,1 mol => m Cu = 0,1 . 64 = 6,4 g
=> m chất rắn = 11,2 + 6,4 = 17,6 g > 12 g > 6,4
=> kim loại Fe dư sau phản ứng Vì CuSO4 phản ứng trước sau đó mới đến FeSO4 phản ứng
CuSO4 đã hết và phản ứng với 1 phần FeSO4
12 g = m Cu + m Fe phản ứng = 6,4 g + m Fe phản ứng
=> m Fe = 5,6 g => n Fe = 0,1 mol => n FeSO4 dư = 0,2 – 0,1 = 0,1 mol
Theo PTHH : n Mg = 0,1 + 0,1 = 0,2 mol ( bắng số mol CuSO4 và FeSO4 phản ứng )
Theo PTHH : n Mg = n MgSO4 = n Mg(OH)2 = n MgO = 0,2 mol
n FeSO4 dư = n Fe(OH)2 = n Fe2O3 . 2 = 0,1 mol
=> n Fe2O3 = 0,1 mol
=> m chất rắn = m Fe2O3 + m MgO = 0,1 . 160 + 0,2 . 40 = 24 g
Đúng 0
Bình luận (0)
Cho 160 gam dung dịch CuSO4 nồng độ 10%phản ứng với 150 gam dung dịch NaOH 8%, thu được m gam kết tủa Cu(OH)2và dung dịch X. Tính m và nồng độ phần trăm mỗi chất tan trong dung dịch X
\(n_{CuSO_4}=\dfrac{160.10\%}{160}=0,1\left(mol\right)\)
\(n_{NaOH}=\dfrac{150.8\%}{40}=0,3\left(mol\right)\)
PTHH: CuSO4 + 2NaOH --> Cu(OH)2 + Na2SO4
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,3}{2}\) => CuSO4 hết, NaOH dư
PTHH: CuSO4 + 2NaOH --> Cu(OH)2 + Na2SO4
0,1------>0,2------->0,1------->0,1
=> m = 0,1.98 = 9,8 (g)
\(\left\{{}\begin{matrix}m_{NaOH_{dư}}=\left(0,3-0,2\right).40=4\left(g\right)\\m_{Na_2SO_4}=0,1.142=14,2\left(g\right)\end{matrix}\right.\)
mdd sau pư = 160 + 150 - 9,8 = 300,2 (g)
\(\left\{{}\begin{matrix}C\%_{NaOH_{dư}}=\dfrac{4}{300,2}.100\%=1,33\%\\C\%_{Na_2SO_4}=\dfrac{14,2}{300,2}.100\%=4,73\%\end{matrix}\right.\)
Đúng 5
Bình luận (0)
\(m_{CuSO_4}=\dfrac{160.10}{100}=16\left(g\right)\\ n_{NaOH}=\dfrac{8.150}{100}=12\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}n_{CuSO_4}=\dfrac{16}{160}=0,1\left(mol\right)\\n_{NaOH}=\dfrac{12}{40}=0,3\left(mol\right)\end{matrix}\right.\)
PTHH: 2NaOH + CuSO4 ---> Cu(OH)2 + Na2SO4
LTL: \(0,1< \dfrac{0,3}{2}\rightarrow\) NaOH dư
Theo pt: \(\left\{{}\begin{matrix}n_{NaOH\left(pư\right)}=\dfrac{1}{2}n_{CuSO_4}=2.0,1=0,2\left(mol\right)\\n_{Na_2SO_4}=n_{Cu\left(OH\right)_2}=n_{CuSO_4}=0,1\left(mol\right)\end{matrix}\right.\)
\(\rightarrow m=0,1.98=9,8\left(g\right)\\ m_{dd}=160+150-9,8=300,2\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}C\%_{NaOH\left(dư\right)}=\dfrac{\left(0,3-0,2\right).40}{300,2}=1,33\%\\C\%_{Na_2SO_4}=\dfrac{0,1.142}{300,2}=4,73\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)