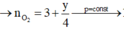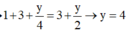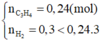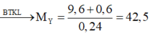Trộn một hiđrocacbon X với lượng O2 vừa đủ để đốt cháy hết X, được hỗn hợp A ở 0oC và áp suất P1. Đốt cháy hoàn toàn X, thu được hỗn hợp sản phẩm B ở 218,4oC có áp suất P2 gấp 2 lần áp suất P1. Công thức phân tử của X là :

Những câu hỏi liên quan
Trộn một hiđrocacbon X với lượng O2 vừa đủ để đốt cháy hết X, được hỗn hợp A ở 0oC và áp suất P1. Đốt cháy hoàn toàn X, thu được hỗn hợp sản phẩm B ở 218,4oC có áp suất P2 gấp 2 lần áp suất P1. Công thức phân tử của X là : A. C3H8 B. C2H6 C. C3H6 D. C4H10
Đọc tiếp
Trộn một hiđrocacbon X với lượng O2 vừa đủ để đốt cháy hết X, được hỗn hợp A ở 0oC và áp suất P1. Đốt cháy hoàn toàn X, thu được hỗn hợp sản phẩm B ở 218,4oC có áp suất P2 gấp 2 lần áp suất P1. Công thức phân tử của X là :
A. C3H8
B. C2H6
C. C3H6
D. C4H10
Trộn một hiđrocacbon X với lượng O2 vừa đủ để đốt cháy hết X, được hỗn hợp A ở 0oC và áp suất P1. Đốt cháy hoàn toàn X, thu được hỗn hợp sản phẩm B ở 218,4oC có áp suất P2 gấp 2 lần áp suất P1. Công thức phân tử của X là : A. C4H10 B. C2H6 C. C3H6 D. C3H8
Đọc tiếp
Trộn một hiđrocacbon X với lượng O2 vừa đủ để đốt cháy hết X, được hỗn hợp A ở 0oC và áp suất P1. Đốt cháy hoàn toàn X, thu được hỗn hợp sản phẩm B ở 218,4oC có áp suất P2 gấp 2 lần áp suất P1. Công thức phân tử của X là :
A. C4H10
B. C2H6
C. C3H6
D. C3H8
Đáp án B
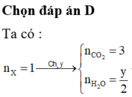
Để đơn giản cho việc tính toán ta chọn số mol của X (CxHy) là 1 mol thì từ giả thiết và phương trình phản ứng ta thấy số mol O2 đem phản ứng là : 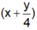
Phương trình phản ứng :
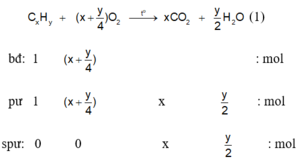
Ở 218,4oC nước ở thể hơi và gây áp suất lên bình chứa.
Tổng số mol khí trước phản ứng : 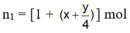
Tổng số mol khí sau phản ứng : 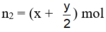
Do nhiệt độ trước và sau phản ứng thay đổi đổi nên :

Vậy A là C2H6
Đúng 0
Bình luận (0)
Trộn 1 hiđrocacbon X với lượng O2 vừa đủ để đốt cháy hết X được hỗn hợp A ở 0°C và áp suất P1. Đốt cháy hoàn toàn X thu đc hỗn hợp sản phẩm B ở 218,4°C có áp suất P2 gấp 2 lần áp suất P1. Công thức phân tử của X?
Xem chi tiết
X là hỗn hợp gồm một số hiđrocacbon ở thể khí, Y là không khí. Trộn X với Y ở cùng nhiệt độ áp suất theo tỉ lệ thể tích (1:15) được hỗn hợp khí Z. Cho Z vào bình kín dung tích không đổi V. Nhiệt độ và áp suất trong bình là toC và p atm. Sau khi đốt cháy X trong bình chỉ có N2, CO2 và hơi nước với
V
C
O
2
:
V
H...
Đọc tiếp
X là hỗn hợp gồm một số hiđrocacbon ở thể khí, Y là không khí. Trộn X với Y ở cùng nhiệt độ áp suất theo tỉ lệ thể tích (1:15) được hỗn hợp khí Z. Cho Z vào bình kín dung tích không đổi V. Nhiệt độ và áp suất trong bình là toC và p atm. Sau khi đốt cháy X trong bình chỉ có N2, CO2 và hơi nước với V C O 2 : V H 2 O = 7 : 4 . Sau khi đưa bình về toC, áp suất trong bình sau khi đốt là p1 có giá trị là
A. p 1 = 3 5 p
B. p1 = p.
C. p 1 = 16 17 p
D. p 1 = 47 48 p
Đáp án D
Giả sử trộn 1 mol X và 15 mol Y → số mol O2 : 3 mol, số mol N2 : 12 mol
Gọi số mol của CO2 và H2O lần lượt 7x và 4x mol
Bảo toàn nguyên tố O → 7x. 2 + 4x = 3.2 → x = 1/3 mol
Vậy sau phản ứng trong bình chứa 7/3mol CO2 , 4/3 mol H2O và 12 mol N2
Có trong cùng điều kiện nhiệt độ thể tích thì

Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 1 lít hỗn hợp khí gồm ankin X và hiđrocacbon Y cần dùng 2,25 lít khí O2, thu được 1,5 lít khí CO2 (các thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất). Công thức phân tử của X và Y lần lượt là: A. C2H2 và CH4 B. C3H4 và C2H6 C. C2H2 và C2H4 D. C3H4 và CH4
Đọc tiếp
Đốt cháy hoàn toàn 1 lít hỗn hợp khí gồm ankin X và hiđrocacbon Y cần dùng 2,25 lít khí O2, thu được 1,5 lít khí CO2 (các thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất). Công thức phân tử của X và Y lần lượt là:
A. C2H2 và CH4
B. C3H4 và C2H6
C. C2H2 và C2H4
D. C3H4 và CH4
Hỗn hợp X gồm O2 và O3 có tỉ khối so với H2là 22. Hỗn hợp khí Y gồm metylamin và etylamin có tỉ khối so với H2 là 17,833. Để đốt cháy hoàn toàn V1 lít Y cần vừa đủ V2 lít X (biết sản phẩm cháy gồm CO2, H2O và N2, các chất khí đo ở cùng điều kiện nhiệt độ, áp suất). Tỉ lệ V1 :V2 là A. 3 : 5 B. 5 : 3 C. 2 : 1 D. 1: 2
Đọc tiếp
Hỗn hợp X gồm O2 và O3 có tỉ khối so với H2là 22. Hỗn hợp khí Y gồm metylamin và etylamin có tỉ khối so với H2 là 17,833. Để đốt cháy hoàn toàn V1 lít Y cần vừa đủ V2 lít X (biết sản phẩm cháy gồm CO2, H2O và N2, các chất khí đo ở cùng điều kiện nhiệt độ, áp suất). Tỉ lệ V1 :V2 là
A. 3 : 5
B. 5 : 3
C. 2 : 1
D. 1: 2
X mạch hở có công thức C3Hy. Một bình có dung tích không đổi chứa hỗn hợp khí gồm X và O2 dư ở 1500C, áp suất 2 atm. Bật tia lửa điện để đốt cháy X sau đó đưa bình và 1500C áp suất bình vẫn là 2 atm. Người ta trộn 9,6 gam X với 0,6 gam H2 rồi cho qua bình Ni nung nóng (H100%) thì thu được hỗn hợp Y. Khối lượng mol trung bình của Y là: A. 30 B. 46,5 C. 48,5. D. 42,5
Đọc tiếp
X mạch hở có công thức C3Hy. Một bình có dung tích không đổi chứa hỗn hợp khí gồm X và O2 dư ở 1500C, áp suất 2 atm. Bật tia lửa điện để đốt cháy X sau đó đưa bình và 1500C áp suất bình vẫn là 2 atm. Người ta trộn 9,6 gam X với 0,6 gam H2 rồi cho qua bình Ni nung nóng (H=100%) thì thu được hỗn hợp Y. Khối lượng mol trung bình của Y là:
A. 30
B. 46,5
C. 48,5.
D. 42,5
Hỗn hợp X gồm
O
2
v
à
O
3
có tỉ khối so với
H
2
là 22. Hỗn hợp khí Y gồm metylamin và etylamin có tỉ khối so với
H
2
là 17,833. Để đốt cháy hoàn toàn V1 lít Y cần vừa đủ V2 lít X (biết sản phẩm cháy gồm
C
O
2
,
...
Đọc tiếp
Hỗn hợp X gồm O 2 v à O 3 có tỉ khối so với H 2 là 22. Hỗn hợp khí Y gồm metylamin và etylamin có tỉ khối so với H 2 là 17,833. Để đốt cháy hoàn toàn V1 lít Y cần vừa đủ V2 lít X (biết sản phẩm cháy gồm C O 2 , H 2 O v à N 2 , các chất khí khi đo ở cùng điều kiện nhiệt độ, áp suất). Tỉ lệ V 1 : V 2 là :
A. 3 : 5
B. 5 : 3
C. 2 : 1
D. 1 : 2
Đặt CTPT trung bình của 2 amin là .
Theo giả thiết suy ra: 14 n ¯ + 17 = 2.17 , 833 ⇒ n ¯ = 4 3
Quy đổi hỗn hợp O 3 , O 2 thành O, theo định luật bảo toàn khối lượng ta có.
Sơ đồ phản ứng:
C H 2 + 3 N → t ° 2 C O 2 + ( 2 + 3 ) H 2 O + N 2 1
mol : 1 n ¯ 2 + 3 2
Theo (1) ta có:
n O p u = 2 + 2 + 3 2 = 5 , 5 m o l
⇒ m ( O 3 , O 2 ) = m O = 5 , 5.16 = 88 g a m ⇒ n ( O 3 , O 2 ) = 88 2.22 = 2 m o l .
V ậ y V Y : V X = 1 : 2 .
Đáp án cần chọn là: D
Đúng 0
Bình luận (0)
Hỗn hợp X gồm
O
2
và
O
3
có tỉ khối so với
H
2
là 22. Hỗn hợp khí Y gồm metylamin và etylamin có tỉ khối so với
H
2
là 17,833. Để đốt cháy hoàn toàn
V
1
lít Y cần vừa đủ
V
2
lít X (biết sản phẩm cháy gồm
C
O
2...
Đọc tiếp
Hỗn hợp X gồm O 2 và O 3 có tỉ khối so với H 2 là 22. Hỗn hợp khí Y gồm metylamin và etylamin có tỉ khối so với H 2 là 17,833. Để đốt cháy hoàn toàn V 1 lít Y cần vừa đủ V 2 lít X (biết sản phẩm cháy gồm C O 2 , H 2 O và N 2 , các chất khí khi đo ở cùng điều kiện nhiệt độ, áp suất). Tỉ lệ V 1 : V 2 là:
A. 3 : 5.
B. 5 : 3.
C. 2 : 1.
D. 1 : 2