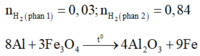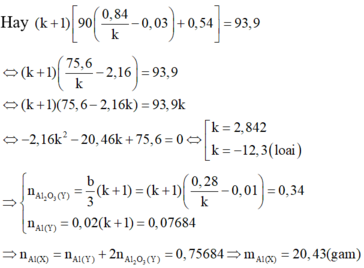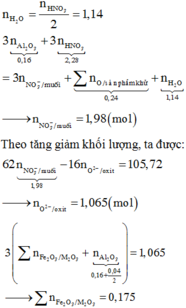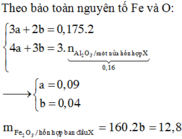Cho m gam hỗn hợp A gồm Al và Fe3O4. Nung A trong khí trơ, nhiệt độ cao để phản ứng xảy ra hoàn toàn thu được hỗn hợp B. Nghiền nhỏ hỗn hợp B, trộn đều, chia làm hai phần không bằng nhau: + Phần 1 (phần ít): Tác dụng với dung dịch NaOH dư thu được 1,176 lít khí H2. Tách riêng chất không tan đem hòa tan trong dung dịch HCl dư thu được 1,008 lít khí. + Phần 2 (phần nhiều): Cho tác dụng với dung dịch HCl dư thu được 6,552 lít khí. Giá trị của m và thành phần phần trăm khối lượng của một chất có tro...
Đọc tiếp
Cho m gam hỗn hợp A gồm Al và Fe3O4. Nung A trong khí trơ, nhiệt độ cao để phản ứng xảy ra hoàn toàn thu được hỗn hợp B. Nghiền nhỏ hỗn hợp B, trộn đều, chia làm hai phần không bằng nhau:
+ Phần 1 (phần ít): Tác dụng với dung dịch NaOH dư thu được 1,176 lít khí H2. Tách riêng chất không tan đem hòa tan trong dung dịch HCl dư thu được 1,008 lít khí.
+ Phần 2 (phần nhiều): Cho tác dụng với dung dịch HCl dư thu được 6,552 lít khí.
Giá trị của m và thành phần phần trăm khối lượng của một chất có trong hỗn hợp A (thể tích các khí đo ở đktc) gần giá trị nào nhất sau đây?
A. 22 và 63%.
B. 23 và 64%.
C. 23 và 37%.
D. 22 và 36%.