Ở 20 độ C độ tan trong nc của Cu (NO3)2.6H2O là 125g. Tính khối lượng Cu (NO3)2.6H2O cần lấy để pha chế 450g dung dịch bão hòa và tính nồng độ % Cu (NO3)2 bão hòa ở nhiệt độ đó

Những câu hỏi liên quan
Ở 20 độ C, hòa tan m g Cu(NO3)2.6H2O vào 100g dd Cu(NO3)2 30% thu đc dung dịch bão hòa Cu(NO3)2. Tính m. Biết đọ tan của Cu(NO3)2 tại 20 độ C là 125g
Mong mn giúp :((
\(C\%_{bh}=\dfrac{125}{225}=\dfrac{\dfrac{m}{296}.188+100.0,3}{m+100}\\ m=321,132\left(g\right)\)
Đúng 1
Bình luận (1)
ở 20độ C độ tan tronh nc của Cu(NO3)2 * 6H2O là 125g . tính khối lượng của Cu(NO3)2 * 6H2O cần lấy để pha chế 450g đ bão hòa tính khối lượng Cu(NO3)2 VÀ C % của dd đó ở 20 độ C
Ở 20oC
100 g nước ht 125g muối tạo thành 225 g dung dịch
Vậy xg nuoc ht y g muối tạo 450 g dd
--->y=\(\frac{450.125}{225}=250\left(g\right)\)
Cứ 296g Cu(NO3)2.6H2O có 188 g Cu(NO3)2
Vậy 250g .............................a g ................
-->m \(_{Cu\left(NO3\right)2}=\frac{250.188}{296}=158,78\left(g\right)\)
C%=\(\frac{158,78}{450}.100\%=35,28\%\)
ở 20độ C độ tan tronh nc của Cu(NO3)2 * 6H2O cần lấy để pha chế 450g đ bão hòa tính khối lượng Cu(NO3)2 VÀ C % của dd đó ở 20 độ C
Đề thiếu độ tan của Cu(NO3)2
Hòa tan 32 g CuSO4 vào nước được 100ml dung dịch cuso4 bão hòa ở 60 độ c. Biết độ tan của CuSO4 ở nhiệt độ này là 40 gam.
a) Tính nồng độ mol và nồng độ phần trăm của dd CuSO4 bão hòa ở nhiệt độ trên
b)Tinh khối lượng H2O cần dùng pha vào dd trên để được dd CuSO4 10 phần trăm
GIÚP MÌNH LẸ VỚI. MÌNH ĐANG CẦN GẤP.
Giải thích các bước giải:
a Để tính nồng độ % của dung dịch CuSO4 bão hòa ở nhiệt độ trên, ta dùng công thức:
Nồng độ % = (Khối lượng chất tan/Công thức phân tử chất tan) / Thể tích dung dịch x 100%
Với dung dịch CuSO4 bão hòa ở 60 độ C, ta có:
Khối lượng chất tan (CuSO4) = 40 kg = 40000 g
Thể tích dung dịch = 100 ml = 100 cm^3
Công thức phân tử CuSO4: 1 Cu + 1 S + 4 O = 63.5 + 32 + 4 x 16 = 159.5
Nồng độ % = (40000/159.5) / 100 = 25.08 %
Vậy, nồng độ % của dung dịch CuSO4 bão hòa ở nhiệt độ 60 độ C là khoảng 25.08 %.
b) Để tính khối lượng H2O cần dùng để pha vào dung dịch trên và có được dung dịch CuSO4 10%, ta dùng công thức:
Khối lượng H2O = Khối lượng chất tan ban đầu - Khối lượng chất tan sau pha / (Nồng độ sau pha - Nồng độ ban đầu)
Giả sử khối lượng chất tan sau khi pha là x g (= 10/100 x khối lượng dung dịch sau khi pha)
Vậy, ta có:
Khối lượng chất tan sau pha = 32 g + x g
Nồng độ sau pha = 10%
Nồng độ ban đầu = 25.08 %
Ứng dụng công thức, ta có:
x = (32 - 0.1 x (32 + x)) / (0.100 - 0.2508)
10000 x = 32 - 0.1 x (32 + x)
10000 x = 32 - 3.2 - 0.1x^2
0.1x^2 - 9967.2x + 3.2 = 0
Giải phương trình trên bằng phương pháp giải phương trình bậc hai ta có:
x ≈ 0.3145 hoặc x ≈ 9965.88
Với x ≈ 0.3145, ta được khối lượng H2O ≈ 32 - 0.3145 = 31.6855 g
Vậy, để có được dung dịch CuSO4 10%, ta cần dùng khoảng 31.6855 g nước.
Đúng 1
Bình luận (0)
.1
Tính khối lượng BaCl2 có trong 200g dung dịch BaCl2 25%
2
Có 40g Cu(NO3)2 trong 200g dung dịch. Tính nồng độ phần trăm của dung dịch Cu(NO3)2
3
Biết SNaCl (25 0 C) = 36 gam. Hãy tính nồng độ phần trăm của dung dịch NaCl ở nhiệt độ này
1.\(m_{BaCl_2}\) = 200.25% = 50g
2.\(C\%_{Cu\left(NO_3\right)_2}\) = \(\dfrac{40}{200}.100\) = \(20\%\)
3.Ở 25\(^o\)C 100g nước hòa tan được 36 g NaCl để tạo dung dịch bão hòa
\(m_{dd}=m_{ct}+m_{dm}=36+100=136g\)
Nồng độ phần trăm của dung dịch NaCl:C% = \(\dfrac{36}{136}.100=26,47\%\)
Đúng 2
Bình luận (1)
\(1,m_{BaCl_2}=\dfrac{200.25}{100}=50\left(g\right)\\ 2,C\%_{Cu\left(NO_3\right)_2}=\dfrac{4}{200}.100\%=20\%\\ 3,C\%=\dfrac{36}{36+100}.100\%=26,47\%\)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam Cu vào 400 gam dung dịch Fe(NO3)3 12,1% thu được dung dịch A có nồng độ Cu(NO3)2 là 3,71%. Nồng độ % Fe(NO3)3 trong dung dịch A là
A. 2,39%.
B. 3,12%.
C. 4,20%.
D. 5,64%.
Chọn đáp án A
mFe(NO3)3 bđ = 400.12,1/100 = 48,4 (g)
Gọi số mol của Cu là x (mol)
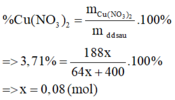
Cu + 2Fe3+ → 2Fe2+ + Cu2+
0,08 → 0,16 (mol)
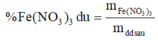
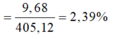
=> mFe(NO3)3 dư = 48,4 – 0,16.242 = 9,68 (g)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam Cu vào 400 gam dung dịch Fe(NO3)3 12,1% thu được dung dịch A có nồng độ Cu(NO3)2 là 3,71%. Nồng độ % Fe(NO3)3 trong dung dịch A là
A. 2,39%.
B. 3,12%.
C. 4,20%.
D. 5,64%.
Chọn đáp án A
mFe(NO3)3 bđ = 400.12,1/100 = 48,4 (g)
Gọi số mol của Cu là x (mol)
mdd sau = mCu + mddFe(NO3)2 => mdd sau =( 64x + 400) g
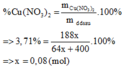
Cu + 2Fe3+ → 2Fe2+ + Cu2+
0,08 → 0,16 (mol)
=> mFe(NO3)3 dư = 48,4 – 0,16.242 = 9,68 (g)
![]()
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam Cu vào 400 gam dung dịch Fe(NO3)3 12,1% thu được dung dịch A có nồng độ Cu(NO3)2 là 3,71%. Nồng độ % Fe(NO3)3 trong dung dịch A là A. 2,39%. B. 3,12%. C. 4,20%. D. 5,64%.
Đọc tiếp
Hòa tan hoàn toàn m gam Cu vào 400 gam dung dịch Fe(NO3)3 12,1% thu được dung dịch A có nồng độ Cu(NO3)2 là 3,71%. Nồng độ % Fe(NO3)3 trong dung dịch A là
A. 2,39%.
B. 3,12%.
C. 4,20%.
D. 5,64%.
a, Nồng độ dung dịch KCl bão hòa ở 40°C là 28,57% Tính độ tan của KCl trong dung dịch ở nhiệt độ đó. b,xác định khối lượng AgNO3 bão hòa ở 60°C xuống 10°C biết độ tan AgNO3 ỏe 60°C là 525 gam ở 10°C là 170gam
Bài này có 2 phần phần b bị dính vô phần a mọi người thông cảm giúp
Đúng 0
Bình luận (0)
\(S_{KCl}=\dfrac{100.28,57}{100-28,57}=39,99\%\)
Đúng 1
Bình luận (5)



















