0,672 lít hỗn hợp gồm C2H4 và C2H2 với tỉ lệ sớ mol là 1: 2 được dẫn qua dung dịch Brôm dư .hỏi sau phản ứng bình Brôm tăng bao nhiêu gam ?
cá bạn giúp mk vs nhe s mk đang cần gấp !!! cám ơn mọi người trước !!! ^_^ ^_^
Dẫn 4,48l hỗn hợp gồm CH4 và C2H4 vào dung dịch brôm dư,thấy khối lượng Brom phản ứng là 24 gam.Tính phần trăm về thể tích các khí trong hỗn hợp ban đầu
Mọi ng ơi giúp mk với mk đang cần gấp huhuhu......
Ta có: \(n_{Br_2}=\dfrac{24}{160}=0,15\left(mol\right)\)
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{C_2H_4}=n_{Br_2}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,15.22,4}{4,48}.100=75\%\\\%V_{CH_4}=25\%\end{matrix}\right.\)
Một hỗn hợp X gồm 0,1 mol C2H4; 0,15 mol C3H6 và 0,25 mol H2. Dẫn hỗn hợp X qua Ni nung nóng thu được hỗn hợp Y. Dẫn hỗn hợp Y qua dung dịch Br2 dư thấy khối lượng bình tăng 1,82 gam và có 8 gam brôm đã tham gia phản ứng. Xác định hiệu suất phản ứng hiđro hoá của etilen và propen. Biết rằng hiệu suất hiđro hóa của 2 anken là như nhau.
A. 75%
B. 80%
C. 67%
D. 67%
nBr2 = 0,05
Dẫn hỗn hợp Y qua dung dịch Br2 dư thấy khối lượng bình tăng 1,82 gam và có 8 gam brom đã tham gia phản ứng
⇒ nAnken/Y = nBr2 = 0,05 = nC2H4 dư + nC3H6 dư (1)
mAnken/Y = 1,82g
Vì Hiệu suất hidro hóa của 2 anken như nhau
⇒ nC2H4 phản ứng : nC2H4 ban đầu = nC3H6 phản ứng : nC3H6 ban đầu
⇒ nC2H4 dư : nC2H4 = nC3H6 dư : nC3H6
⇒ nC2H4 dư : 0,1 = nC3H6 dư : 0,15 (2)
Từ (1) và (2) ⇒ nC2H4 dư = 0,02 ; nC3H6 = 0,03
nC2H4 phản ứng = 0,1 – 0,02 = 0,08
⇒ H = (0,08 : 0,1).100% = 80%
Đáp án B.
Trộn hỗn hợp gồm 0,1 mol C2H4, 0,2 mol C3H6, 0,1 mol C4H8, 0,1 mol C2H2 với 0,6 H2 vừa đủ thu được hỗn hợp X. Cho X vào bình kín ở nhiệt độ thường, có chứa xúc tác Ni sau đó đun nóng hỗn hợp một thời gian thu được hỗn hợp Y (không tạo kết tủa khi cho qua dung dịch AgNO3/NH3). Cho hỗn hợp Y đi qua bình đựng nước Brôm dư thấy khối lượng bình tăng lên m gam. Hỗn hợp Z bay ra khỏi bình brom có tỉ khối so với He là 6,075. Biết các hiđrocacbon có tốc độ phản ứng khác nhau. Giá trị của m là
A. 12,675 gam
B. 8,45 gam
C. 8,96 gam
D. 12,35 gam
Đáp án B
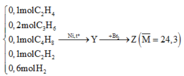
Vì Y không còn C2H2 nên có thể quy đổi X gồm 0,5 mol anken và 0,5 mol H2
Xét trong Y, ta có: ![]()
Áp dụng bảo toàn khối lượng ta có:
![]()
Trộn hỗn hợp gồm 0,1 mol C2H4, 0,2 mol C3H6, 0,1 mol C4H8, 0,1 mol C2H2 với 0,6 H2 vừa đủ thu được hỗn hợp X. Cho X vào bình kín ở nhiệt độ thường, có chứa xúc tác Ni sau đó đun nóng hỗn hợp một thời gian thu được hỗn hợp Y (không tạo kết tủa khi cho qua dung dịch AgNO3/NH3). Cho hỗn hợp Y đi qua bình đựng nước Brôm dư thấy khối lượng bình tăng lên m gam. Hỗn hợp Z bay ra khỏi bình brom có tỉ khối so với He là 6,075. Biết các hiđrocacbon có tốc độ phản ứng khác nhau. Giá trị của m là
A. 12,675 gam
B. 8,45 gam
C. 8,96 gam
D. 12,35 gam
Đáp án B
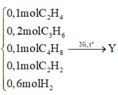
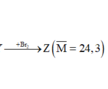
Vì Y không còn C2H2 nên có thể quy đổi X gồm 0,5 mol anken và 0,5 mol H2
Xét trong Y, ta có:
![]()
Áp dụng bảo toàn khối lượng ta có:
![]()
Trộn hỗn hợp gồm 0,1 mol C2H4, 0,2 mol C3H6, 0,1 mol C4H8, 0,1 mol C2H2 với 0,6 H2 vừa đủ thu được hỗn hợp X. Cho X vào bình kín ở nhiệt độ thường, có chứa xúc tác Ni sau đó đun nóng hỗn hợp một thời gian thu được hỗn hợp Y (không tạo kết tủa khi cho qua dung dịch AgNO3/NH3). Cho hỗn hợp Y đi qua bình đựng nước Brôm dư thấy khối lượng bình tăng lên m gam. Hỗn hợp Z bay ra khỏi bình brom có tỉ khối so với He là 6,075. Biết các hiđrocacbon có tốc độ phản ứng khác nhau. Giá trị của m là
A. 12,675 gam
B. 8,45 gam
C. 8,96 gam
D. 12,35 gam
Đáp án B
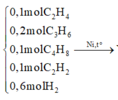
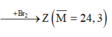
Vì Y không còn C2H2 nên có thể quy đổi X gồm 0,5 mol anken và 0,5 mol H2
Xét trong Y, ta có: n H 2 d ư = n a n k e n
![]()
Áp dụng bảo toàn khối lượng ta có:
![]()
Dẫn 11,2 lít hỗn hợp khí CH4 và C2H4 ở đktc qua 250 gam dung dịch brom, sau phản ứng thấy khối lượng bình brôm tăng 5,6 gam.Tính thành phần trăm theo thể tích và khối lượng của mỗi khí trong hỗn hợp đầu.b- Tính nồng độ phần trăm của dung dịch brom ban đầu. c- Nếu đốt cháy lượng C2H4 trên, rồi dẫn khí thu được vào 200ml dd NaOH 2M, thì muối nào được tạo thành? Tìm CM của muối.
Cho 8,96 lít (đktc) hỗn hợp metan và axetylen qua bình đựng dung dịch brôm. Phản ứng xong thấy bình đựng dung dịch brôm tăng lên 5,2 gam. a/ Tính thành phần phần trăm theo thể tích mỗi khí trong hỗn hợp. b/ Đốt cháy toàn bộ hỗn hợp khí trên rồi dẫn toàn bộ sản phẩm qua bình đựng dung dịch nước vôi trong dư. Tính khối lượng kết tủa thu được.
a)
\(m_{C_2H_2} = m_{tăng} = 5,2\ gam\\ \Rightarrow n_{C_2H_2} = \dfrac{5,2}{26} = 0,2(mol)\)
Vậy :
\(\%V_{C_2H_2} = \dfrac{0,2.22,4}{8,96}.100\% = 50\%\\ \%V_{CH_4} = 100\%-50\% = 50\%\)
b)
\(n_{CH_4} = n_{C_2H_2} = 0,2(mol)\)
CH4 + O2 \(\xrightarrow{t^o}\) CO2 + H2O
0,2.........................0,2...................................(mol)
C2H2 + \(\dfrac{5}{2}\)O2 \(\xrightarrow{t^o}\) 2CO2 + H2O
0,2................................0,4.................................(mol)
CO2 + Ca(OH)2 → CaCO3 + H2O
(0,2+0,4)............................(0,2+0,4)........................................(mol)
\(\Rightarrow m_{CaCO_3} =(0,2 + 0,4).100 = 60(gam)\)
Hỗn hợp X gồm C2H2 và H2 (có tỉ lệ mol tương ứng là 1 : 2). Đun nóng 10,08 lít (đktc) hỗn hợp X với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y. Dẫn hỗn hợp Y qua dung dịch nước brom dư, thấy bình brom tăng 3 gam và còn lại V lít (đktc) hỗn hợp khí Z không bị hấp thụ. Tỉ khối của Z so với heli bằng 5/3. Giá trị của V là
A. 13,44 lít
B. 4,48 lít
C. 10,08 lít
D. 5,04 lít
Đáp án D
Ta có nC2H2 = 0,15 mol, nH2 = 0,3 mol
Ta có mX = mY = mbình tăng + mZ
→ 0,15. 26 + 0,3. 2 = 3 + mZ → mZ = 1,5 gam
→ nZ =
1
,
5
5
3
.
4
= 0,225 mol → V= 5,04 lít.
Hỗn hợp khí X gồm C2H4,C2H2,C3H8,C4H10, H2. Dẫn 6,32 gam X qua bình đựng dung dịch Brom dư thì có 0,12 mol Br2 phản ứng. Đốt cháy hoàn toàn 2,24 lít X(đktc), thu được 4,928lít CO2 và m gam H2O.Giá trị của m là :
A. 5,85
B. 4.68
C. 3,51
D. 2,34
Đáp án : B
nX = 0,1 mol ; nCO2 = nC(X) = 0,22mol
Giả sử lượng chất trong 6,32g X gấp t lần lượng chất có trong 0,1 mol X
Xét 6,32g X :
=> nX = 0,1t mol ; nCO2 = 0,22t mol
=> Nếu đốt cháy thì ( số p - 1)nX = nCO2 – nH2O
=> np - nX = nCO2 – nH2O
=> 0,12 – 0,1t = 0,22t – nH2O
=> nH2O = 0,32t – 0,12 mol
Bảo toàn khối lượng : mX = mC + mH
=> 6,32 = 0,22t.12 + ( 0,32t – 0,12).2
=> t = 2
=> Trong 6,32g X có nH2O = 0,52mol
=> Trong 0,1 mol X có nH2O = 0,52. ½ = 0,26 mol
=> m = 4,68g