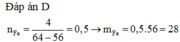Nhúng một thanh sắt có khối lượng 15,6 gam vào dung dịch CuSO4 sau một thời gian lấy đinh sắt ra khỏi dung dịch thấy khối lượng thanh sắt là 16,4 gam tính khối lượng sắt tham gia phản ứng biết rằng tất cả đồng sinh ra đều bám lên bề mặt của sắt

Những câu hỏi liên quan
Nhúng 1 thanh sắt có khối lượng 50g vào dung dịch CuSO4 sau 1 thời gian lấy đinh sắt ra khỏi dung dịch thấy khối lượng thanh sắt là 51g. Tính khối lượng đinh sắt tham gia phản ứng
\(Fe\left(x\right)+CuSO_4\rightarrow FeSO_4+Cu\left(x\right)\)
Khối lượng thanh sắt tăng thêm đúng bằng khối lượng Cu thêm vào trừ đi khối lượng Fe tham gia phản ứng.
Gọi số mol của Fe tham gia phản ứng là x
\(64x-56x=51-50=1\)
\(\Leftrightarrow x=0,125\)
\(\Rightarrow m_{Fe\left(pứ\right)}=56.0,125=7\)
Đúng 1
Bình luận (0)
Nhúng một thanh sắt vào dung dịch Cu(NO3)2. Sau một thời gian lấy thanh sắt ra, làm khô, thấy khối lượng thanh sắt tăng 4 gam. Khối lượng sắt đã phản ứng là:
A. 7,0 gam
B. 8,4 gam
C. 21gam
D. 28 gam
Nhúng một thanh sắt vào dung dịch
CuSO
4
, sau một thời gian thấy khối lượng chất rắn tăng 1,6 gam. Số mol
CuSO
4
đã tham gia phản ứng là: A. 0,1 mol. B. 0,2 mol. C. 0,3 mol. D. 0,4 mol.
Đọc tiếp
Nhúng một thanh sắt vào dung dịch CuSO 4 , sau một thời gian thấy khối lượng chất rắn tăng 1,6 gam. Số mol CuSO 4 đã tham gia phản ứng là:
A. 0,1 mol.
B. 0,2 mol.
C. 0,3 mol.
D. 0,4 mol.
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là A. 2,8 gam. B. 7,0 gam. C. 3,5 gam. D. 5,6 gam.
Đọc tiếp
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là
A. 2,8 gam.
B. 7,0 gam.
C. 3,5 gam.
D. 5,6 gam.
Ta có phản ứng: Fe + Cu2+ → Fe2+ + Cu↓
+ Đặt nFe pứ = a mol ⇒ nCu tạo thành = a mol.
⇒ mCu – mFe = 64a – 56a = 8a = 1 gam.
→ a = 0,125 ⇒ mFe đã pứ = 0,125×56 = 7 gam.
Đáp án B
Đúng 0
Bình luận (0)
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là A. 3,5 gam B. 7,0 gam C. 5,6 gam D. 2,8 gam
Đọc tiếp
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là
A. 3,5 gam
B. 7,0 gam
C. 5,6 gam
D. 2,8 gam
Đáp án : B
Fe + Cu2+ -> Fe2+ + Cu
x -> x
mtăng = 64x – 56x = 1g => x = 0,125 mol
=> mFe pứ = 7g
Đúng 0
Bình luận (0)
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là:
A. 3,5 gam.
B. 2,8 gam.
C. 7,0 gam.
D. 5,6 gam.
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là
A. 3,5 gam
B. 2,8 gam
C. 7,0 gam
D. 5,6 gam
Đáp án C
Fe + Cu2+ -> Fe2+ + Cu
.x -> x mol
=> mtăng = 64x – 56x = 1g => x = 0,125 mol
=> mFe pứ = 7g
Đúng 0
Bình luận (0)
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là:A. 2,8 gam. A. 2,8 gam. B. 7,0 gam. C. 3,5 gam. D. 5,6 gam.
Đọc tiếp
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là:A. 2,8 gam.
A. 2,8 gam.
B. 7,0 gam.
C. 3,5 gam.
D. 5,6 gam.
Đáp án B
Ta có phản ứng: Fe + Cu2+ → Fe2+ + Cu↓
+ Đặt nFe pứ = a mol ⇒ nCu tạo thành = a mol.
⇒ mCu – mFe = 64a – 56a = 8a = 1 gam.
Û a = 0,125 ⇒ mFe đã pứ = 0,125×56 = 7 gam
Đúng 0
Bình luận (0)
14/ Cho một thanh sắt có khối lượng 50gam vào dung dịch CuSO4. Sau một thời gian, lấy thanh sắt ra khỏi dung dịch thấy khối lượng thanh sắt là 51gam.
a. Viết PTHH
b. Tính khối lượng của đồng được giải phóng.(Biết rằng tất cả đồng sinh ra bám và bề mặt thanh sắt)
c. Tính khối lượng muối FeSO4 tạo thành
\(a.Fe+CuSO_4\rightarrow FeSO_4+Cu\\ b.Đặt:n_{Fe\left(pứ\right)}=x\left(mol\right)\\ m_{tăng}=m_{Cu\left(sinhra\right)}-m_{Fe\left(pứ\right)}=64x-56x=51-50\\ \Rightarrow x=0,125\left(mol\right)\\ m_{Cu}=0,125.64=8\left(g\right)\\ c.n_{FeSO_4}=n_{Fe\left(pứ\right)}=0,125\left(mol\right)\\ \Rightarrow m_{FeSO_4}=0,125.152=19\left(g\right)\)
Đúng 2
Bình luận (0)