Tìm công thức hóa học của axit có thành phần nguyên tố
a, H=21,12% N=29,8% O=68,08%
b, H=3,7% P=37,8% O=58,5%
1) Hãy tìm CTHH của những axit có thành phần nguyên tố như sau:
a. H: 2,12% ; N: 29,8% ; O: 68,08%
b. H: 3,7% ; P: 37,8% ; O: 58,5% 2)Trung hòa 200ml dung dịch H2SO4 1M bằng dung dịch NaOH 20%
a. Tính số gam dung dịch NaOH cần dùng.
b. Nếu thay dung dịch NaOH bằng dung dịch KOH thì phải dùng bao nhiêu ml dung dịch KOH 5,6% (D = 1,045g/ml) để trung hòa dung dịch axit đã cho?
Hãy tìm công thức hoá học của những axit có thành phần khối lượng như sau : H : 3,7% ; P: 37,8% ; O : 58,5%.
H : 3,7% ; P: 37,8% ; O : 58,5%.
Gọi công thức là: H x P y O z :
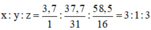
⇒ H 3 PO 3
Hãy tìm công thức hoá học của những axit có thành phần khối lượng như sau :
a) H : 2,1% ; N : 29,8% ; O : 68,1%.
b) H : 2,4% ; S : 39,1% ; O : 58,5%.
c) H : 3,7% ; P: 37,8% ; O : 58,5%.
Hãy tìm công thức hoá học của những axit có thành phần khối lượng như sau : H : 2,1% ; N : 29,8% ; O : 68,1%.
Đặt công thức hoá học của axit là H x N y O z . Ta có :
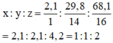
Công thức hoá học của axit là HNO 2 (axit nitrơ).
lập công thức hóa học của 1 hợp chất, biết rằng thành phần phần trăm khối lượng các nguyên tố trong hợp chất như sau : 58,5%C; 4,1%H; 11,4%N còn lại là O
CTHH : CaHbNCOd
ta có : %O =100 - ( 58,5 + 4,1 + 11,4 ) = 26 %
\(\frac{\%C}{MC}\):\(\frac{\%H}{MH}\):\(\frac{\%N}{MN}\):\(\frac{\%O}{MO}\)\(\frac{58,5}{12}:\frac{4,1}{1}:\frac{11,4}{14}:\frac{26}{16}\)=5 : 4 : 1 : 2
VẬY TA CÓ CTHH LÀ : C5H4NO2
Hãy tìm công thức hoá học của những axit có thành phần khối lượng như sau : H : 2,4% ; S : 39,1% ; O : 58,5%.
H : 2,4% ; S : 39,1% ; O : 58,5%.
Gọi công thức là H x S y O z :

⇒ HSO 3
Biết khối lượng mol của hợp chất A là 58,5 g, công thức hóa học của hợp chất A gồm 2 nguyên tố có thành phần % các nguyên tố Natri: 60,68%, còn lại là Clo.Xác định công thức hóa học của hợp chất?
Gọi công thức tổng quát của hợp chất A là NaxCly
% Cl = 100% - 60,68% = 39.32%
Ta có tỉ lệ : 60,68/23 : 39,32/35.5 = a: b
bạn xem đề bài có sai ko nhé ... CTHH của hợp chất này chắc chắn là NaCl , bạn chép sai đề hay sao ý, %Cl phải là 60,68%
Giúp mình với mai mình phải nộp rồi!
1/hợp chất A có thành phần các nguyên tố sau 52,94% Al và O . xác định công thức hóa học của A biết khối lượng mol của A 120g/mol
2/hợp chất C có thành phần các nguyên tố sau 2705% Na và16,47%N và O . xác định công thức hóa học của C biết khối lượng mol của C 85g/mol
a, Gọi CTHH cua a là : AlxOy
=>CTHH là Al2O3
b)
mNa = 85 . 27,06% = 23 (g)
mN = 85 . 16,47% = 14 (g)
mO = 85 - 23 - 14= 48 (g)
Tìm số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất:
nNa = 2323 = 1 (mol)
nN = 1414 = 1 (mol)
nO = 4816 = 3 (mol)
Suy ra trong một phân tử hợp chất có 1 nguyên tử Na, 1 nguyên tử N, 3 nguyên tử O
CTHH của Y: NaNO3
hãy tìm công thức hóa học của những hợp chất có thành phần các nguyên tố như sau
hợp chất A có khối lượng mol phân tử là 58,5 gam/mol thành phần các nguyên tố theo khối lượng 43,3% Na ; 11,3% C và còn lại là O
hợp chất B có khối lượng mol phân tử là 106 gam/mol thành phần các nguyên tố theo khối lượng 60,68% Cl và còn lại là Na
Hợp chất A:
- Khối lượng của từng nguyên tố là:
\(m_{Na}=\dfrac{58,5\text{x}43,3}{100}=25\left(g\right)\)
\(m_C=\dfrac{58,5x11,3}{100}=7\left(g\right)\)
\(m_O=58,5-25-7=26,5\left(g\right)\)
- Số mol của từng nguyên tố là:
\(n_{Na}=\dfrac{25}{23}=1\left(mol\right)\)
\(n_C=\dfrac{7}{12}=1\left(mol\right)\)
\(n_O=\dfrac{26,5}{16}=2\left(mol\right)\)
Vậy: Công thức hoá học của hợp chất A là \(NaCO_2\)
- Hợp chất B:
- Khối lượng của từng nguyên tố:
\(m_{Cl}=\dfrac{60,68\text{x}106}{100}=64\left(g\right)\)
\(m_{Na}=106-64=42\left(g\right)\)
- Số mol của từng nguyên tố là:
\(n_{Cl}=\dfrac{64}{35,5}=2\left(mol\right)\)
\(n_{Na}=\dfrac{42}{23}=2\left(mol\right)\)
Vậy: Công thức hoá học của hợp chất B là \(Na_2Cl_2\)