Cho m = 200g. khí ôxi dãn nở đẳng áp thể tích tăng hai lần và thực hiện công 15572J. Nhiệt dung riêng đẳng áp của ôxi \(c_p=0,92.10^3J\). Tính :
a) Nhiệt độ ban đầu của khí.
b) Nhiệt lượng chuyển của khí.
c) Độ biến thiên nội năng của khí.

Những câu hỏi liên quan
Người ta đốt nóng cho dãn nở đẳng áp 20g ôxi ở áp suất 2,8at và nhiệt độ
27
°
C
đến thể tích 8 lít. Cho ôxi có
μ
32
, lấy R 8,31J/mol.K, nhiệt dung riêng đẳng áp Cp 0,91.103J/kg.độ; 1at 9,81.104N/m2.a) Tính nhiệt độ cuối cùng và công của khí sinh ra khi dãn nở.b) Độ biến thiên nội năng của khí trong quá trình dãn nở.
Đọc tiếp
Người ta đốt nóng cho dãn nở đẳng áp 20g ôxi ở áp suất 2,8at và nhiệt độ 27 ° C đến thể tích 8 lít. Cho ôxi có μ = 32 , lấy R = 8,31J/mol.K, nhiệt dung riêng đẳng áp Cp = 0,91.103J/kg.độ; 1at = 9,81.104N/m2.
a) Tính nhiệt độ cuối cùng và công của khí sinh ra khi dãn nở.
b) Độ biến thiên nội năng của khí trong quá trình dãn nở.
a) Ở trạng thái cuối ta có:
![]()
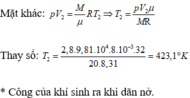
Trong quá trình đẳng áp:
![]()
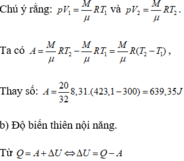
Trong đó:
![]()
Độ biến thiên nội năng:
![]()
Đúng 1
Bình luận (0)
Người ta đốt nóng cho dãn nở đẳng áp 20 g ôxi ở áp suất 2,8 at và nhiệt độ 27 oC đến thể tích 8 lít. Cho ôxi có μ 32g/mol, lấy R 8,31J/mol.K, nhiệt dung riêng đẳng áp Cp 0,91.103 J/kg.K; 1at 9,81.104N/m2. Độ biến thiên nội năng của khí trong quá trình dãn nở là: A. 2010J B. 1510J C. 1601,07J D. 2510J
Đọc tiếp
Người ta đốt nóng cho dãn nở đẳng áp 20 g ôxi ở áp suất 2,8 at và nhiệt độ 27 oC đến thể tích 8 lít. Cho ôxi có μ = 32g/mol, lấy R = 8,31J/mol.K, nhiệt dung riêng đẳng áp Cp = 0,91.103 J/kg.K; 1at = 9,81.104N/m2. Độ biến thiên nội năng của khí trong quá trình dãn nở là:
A. 2010J
B. 1510J
C. 1601,07J
D. 2510J
Đáp án: C
Ở trạng thái cuối ta có:
Thể tích:
V2 = 8.10-3 m3
Áp suất:
p = 2,8 at = 2,8.9,81.104 N/m2.
Mặt khác:
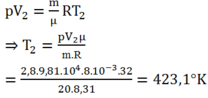
Công của khí sinh ra khi dãn nở trong quá trình đẳng áp:
![]()
Chú ý rằng:
![]()
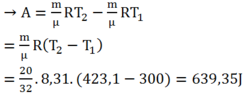
Độ biến thiên nội năng:
∆U = A + Q
Với quy ước dấu, khí sinh công A < 0, nhận nhiệt Q > 0.
Trong đó:
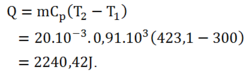
![]()
Đúng 0
Bình luận (0)
Một khối khí lý tưởng thể tích 3l, áp suất 2.10^5 N/m, nhiệt độ 27°C được đun nóng đẳng tích rồi cho dãn nở đẳng áp. Trong quá trình dãn nở nhiệt độ tăng thêm 30°C. Công mà khí đã thực hiện là
quá trình đẳng áp :
\(\dfrac{V_1}{T_1}=\dfrac{V_2}{T_2}\Rightarrow\dfrac{3}{27+273}=\dfrac{V_2}{30+27+273}\Rightarrow V_2=3,3\left(l\right)\)
độ thay đổi thể tích :
\(\Delta V=V_2-V_1=3,3-3=0,3\left(l\right)=0,0003\left(m^3\right)\)
công mà khí đã thực hiện :
\(A=p.\Delta V=2.10^5.0,0003=60\left(J\right)\)
Đúng 2
Bình luận (0)
Trong xilanh có tiết diện
200
c
m
2
, pittong cách đáy 30cm, có khí ở
27
0
C
và áp suất
10
6
N
/
m
2
. Khi nhận nhiệt lượng do 5g xăng bị cháy cung cấp, khí dãn nở đẳng áp, nhiệt độ tăng thêm
150
0
C
. Biết khi cháy 10% nhiệt lượng của xăng...
Đọc tiếp
Trong xilanh có tiết diện 200 c m 2 , pittong cách đáy 30cm, có khí ở 27 0 C và áp suất 10 6 N / m 2 . Khi nhận nhiệt lượng do 5g xăng bị cháy cung cấp, khí dãn nở đẳng áp, nhiệt độ tăng thêm 150 0 C . Biết khi cháy 10% nhiệt lượng của xăng cung cấp cho khí. Năng suất tỏa nhiệt của xăng là 4 , 8 . 10 7 J / k g . Tính công do khí thực hiện
A. 1500J
B. 3000J
C. 2480J
D. 1240J
Ta có:
Thể tích V 1 = S h = 200.30 = 6000 c m 3
Quá trình đẳng áp: → V 1 T 1 = V 2 T 2
→ V 2 = V 1 T 2 T 1 = 6000. 27 + 150 + 273 27 + 273 = 9000 c m 3
Công do khí thực hiện:
A = p V 2 − V 1 = 10 6 9000 − 6000 .10 − 6 = 3000 J
Đáp án: B
Đúng 0
Bình luận (0)
Trong xilanh có tiết diện
50
c
m
2
, pittong cách đáy 30cm, có khí ở
32
0
C
và áp suất
10
6
N
/
m
2
. Khi nhận nhiệt lượng do 5g xăng bị cháy cung cấp, khí dãn nở đẳng áp, nhiệt độ tăng thêm
150
0
C
. Biết khi cháy 10% nhiệt lượng của xăng c...
Đọc tiếp
Trong xilanh có tiết diện 50 c m 2 , pittong cách đáy 30cm, có khí ở 32 0 C và áp suất 10 6 N / m 2 . Khi nhận nhiệt lượng do 5g xăng bị cháy cung cấp, khí dãn nở đẳng áp, nhiệt độ tăng thêm 150 0 C . Biết khi cháy 10% nhiệt lượng của xăng cung cấp cho khí. Năng suất tỏa nhiệt của xăng là 4 , 8 . 10 7 J / k g . Tính công do khí thực hiện
A. 1500J
B. 2237,7J
C. 737,7J
D. 1005,5J
Ta có:
Thể tích V 1 = S h = 50.30 = 1500 c m 3
Quá trình đẳng áp:
⇒ V 1 T 1 = V 2 T 2 ⇒ V 2 = V 1 T 2 T 1 = 1500. 32 + 150 + 273 32 + 273 = 2237 , 7 c m 3
Công do khí thực hiện:
A = p V 2 − V 1 = 10 6 2237 , 7 − 1500 .10 − 6 = 737 , 7 J
Đáp án: C
Đúng 0
Bình luận (0)
Lấy 2,5 mol khí lí tưởng ở nhiệt độ 300K .Nung nóng đẳng áp lượng khí này cho đến khi thể tích của nó bằng 1,5 lần thể tích lúc đầu .Nhiệt lượng cung cấp cho khí trong quá trình này là 11,04 kJ. Tính công mà khí thực hiện và độ tăng nội năng.
\(\frac{T_2}{T_1}=\frac{V_2}{V_1}=1,5\) → T2 = 1,5 . 300 = 450K
Áp dụng phương trình Clapêrôn - Menđêlêép cho 2 quá trình :
pV1 = 2,5RT1
→ p(V2 - V1 ) = 2,5R( T2 - T1 )
pV2 = 2,5RT2
Vì quá trình đẳng áp → A = p\(\triangle V\) = 2,5R.\(\triangle\)T = 2,5 . 8,31 . 150
= 3116,25 J = 3,12 kJ
\(\triangle U=A+Q=-3,12+11,04=7,92kJ\)
Đúng 0
Bình luận (0)
Thôi nhá
Đừng tử hỏi tự trả lời nữa
Không ai cạnh tranh đc đâu
Đúng 0
Bình luận (0)
Lấy 2,5 mol khí lí tưởng ở nhiệt độ 300 K. Nung nóng đẳng áp khi này cho đến khi thể tích của nó bằng 1,5 lần thể tích lúc đầu. Nhiệt lượng cung cấp cho quá trình này là 11,04 kJ. Tính công mà khí này thực hiện và độ tăng nội năng. A. 5,96 kJ B. 7,92 kJ C. 6,27 kJ D. 7,01kJ
Đọc tiếp
Lấy 2,5 mol khí lí tưởng ở nhiệt độ 300 K. Nung nóng đẳng áp khi này cho đến khi thể tích của nó bằng 1,5 lần thể tích lúc đầu. Nhiệt lượng cung cấp cho quá trình này là 11,04 kJ. Tính công mà khí này thực hiện và độ tăng nội năng.
A. 5,96 kJ
B. 7,92 kJ
C. 6,27 kJ
D. 7,01kJ
Đáp án: B
Nung nóng đẳng áp:

Áp dụng phương trình Claperon- Mendeleep cho hai quá trình:
p.V1 = 2,5RT1; p.V2 = 2,5RT2
→ p.(V2 – V1) = 2,5.R.(T2 – T1)
Vì quá trình đẳng áp
→ A = p.ΔV = 2,5.R.ΔT = 2,5.8,31.150
= 3116,25J = 3,12kJ
Với quy ước dấu, khí sinh công A < 0, nhận nhiệt Q > 0.
→ ΔU = A + Q = -3,12 + 11,04 = 7,92kJ
Đúng 0
Bình luận (0)
Một lượng khí ở áp suất p = 3.105N/m2 có thể tích V1 = 10lít. Sau khi nhận được nhiệt lượng 5000J thì nó biến đổi đẳng áp, thực hiện công và nội năng tăng 2000J.
a. Tính thể tích của khí ở cuối quá trình biến đổi.
b. Nhiệt độ lúc đầu là 300C. Tính nhiệt độ cuối.
Một khối khí trong xi lanh, ban đầu thể tính V1 4,2 lít, nhiệt độ t1 27oC và áp suất 4 atm.Khí được biến đổi theo một chu trình kín gồm 3 giai đoạn.-Giai đoạn 1: dãn nở đẳng áp, thể tích tăng đến 8,4 lít-Giai đoạn 2: nén đẳng nhiệt-Giai đoạn 3:làm lạnh đẳng tíchXác định các thông số trong mỗi trạng thái. Vẽ chu trình trên trong các hệ tọa độ(p,V),(p,T),(V,T)
Đọc tiếp
Một khối khí trong xi lanh, ban đầu thể tính V1= 4,2 lít, nhiệt độ t1= 27oC và áp suất 4 atm.
Khí được biến đổi theo một chu trình kín gồm 3 giai đoạn.
-Giai đoạn 1: dãn nở đẳng áp, thể tích tăng đến 8,4 lít
-Giai đoạn 2: nén đẳng nhiệt
-Giai đoạn 3:làm lạnh đẳng tích
Xác định các thông số trong mỗi trạng thái. Vẽ chu trình trên trong các hệ tọa độ(p,V),(p,T),(V,T)











