Điện phân 100 ml dung dịch A chứa AgNO3 0,2M ; Cu(NO3)2 0,1M và Zn(NO3)2 0,15 M với cường độ dòng điện I = 1,34A trong 72 phút. Số kim loại thu được ở catot sau điện phân là :
A. 3,775g
B. 2,80g
C. 2,48g
D. 3,45g
Điện phân 100 ml dung dịch A chứa AgNO3 0,2M, Cu(NO3)2 0,1M và Zn(NO3)2 0,15M với cường độ dòng điện I = 1,34A trong 72 phút. Số gam kim loại thu được ở catot sau điện phân là:
A. 3,775 gam
B.2,48 gam
C. 2,80 gam
D.3,45 gam
Điện phân 100 ml dung dịch A chứa AgNO3 0,2M, Cu(NO3)2 0,1M và Zn(NO3)2 0,l5M với cường độ dòng điện I = 1,34 A trong 72 phút. Số gam kim loại thu được ở catot sau điện phân là
A. 3,775 gam
B. 2,80 gam
C. 2,48 gam
D. 3,45 gam
Điện phân 100 ml dung dịch A chứa AgNO3 0,2M, Cu(NO3)2 0,1M và Zn(NO3)2 0,l5M với cường độ dòng điện I = 1,34 A trong 72 phút. Số gam kim loại thu được ở catot sau điện phân là :
A. 3,45 gam.
B. 2,80 gam.
C. 3,775 gam.
D. 2,48 gam.
Cho một dòng điện có cường độ không đổi đi qua 2 bình điện phân mắc nối tiếp. Bình 1 chứa 500 ml dung dịch CuSO4(điện cực trơ), bình 2 chứa 100 ml dung dịch hỗn hợp AgNO3 0,2M; Cu(NO3)2 0,3M, Fe(NO3)3 0,1M (điện cực trơ). Sau một thời gian ngắt dòng điện, thấy bình 1 có pH =1 và catot của bình 2 tăng thêm m gam. Biết thể tích dung dịch không thay đổi trong suốt quá trình điện phân. Giá trị của m là
A. 1,72
B. 2,16
C. 3,44
D. 2,80
+/Bình 1: Tại Anot: 2H2O → 4H+ + O2 + 4e
Do pH = 1 => n H+ = 0,1.0,5 = 0,05 mol
Do 2 bình mắc nối tiếp nên I1 = I2 => số mol e trao đổi như nhau ở 2 bình
=> n e trao đổi = 0,05 mol
+/Bình 2: Tại Catot : Fe3+ + 1e → Fe2+ Ag+ + 1e → Ag Cu2+ + 2e → Cu
=> m = m Ag + m Cu = 108.0,02 + 64.0,01 =2,8g
=>D
Điện phân 100 ml dung dịch hỗn hợp Cu(NO3)2 0,2M và AgNO3 0,1M (điện cực trơ, hiệu suất điện phân 100%) với cường độ dòng điện không đổi 3,86A. Thời gian điện phân đến khi thu được 1,72 gam kim loại ở catot là t giây. Giá trị của t là
A. 250
B. 750
C. 1000
D. 500
Câu 16: Cho một lượng dư dung dịch AgNO3 tác dụng với 100 ml dung dịch chứa hỗn hợp NaF 0,4M; NaBr 0,5M và NaCl 0,2M . Khối lượng kết tủa thu được là bao nhiêu
\(AgNO_3 + NaBr \to AgBr + NaNO_3\\ AgNO_3 + NaCl \to AgCl + NaNO_3\\ n_{AgBr} = n_{NaBr} = 0,1.0,5 = 0,05(mol)\\ n_{AgCl} = n_{NaCl} = 0,1.0,5 = 0,05(mol)\\ \Rightarrow m_{kết\ tủa} = m_{AgCl} + m_{AgBr} = 0,05.143,5 + 0,05.188 = 16,575(gam)\)
Dung dịch X thu được khi trộn một thể tích dung dịch H2SO4 0,1M với một thể tích dung dịch HCl 0,2M. Dung dịch Y chứa NaOH 0,2M và Ba(OH)2 0,1M. Đổ 100 ml dung dịch X vào 100 ml dung dịch Y , khuấy đều để phản ứng xảy ra hoàn toàn thu được 200 ml dung dịch X có pH = a và m gam kết tủa Y ( Coi H2SO4 điện ly hoàn toàn cả 2 nấc). Giá trị của a và m lần lượt là :
A. 13 và 1,165
B. 7 và 2,330
C. 1 và 2,330
D. 7 và 1,165
Đáp án : A
dd X : nH+ = 2nH2SO4 + nHCl = 0,02 mol
dd Y : nOH = nNaOH + 2nBa(OH)2 = 0,04 mol
=> Trong Y : nOH – nH+ = 0,02 mol = nOH- => COH = 0,1M => pH = 13
Nhỏ từ từ dung dịch đến dư Ba OH 2 0,2M vào 100 ml dung dịch A chứa Al 2 SO 4 3 xM. Mối quan hệ giữa khối lượng kết tủa và số mol OH - được biểu diễn bằng đồ thị sau:
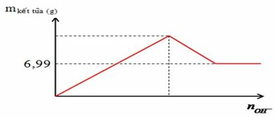
Nếu cho 100 ml dung dịch hỗn hợp Ba OH 2 0,2M và NaOH 0,3M vào 100 ml dung dịch A thì khối lượng kết tủa thu được là bao nhiêu?
A. 5,44 gam
B. 4,66 gam
C. 5,70 gam
D. 6,22 gam
Nhỏ từ từ đến dư dung dịch Ba(OH)2 0,2M vào 100 ml dung dịch A chứa Al2(SO4)3 xM. Mối quan hệ giữa khối lượng kết tủa và số mol OH- được biểu diễn bằng đồ thị sau:

Nếu cho 100 ml dung dịch hỗn hợp Ba(OH)2 0,2M và NaOH 0,3M vào 100 ml dung dịch A thì khối lượng kết tủa thu được là
A. 5,44 gam
B. 4,66 gam
C. 5,70 gam
D. 6,22 gam