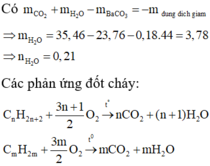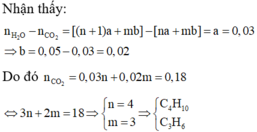chất gì nhiệt phân ra ba sản phẩm trong đó có 2 chất là O2 và H2O

Những câu hỏi liên quan
Để đốt cháy hoàn toàn 2,50 g chất A phải dùng vừa hết 3,36 lít
O
2
(đktc). Sản phẩm cháy chỉ có
C
O
2
và
H
2
O
, trong đó khối lượng
C
O
2
hơn khối lượng
H
2
O
là 3,70 g. Tính phần trăm khối lượng của từng nguyên tố tron...
Đọc tiếp
Để đốt cháy hoàn toàn 2,50 g chất A phải dùng vừa hết 3,36 lít O 2 (đktc). Sản phẩm cháy chỉ có C O 2 và H 2 O , trong đó khối lượng C O 2 hơn khối lượng H 2 O là 3,70 g. Tính phần trăm khối lượng của từng nguyên tố trong chất A.
Khi A tác dụng với O 2 chỉ sinh ra, và H 2 O , vậy A có chứa cacbon, hiđro, có thể có hoặc không có oxi.
Theo định luật bảo toàn khối lượng :
m C O 2 + m H 2 O = m A + m O 2 = 7,30 (g) (1)
Theo đầu bài: m C O 2 + m H 2 O = 3,70(g). (2)
Từ hệ (1) và (2), tìm được m C O 2 = 5,50 g; m H 2 O = 1,80 g.
Khối lượng C trong 5,50 g
C
O
2
: 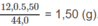
Khối lượng H trong 1,8 g
H
2
: 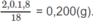
Đó cũng là khối lượng c và H trong 2,50 g chất A. Vậy chất A phải chứa O.
Khối lượng O trong 2,50 g A: 2,50 - 1,50 - 0,200 = 0,80 (g)
Phần trăm khối lượng của C: 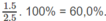
Phần trăm khối lương của H: 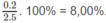
Phần trăm khối lương của O: 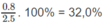
Đúng 0
Bình luận (0)
ĐỀ CƯƠNG ÔN TẬP A. Trắc nghiệmCâu 1. Sản phẩm của phản ứng phân huỷ Fe(OH)3 bởi nhiệt là :A. FeO và H2O B. Fe2O3 và H2O C. Fe2O3 và H2 D. FeO và H2 Câu 2: Trong số các chất sau đây, chất nào là axit? A. Ca(OH)2 B. CaCO3 C. CaO D. H2SO4 Câu 3: Dung dịch làm phenolphtalein không màu thành màu hồng là A. Ba(OH)2 B. HCl ...
Đọc tiếp
ĐỀ CƯƠNG ÔN TẬP
A. Trắc nghiệm
Câu 1. Sản phẩm của phản ứng phân huỷ Fe(OH)3 bởi nhiệt là :
A. FeO và H2O B. Fe2O3 và H2O C. Fe2O3 và H2 D. FeO và H2
Câu 2: Trong số các chất sau đây, chất nào là axit?
A. Ca(OH)2 B. CaCO3 C. CaO D. H2SO4
Câu 3: Dung dịch làm phenolphtalein không màu thành màu hồng là
A. Ba(OH)2 B. HCl C. NaCl D. K2SO4
Câu 4: Bazơ nào sau đây bị nhiệt phân hủy?
A. Cu(OH)2 B. NaOH C. Ca(OH)2 D. KOH
Câu 5. Cho dung dịch BaCl2 tác dụng với dung dịch Na2SO4 có hiện tượng gì ?
A. Xuất hiện kết tủa màu trắng B. Không có hiện tượng gì
C. Xuất hiện kết tủa màu xanh D. Có kết tủa màu đỏ
Câu 6. Điều kiện để muối tác dụng với muối là:
A. Không có điều kiện gì. B. Tạo muối mới và axit mới không tan.
C. Tạo muối mới và bazơ mới không tan D. Ít nhất một muối tạo thành không tan Câu 7: Chất nào sau đây tác dụng được với nước ở nhiệt độ thường?
A. Fe2O3 B. CuO C. SO2 D. MgO
Câu 8: Natri clorua có nhiều trong nước biển, được dùng để sản xuất muối ăn. Công thức của natri clorua là
A. KCl B. CaCl2 C. NaCl D. Na2SO4
Câu 9: Có các loại phân bón hóa học sau: CO(NH2)2; KCl; Ca(H2PO4)2; K2SO4. Chất thuộc loại phân đạm là
A. KCl B. CO(NH2)2 C. Ca(H2PO4)2 D. K2SO4
Câu 10: Chất không tác dụng với dung dịch H2SO4 là
A. Na2SO4 B. CaCO3 C. Na2SO3 D. BaCl2
Câu 11: Trong số các chất sau đây, chất nào là muối?
A. Ca(OH)2 B. CaCO3 C. CaO D. H2SO4
Câu 12. Dãy các chất phản ứng với nước ở điều kiện thường là
A. SO2, CuO, Na2O, P2O5. B. NO, CaO, SO3, N2O5
C. SO2, K2O, BaO, SO3 D. N2O5, Fe2O3, CuO, P2O5
Câu 13: Chất làm giấy quỳ tím ẩm hoá đỏ là
A. Na2O B. SO2 C. CO D. Fe2O3
Câu 14. Muối nào sau đây tác dụng được với dung dịch NaOH ?
A. BaCO3 B. K2CO3 C. CuSO4 D. CaCO3
Câu 15: Dãy gồm các chất đều phản ứng với dung dịch NaOH là
A. SO2 ; CO2; SO3. B. Fe2O3; Al2O3; CO2.
C. CO2; N2O5; CO. D. N2O5; BaO; CuO.
Câu 16: Cặp chất nào sau đây phản ứng với nhau tạo ra sản phẩm khí ?
A. Dung dịch Na2SO4 và dung dịch BaCl2. B. Dung dịch Na2CO3 và dung dịch HCl.
C. Dung dịch KOH và dung dịch MgCl2. D. Dung dịch KCl và dung dịch AgNO3.
Câu 17: Dãy chất nào sau đây chỉ có muối?
A. NaCl, CuSO4, BaO, KMnO4 B. KMnO4, Na2SO4, CuCl2, Ba(NO3)2
C. FeCl3, NaOH, AgNO3, Na2S D. MgSO4, BaCl2, Cu(NO3)2, Al2O3
Câu 18: Trong dung dịch, cặp chất nào sau đây không có phản ứng xảy ra
A. NaOH và MgCl2 B. CaCl2 và KCl C. FeCl3 và KOH D. Na2SO4 và BaCl2
Câu 19: Khí SO2 được tạo thành từ phản ứng giữa cặp chất nào sau đây.
A. Na2SO3 và H2SO4 B. Na2SO4 và H2SO3
C. Na2CO3 và H2SO4 D. A. K2SO3 và H2SO3
Câu 20: Chất nào sau đây không bị nhiệt phân hủy?
A. KClO3 B. NaCl C. CaCO3 D. KMnO4
B. Tự luận
Câu 1: Hoàn thành sơ đồ chuyển hóa sau, ghi rõ điều kiện phản ứng nếu có:
a) Na2O NaOH Cu(OH)2 CuO CuSO4
b) FeCl3 Fe(OH)3 Fe2O3 Fe2(SO4)3 FeCl3
b) Cu CuO CuSO4 Cu(OH)2 CuCl2
Câu 2: Viết PTHH (nếu có) khi cho dung dịch:
a) axit HCl lần lượt tác dụng với:
Zn; MgO; Fe(OH)3; dung dịch AgNO3.
b) axit H2SO4 loãng lần lượt tác dụng với:
Fe; ZnO; Cu(OH)2; dung dịch BaCl2.
c) Na2 CO3 lần lượt tác dụng với:
Ca(OH)2; dung dịch BaCl2; HCl
-------------------------------------------------------
Tự luận:
Câu 1 :
a, \(Na_2O+H_2O\rightarrow2NaOH\)
\(2NaOH+CuSO_4\rightarrow Na_2SO_4+Cu\left(OH\right)_2\)
\(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
b, \(FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\)
\(2Fe\left(OH\right)_3\rightarrow\left(t^o\right)Fe_2O_3+3H_2O\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
\(Fe_2\left(SO_4\right)_3+3BaCl_2\rightarrow2FeCl_3+3BaSO_4\)
\(c,2Cu+O_2\underrightarrow{t^o}2CuO\)
\(CuO+H_2SO_4\rightarrow CuSO_4\rightarrow H_2O\)
\(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
\(Cu\left(OH\right)_2+2HCl\rightarrow CuCl_2+2H_2O\)
Đúng 2
Bình luận (0)
Trong một bình kín có dung tích là 20 lít có chứa hỗn hợp X gồm 2 chất hữu cơ có công thức phân tử lần lượt là CnH2n+2 và CmH2m và 9,6 gam O2. Nhiệt độ trong bình lúc này là 0°C và áp suất là 0,392 atm. Đốt cháy hết hỗn hợp A trong bình, giữ nhiệt độ trong bình là 136,5°C và áp suất là p atm. Cho sản phẩm cháy vào dung dịch Ba(OH)2 dư, thu được 35,46 gam kết tủa và khối lượng dung dịch giảm 23,76 gam. Công thức phân tử của hai chất trong hỗn hợp X là A. C3H6 và C4H10 B. C3H8 và C4H8 C. C3H6 và...
Đọc tiếp
Trong một bình kín có dung tích là 20 lít có chứa hỗn hợp X gồm 2 chất hữu cơ có công thức phân tử lần lượt là CnH2n+2 và CmH2m và 9,6 gam O2. Nhiệt độ trong bình lúc này là 0°C và áp suất là 0,392 atm. Đốt cháy hết hỗn hợp A trong bình, giữ nhiệt độ trong bình là 136,5°C và áp suất là p atm. Cho sản phẩm cháy vào dung dịch Ba(OH)2 dư, thu được 35,46 gam kết tủa và khối lượng dung dịch giảm 23,76 gam. Công thức phân tử của hai chất trong hỗn hợp X là
A. C3H6 và C4H10
B. C3H8 và C4H8
C. C3H6 và C3H8
D. C2H4 và C4H10
Đốt cháy hoàn toàn amin đơn chức E bằng khí
O
2
vừa đủ. Dẫn toàn bộ sản phẩm cháy (gồm
C
O
2
,
H
2
O
và
N
2
) qua bình đựng dung dịch
B
a
(
O
H
)
2
dư, khối lượ...
Đọc tiếp
Đốt cháy hoàn toàn amin đơn chức E bằng khí O 2 vừa đủ. Dẫn toàn bộ sản phẩm cháy (gồm C O 2 , H 2 O và N 2 ) qua bình đựng dung dịch B a ( O H ) 2 dư, khối lượng bình tăng 7,78 gam và có 27,58 gam kết tủa; chất khí thoát ra khỏi bình có thể tích 0,224 lít (đktc). Công thức phân tử của E là
A. C 6 H 7 N
B. C 2 H 7 N
C. C 3 H 9 N
D. C 7 H 9 N
Hỗn hợp X chứa ba chất hữụ cơ đồng phân. Nếu làm bay hơi 2,10 g X thì thể tích hơi thu được bằng thể tích của 1,54 g khí
C
O
2
ở cùng điều kiện. Để đốt cháy hoàn toàn 1,50 g X cần dùng vừa hết 2,52 lít
O
2
(đktc). Sản phẩm cháy chỉ có
C
O
2
và
H
2
O
theo tỉ lệ 11 : 6 về khối lượng.1. Xác định cô...
Đọc tiếp
Hỗn hợp X chứa ba chất hữụ cơ đồng phân. Nếu làm bay hơi 2,10 g X thì thể tích hơi thu được bằng thể tích của 1,54 g khí C O 2 ở cùng điều kiện. Để đốt cháy hoàn toàn 1,50 g X cần dùng vừa hết 2,52 lít O 2 (đktc). Sản phẩm cháy chỉ có C O 2 và H 2 O theo tỉ lệ 11 : 6 về khối lượng.
1. Xác định công thức phân tử của ba chất trong X.
2. Dựa vào thuyết cấu tạo hoá học, hãy viết công thức cấu tạo (triển khai và rút gọn) của từng chất đó.
Ba chất đồng phân có công thức phân tử giống nhau. Đốt X ta chỉ được C O 2 và H 2 O , vậy các chất trong X có chứa C, H và có thể có chứa O.
Theo định luật bảo toàn khối lượng :
m C O 2 + m H 2 O = m X + m O 2 = 5,1(g)
Mặt khác mCO2: mH2O = 11:6
Từ đó tìm được: m C O 2 = 3,30 g và m H 2 O = 1,80 g
Khối lượng C trong 3,30 g
C
O
2
: 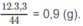
Khối lương H trong 1,80 g
H
2
O
: 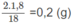
Khối lượng O trong 1,50 g X : 1,50 - 0,9 - 0,2 = 0,4 (g).
Các chất trong X có dạng C x H y O z
x : y : z = 0,075 : 0,2 : 0,025 = 3 : 8 : 1.
Công thức đơn giản nhất là C 3 H 8 O .
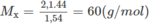
⇒ CTPT cũng là C 3 H 8 O .
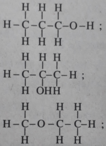
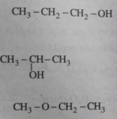
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 0,1 mol chất hữu cơ X mạch hở cần dùng 5,04 lít khí O2 (đktc). Dẫn toàn bộ sản phẩm cháy gồm CO2, H2O và N2 qua bình đựng dung dịch Ba(OH)2 dư, thấy khối lượng bình tăng 13,3 gam và có 39,4 gam kết tủa. Khí thoát ra khỏi bình có thể tích 1,12 lít (đktc). Công thức phân tử của X là: A. C3H5O2N B. C3H7O2N C. C2H5O2N D. C2H7O2N
Đọc tiếp
Đốt cháy hoàn toàn 0,1 mol chất hữu cơ X mạch hở cần dùng 5,04 lít khí O2 (đktc). Dẫn toàn bộ sản phẩm cháy gồm CO2, H2O và N2 qua bình đựng dung dịch Ba(OH)2 dư, thấy khối lượng bình tăng 13,3 gam và có 39,4 gam kết tủa. Khí thoát ra khỏi bình có thể tích 1,12 lít (đktc). Công thức phân tử của X là:
A. C3H5O2N
B. C3H7O2N
C. C2H5O2N
D. C2H7O2N
Đáp án C
Ta có mBình tăng = mCO2 + mH2O = 13,3 gam.
Với nCO2 = nBaCO3 = 0,2 mol ||⇒ nH2O = 0,25 mol.
Nhận thấy nC ÷ nH = 0,2 ÷ (0,25×2) = 2 ÷ 5
Đúng 0
Bình luận (0)
Hỗn hợp A gồm metan và một hợp chất hữu cơ X. Tỉ khối hơi của X so với hiđro nhỏ hơn 18. Đốt cháy hoàn toàn V lít A thu được sản phẩm chỉ gồm CO2 và H2O. Cho sản phẩm cháy hấp thụ hết vào dung dịch Ba(OH)2 lấy dư thấy tạo thành 70,92 gam kết tủa. Xác định các công thức phân tử có thể có của X. Biết rằng: V lít A đúng bằng thể tích của 11,52 gam khí O2 được đo trong cùng điều kiện nhiệt độ và áp suất.
Đọc tiếp
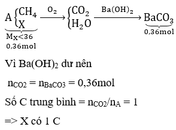
Hỗn hợp A gồm metan và một hợp chất hữu cơ X. Tỉ khối hơi của X so với hiđro nhỏ hơn 18. Đốt cháy hoàn toàn V lít A thu được sản phẩm chỉ gồm CO2 và H2O. Cho sản phẩm cháy hấp thụ hết vào dung dịch Ba(OH)2 lấy dư thấy tạo thành 70,92 gam kết tủa. Xác định các công thức phân tử có thể có của X. Biết rằng: V lít A đúng bằng thể tích của 11,52 gam khí O2 được đo trong cùng điều kiện nhiệt độ và áp suất.
Cho các chất tham gia phản ứng: (1): S+ F2 (2): SO2 + H2S (3): SO2 + O2 (4): S+H2SO4(đặc,nóng) (5): H2S + Cl2 (dư ) + H2O (6): FeS2 + HNO3 Khi các điều kiện xúc tác và nhiệt độ có đủ, số phản ứng tạo ra sản phẩm mà lưu huỳnh ở mức số oxi hoá +6 là A. 4. B. 5. C. 2. D. 3.
Đọc tiếp
Cho các chất tham gia phản ứng:
(1): S+ F2
(2): SO2 + H2S
(3): SO2 + O2
(4): S+H2SO4(đặc,nóng)
(5): H2S + Cl2 (dư ) + H2O
(6): FeS2 + HNO3
Khi các điều kiện xúc tác và nhiệt độ có đủ, số phản ứng tạo ra sản phẩm mà lưu huỳnh ở mức số oxi hoá +6 là
A. 4.
B. 5.
C. 2.
D. 3.
Chọn đáp án A
Các phản ứng thỏa mãn : (1)(3) (5)(6)
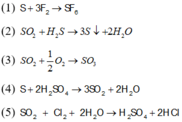
![]()
![]()
Đúng 0
Bình luận (0)
6. Đốt cháy 6,72 lít khí C2H2 (đktc) trong bình chứa 11,2 lít khí O2
(đktc), tạo ra sản phẩm là CO2 và H2O. theo pư:
C2H2 + O2 ⎯⎯to→ CO2 + H2O
Hỏi sau khi phản ứng xong khí C2H2 có cháy hết không? Tính khối
lượng các chất có sau phản ứng
$n_{C_2H_2} = \dfrac{6,72}{22,4} = 0,3(mol) ; n_{O_2} = 0,5(mol)$
$2C_2H_2 + 5O_2 \xrightarrow{t^o} 4CO_2 + 2H_2O$
Ta thấy :
$n_{C_2H_2} : 2 > n_{O_2} : 5$ nên $C_2H_2$ dư
Theo PTHH :
$n_{C_2H_2\ pư} = \dfrac{5}{2} = 0,2(mol)$
$n_{CO_2} = 0,4(mol) ; n_{H_2O} = 0,2(mol)$
Suy ra :
$m_{C_2H_2\ dư} = (0,3 - 0,2).26 = 2,6(gam)$
$m_{CO_2} = 0,4.44 = 17,6(gam)$
$m_{H_2O} = 0,2.18 = 3,6(gam)$
Đúng 2
Bình luận (1)